诺华制药公司近日表示,美国FDA加快了对Tabrecta(capmatinib)申请的审批,以治疗转移性非小细胞肺癌(NSCLC)的成年患者,这些患者肿瘤的突变导致MET的14号外显子跳跃(METex14)。
FDA的决定是基于一项关键性、非随机性的II期GEOMETRY mono-1临床试验的最新结果,该试验评估了每天两次接受Tabrecta(capmatinib)治疗的97名METex14局部晚期或转移性NSCLC患者。结果显示,先前未经治疗的患者的总体缓解率(ORR)为68%,反应持续时间为12.6个月;而先前接受过治疗的患者的总体缓解率(ORR)为41%,反应持续时间为9.7个月。常见的与治疗相关的不良反应事件为水肿、恶心、疲劳、呕吐、呼吸困难和食欲下降。
目前,非小细胞肺癌(non-small cell lung cancer, NSCLC)仍然是人类死亡率最高的恶性肿瘤之一,已经成为严重威胁人们生命健康的社会问题。

原始出处:
https://www.firstwordpharma.com/node/1721926?tsid=4
姚煜教授:抗血管生成单抗联合TKI治疗有望成为EGFR 21L858R突变晚期NSCLC治疗金标准
![]() 0
2020-04-09
点击查看
0
2020-04-09
点击查看

AACR 2020:大样本NSCLC中的FGFR基因突变结果发布
![]() 0
2020-04-28
点击查看
0
2020-04-28
点击查看

AACR 2020:Durvalumab治疗III期不可切除NSCLC的吸烟状态亚组分析
![]() 0
2020-04-29
点击查看
0
2020-04-29
点击查看

AACR 2020:Capmatinib治疗MET 14突变的NSCLC脑转移疗效
![]() 0
2020-04-29
点击查看
0
2020-04-29
点击查看

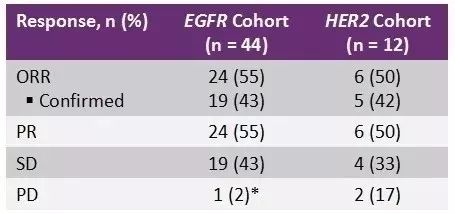
AACR 2020:波奇替尼治疗NSCLC的EGFR 20ins的II期研究
![]() 0
2020-04-29
点击查看
0
2020-04-29
点击查看
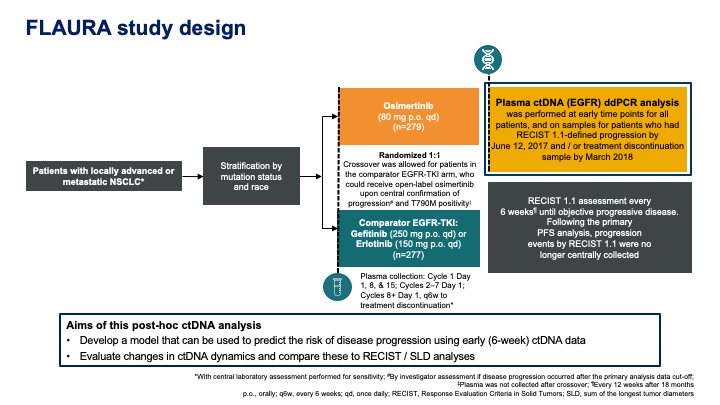
AACR 2020:基于ctDNA的复合型预测模型有效预测EGFR突变阳性晚期NSCLC一线治疗PFS(FLAURA研究)
![]() 0
2020-05-01
点击查看
0
2020-05-01
点击查看