Circ Cardiovasc Imaging:使用心脏磁共振评估南美锥虫病右心室收缩功能!
![]() 0
2017-03-20
点击查看
0
2017-03-20
点击查看
Eur Respir J:早期联合治疗降低肺动脉高压右心室容积!
![]() 0
2017-07-09
点击查看
0
2017-07-09
点击查看
JAMA Cardiol:右心室功能障碍的心力衰竭患者预后较差
![]() 0
2018-08-23
点击查看
0
2018-08-23
点击查看
Pulm Circ:视网膜血管变化和右心室结构和功能综合研究
![]() 0
2019-01-19
点击查看
0
2019-01-19
点击查看

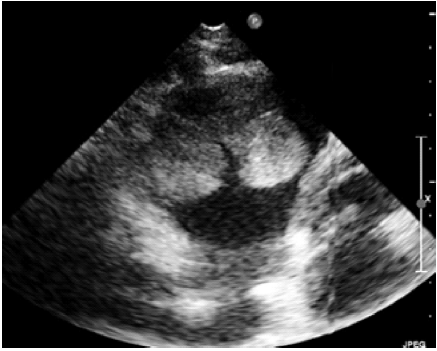
超声心动图诊断右心室黏液瘤1例
![]() 0
2019-03-17
点击查看
0
2019-03-17
点击查看
Int J Cardiol:右心室收缩期与舒张期持续时间比值为PAH成人的预后因素
![]() 0
2019-05-08
点击查看
0
2019-05-08
点击查看
