许多65岁或以上的晚期前列腺癌患者因担心化疗的毒性而未接受过化疗,在75岁或以上的患者中,标准剂量的多西他赛和卡巴他赛化疗方案通常与更多的不良事件和因不良事件而停药相关,尽管这些化疗方案可以为老年患者带来生存优势。卡巴他赛相比多西他赛可以减少脱发、外周神经病变、外周水肿和指甲病变的发生,但卡巴他赛与严重中性粒细胞减少的高发生率相关,通过降低卡巴他赛剂量或从化疗周期1开始预防性使用G-CSF,可以部分降低中性粒细胞减少性并发症的风险,但这一风险在65岁或以上的晚期前列腺癌患者中仍是一个挑战,改变给药方案是进一步降低严重中性粒细胞减少及其并发症发生率的一种策略。先前的研究表明,多西他赛50 mg/m2每2周给药的方案与标准方案(75 mg/m2每3周给药)相比,在疗效相当的情况下耐受性更好。在这一背景下,进行了小样本研究,结果显示每2周16 mg/m2卡巴他赛给药的方案保留了活性,并降低了严重中性粒细胞减少的发生率,因此,开展了CABASTY临床试验,旨在比较这一每2周给药的卡巴他赛方案与标准每3周给药的方案在老年晚期前列腺癌患者中的疗效和安全性。

方法
CABASTY临床试验采用了前瞻性开放标签随机对照研究的方法,将196名65岁或以上的晚期前列腺癌患者随机分为两组,一组接受卡巴他赛16 mg/m2每周两次,另一组接受卡巴他赛25 mg/m2每周三次,两组均从化疗周期1开始预防性使用G-CSF,同时每天口服泼尼松10 mg。主要研究终点是3级或以上中性粒细胞减少和/或中性粒细胞减少性并发症的发生率,次要研究终点包括卡巴他赛剂量减少和延迟、总生存期、无进展生存期、PSA反应率、肿瘤反应率等。
研究结果
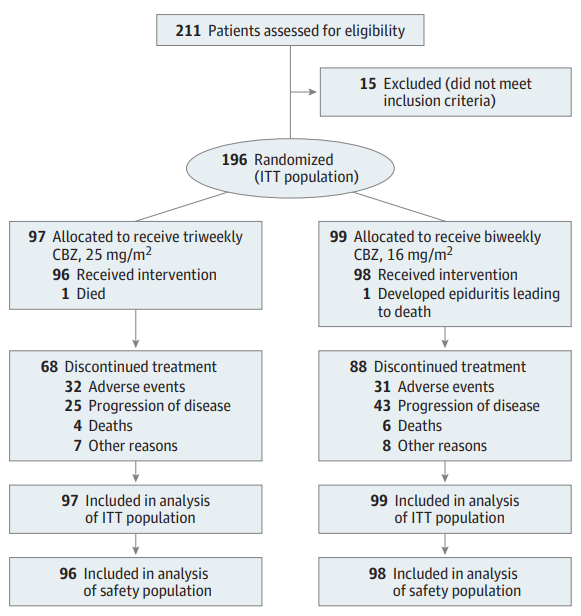
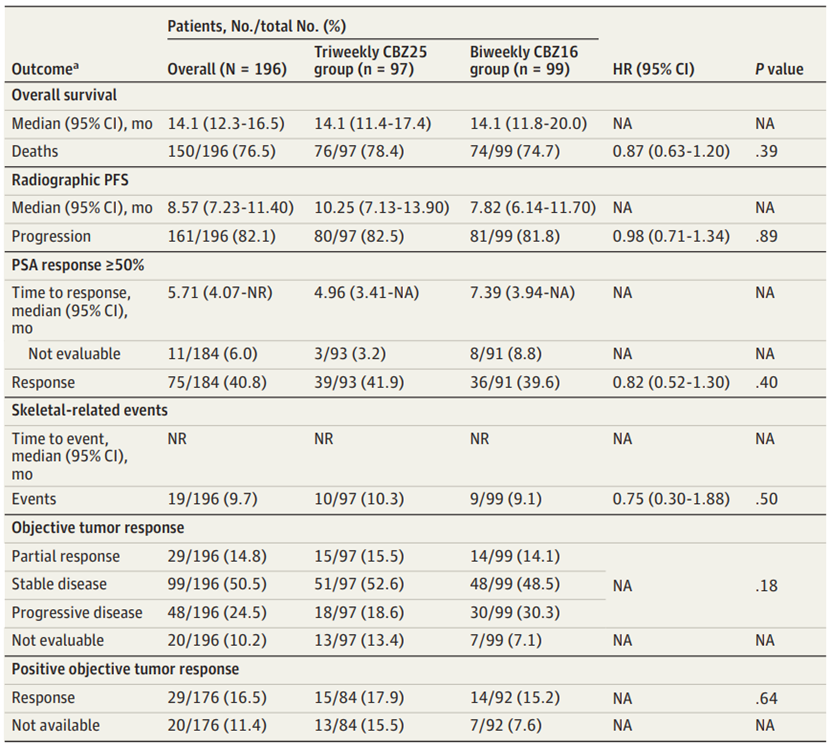
在196名患者中,97名被随机分配到每周三次卡巴他赛25 mg/m2组,99名被随机分配到每周两次卡巴他赛16 mg/m2组。两组患者的中位年龄为74.6岁。在安全人群中,每周三次卡巴他赛25 mg/m2组3级或以上中性粒细胞减少和/或中性粒细胞减少性并发症的发生率为62.5%,而每周两次卡巴他赛16 mg/m2组的发生率为5.1%,具有显著差异(OR=0.03, 95% CI 0.01-0.08, P<0.001),两组的中位总生存期均为14.1个月,无显著差异,两组的无进展生存期、PSA反应率、肿瘤反应率也无显著差异,每周三次卡巴他赛25 mg/m2组的3级或以上不良事件发生率更高(72.9% vs 56.1%),但两组因不良事件而永久停药的比例相近(33.3% vs 31.6%),在两组中,每周两次卡巴他赛16 mg/m2组的严重中性粒细胞减少或中性粒细胞减少性并发症发生率显著降低12倍,这为老年晚期前列腺癌患者提供了一种更安全的治疗选择。


结论
与标准方案相比,每周两次卡巴他赛16 mg/m2方案显著降低了老年晚期前列腺癌患者3级或以上中性粒细胞减少或中性粒细胞减少性并发症的发生风险。在老年晚期前列腺癌患者中,两种卡巴他赛方案的疗效相当,总生存期和无进展生存期没有显著差异,每周两次卡巴他赛16 mg/m2方案的安全性优于标准方案,严重中性粒细胞减少或中性粒细胞减少性并发症的发生率显著降低,对于65岁或以上的晚期前列腺癌患者,标准卡巴他赛方案不适合时,建议采用每周两次卡巴他赛16 mg/m2方案,该研究结果为老年晚期前列腺癌患者提供了更安全的治疗选择,并有望改变临床实践。
原始出处
Oudard S, Ratta R, Voog E, et al. Biweekly vs Triweekly Cabazitaxel in Older Patients With Metastatic Castration-Resistant Prostate Cancer: The CABASTY Phase 3 Randomized Clinical Trial. JAMA Oncol. 2023;9(12):1629–1638. doi:10.1001/jamaoncol.2023.4255.
Br J Sports Med:男性心肺功能变化与前列腺癌发病率和死亡率之间的关系
![]() 0
2024-02-16
点击查看
0
2024-02-16
点击查看

Cancer Metab | 高脂肪饮食通过RPS27促进前列腺癌转移
![]() 0
2024-02-19
点击查看
0
2024-02-19
点击查看

Cancer | 植物性饮食与前列腺癌患者更好的生活质量相关
![]() 0
2024-02-26
点击查看
0
2024-02-26
点击查看
BRCA2突变mCRPC患者PARP抑制剂及铂类耐药,尸检多部位基因检测大揭秘
![]() 0
2024-03-07
点击查看
0
2024-03-07
点击查看

论文解读|Dong S/ Li J/ Sun Z教授团队发现拮抗前列腺癌细胞外泌体miR-18a-5改善骨转移导致的成骨细胞病变
![]() 0
2024-03-15
点击查看
0
2024-03-15
点击查看

JCO:FDA批准他拉唑帕利联合恩杂鲁胺用于治疗HRR基因突变的晚期去势抵抗性前列腺癌
![]() 0
2024-03-13
点击查看
0
2024-03-13
点击查看