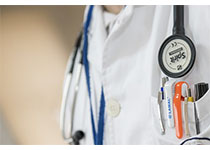
Lung Cancer:安罗替尼可改善晚期非小细胞肺癌患者的生活质量
![]() 0
2018-05-31
点击查看
0
2018-05-31
点击查看
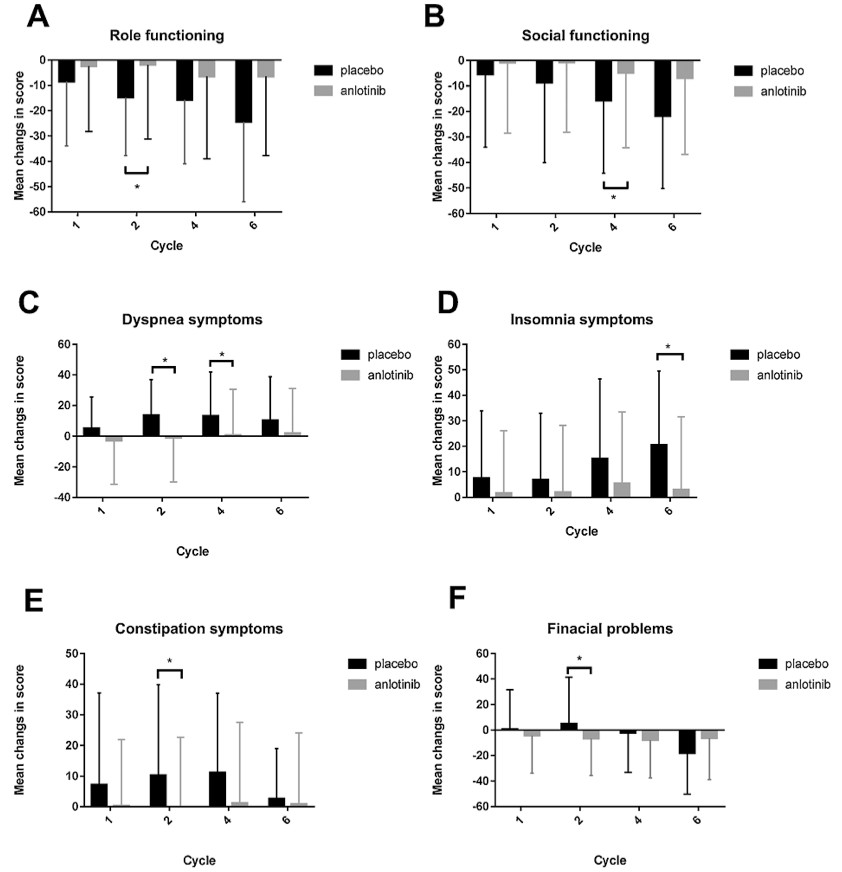
Nat Med:张泽民研究组与合作者发表单细胞水平的肺癌 T 淋巴细胞免疫图谱
![]() 0
2018-06-27
点击查看
0
2018-06-27
点击查看
CLIN CANCER RES:Ensartinib(X-396)治疗ALK阳性非小细胞肺癌
![]() 0
2018-06-29
点击查看
0
2018-06-29
点击查看
NCCN临床实践指南:非小细胞肺癌(2018.V5)
![]() 0
2018-06-30
点击查看
0
2018-06-30
点击查看
CLIN CANCER RES:KEAP1和NFE2L2突变非小细胞肺癌临床病理特征
![]() 0
2018-07-04
点击查看
0
2018-07-04
点击查看

CLIN CANCER RES:非小细胞肺癌患者Osimertinib耐药机制
![]() 0
2018-07-05
点击查看
0
2018-07-05
点击查看