近几年,长链非编码RNA(LncRNA)已成为科研领域瞩目的研究热点,对应的研究亦发表在多种高水平杂志上,目前LncRNA的文章数量逐年上升,研究模式也逐渐完善。铁死亡可以说是老生常谈了,这两个热点联系在一起能够发表在11分+水平的杂志,今天就为大家解读这篇文章。

一、研究背景
腹膜转移(PM)是胃癌(GC)远处转移的主要部位,预后和生存率极差。缺氧是腹膜转移的共同特征,缺氧诱导因子 1 α (HIF-1α) 的上调可能是 PM 发生的潜在驱动因素。铁死亡是最近发现的一种受调控的细胞死亡形式,与肿瘤的发生和发展密切相关。然而,将 HIF-1α 与 GC 的 PM 中的铁死亡联系起来的潜在机制仍然未知。作者研究了PM中差异表达的lncRNA, 并研究其具体功能,为 GC 中 PM 的潜在诊断生物标志物和治疗靶点提供了理论支持。
二、研究方法及结果
样本来源:胃腺癌患者样本
动物实验:慢病毒感染细胞,注射到小鼠体内构建肿瘤模型。
细胞实验:GES-1 和 GC 细胞系
生物信息分析:LncRNA microarrays 、 lncRNA 文库构建/lncRNA-seq
功能以及机制验证实验:免疫组化、透射电镜、免疫荧光、FISH、RIP、CHIP、质谱分析、RNA pull-down、mRNA稳定性分析、Lipid ROS assays、Iron assays、 Cell proliferation、 GSH/GSSG、cell viability measurement、Dual-luciferase assays、RT-qPCR、Western Blot
Figure1:首先作者分析的是,胃癌中远端腹膜转移的细胞中HIF-1α的表达。因为缺氧是腹膜转移的驱动因素,所以分析了一下是否会有缺氧诱导因子被激活,然后验证腹膜转移的胃癌细胞中高表达的LncRNA(命名为PMAN)并确认了其与HIF1α的表达相关性。
Figure2:作者阐明了HIF-1α激活PMAN的机制,进一步应用生物信息学分析PMAN的启动子上的HIF1α转录结合位点。证实 HIF-1α 与 PMAN 启动子内源性 HRE 位点的直接结合,进一步说明了HIF-1α可以在缺氧期间在转录水平上诱导PMAN。(经典研究思路)
Figure 3:推测由 HIF-1α 激活的 PMAN 参与了铁死亡,通过敲低过表达PMAN观察肿瘤细胞的铁死亡表型,发现PMAN 可抑制 GC 细胞中的铁死亡。(引入研究热点)
Figure 4-5:验证LncRNA的功能与铁死亡之间的关系。对铁死亡相关的几个基因,在PMAN过表达及敲减的条件下,进行了表达的分析,发现肿瘤中SLC7A11的表达量会增加,特别是腹膜转移的肿瘤细胞,SLC7A11表达也升高。接着作者继续分析PMAN 调控 SLC7A11 的机制,发现发现SLC7A11的蛋白并没有受到PMAN的影响,而PMAN能维持SLC7A11的mRNA稳定性。由于lncRNA 通常通过与RNA Binding Protein (RBP) 结合来发挥其调节功能PMAN于是他们找到了ELAVL1这个蛋白,并且发现PMAN过表达会导致ELAVL1的胞质易位。
Figure 6-7:详细研究ELAVL1通过维持SLC7A11的mRNA稳定性,抑制肿瘤细铁死亡的机制。(热点:表观遗传)
Figure 9:应用于临床诊断与检测,提高意义。上面这些验证,把“缺氧环境→HIF1α激活→PMAN转录→ELAVL1胞质易位→SLC7A11mRNA稳定性提高”串联起来了。接着他们做了体内验证,来证明PMAN对于肿瘤的影响,证明 PMAN 在体内促进肿瘤的发生和发展。
三、总结
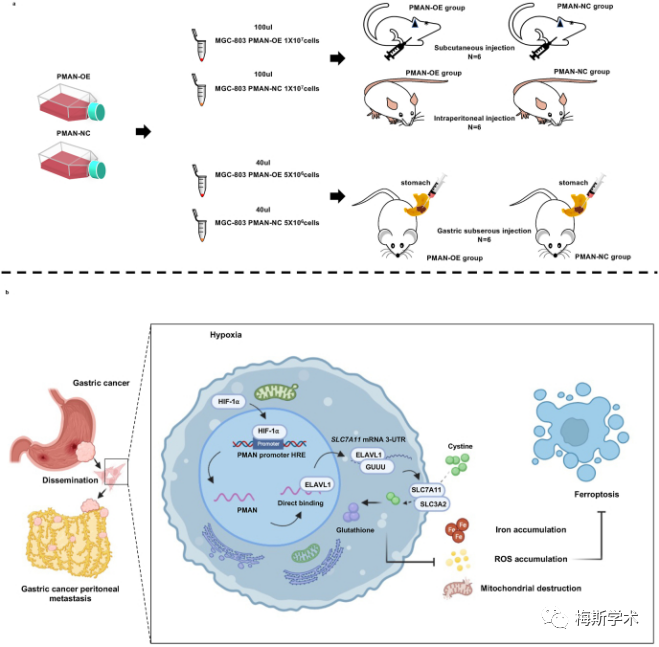
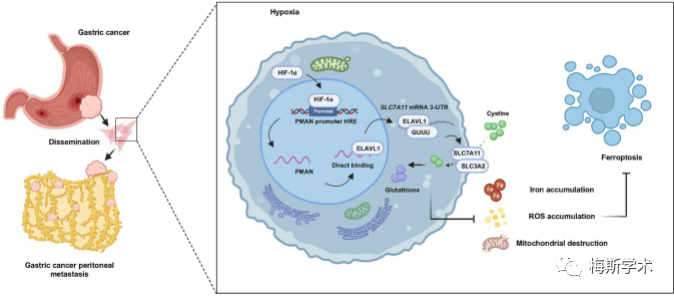
在缺氧条件下,HIF-1α 可以作为 GC 细胞中铁死亡的保护因子。HIF-1α 在转录水平激活 PMAN,从而大大提高了 ELAVL1 在细胞质中的输出。ELAVL1直接与SLC7A11 mRNA 3'-UTR的AREs结合,提高SLC7A11 mRNA的稳定性,从而增加SLC7A11的表达,减少铁死亡过程中ROS和铁的积累,最终促进肿瘤细胞的增殖和发展。
来源:https://www.sciencedirect.com/science/article/pii/S2213231722000842 via%3Dihub
关注梅斯学术微信公众号,一手科研干货、资讯,多重好礼等你领!

Cell Death Dis:lncRNA HOXA-AS2通过结合EZH2并抑制LATS2以促进AML发生发展
![]() 0
2020-12-07
点击查看
0
2020-12-07
点击查看

Sci Rep:肌肉浸润性膀胱癌中关键lncRNA的亚型特异性表达和生存预测
![]() 0
2020-12-16
点击查看
0
2020-12-16
点击查看
Nat Commun:lncRNA MaTAR25通过调控Tns1基因影响乳腺癌的发生发展
![]() 0
2020-12-25
点击查看
0
2020-12-25
点击查看

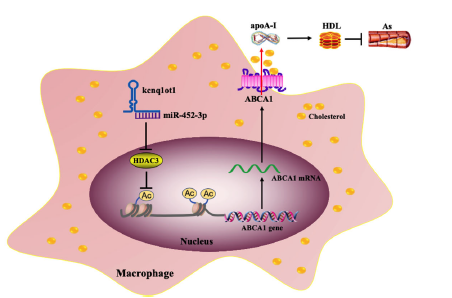
Cell Death Dis:LncRNA kcnq1ot1通过介导miR-452-3p/HDAC3/ABCA1通路促进脂质的积累并促进动脉粥样硬化
![]() 0
2020-12-26
点击查看
0
2020-12-26
点击查看
Cell Death Differ:lncRNA PFI调控SRSF1的表达及活性以预防肺纤维化的发生
![]() 0
2021-05-14
点击查看
0
2021-05-14
点击查看
Nat Commun:lncRNA Nron:抗骨质疏松的新型骨吸收抑制因子
![]() 0
2021-06-04
点击查看
0
2021-06-04
点击查看