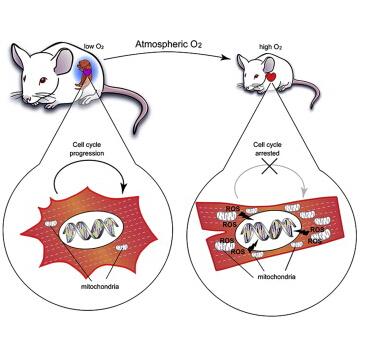
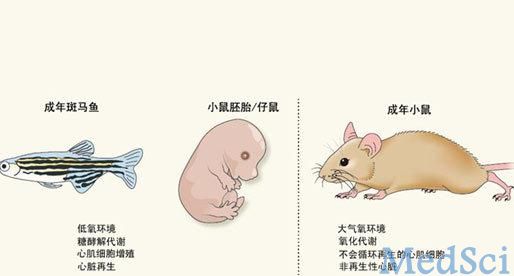
在胚胎发育时期以及新生儿时期,哺乳动物的心脏与成年斑马鱼的心脏之间存在着一些相似之处:它们都存在于低氧环境中,心脏肌细胞(即心肌细胞)都是利用非氧化性的糖酵解代谢(以葡萄糖为基础的代谢)来产生能量,并且都具有增殖能力;如此一来,它们的心脏在受到损伤之后,就能够再生出大部分心脏来修复损伤。而相比之下,成年哺乳动物的心脏存在于富氧环境中,是通过氧化代谢来产生能量的。Puente等人指出,小鼠在出生后,其心脏从低氧环境转移到了含氧量高的环境中,从而使心肌细胞的细胞周期发生阻滞,使心脏不再具备再生能力。
人们对新生动物发育过程的了解大多数来源于小鼠的研究,而小鼠的妊娠期仅为19-21天。与新生小鼠的器官相比,人类胚胎在经过了九个月的妊娠期后,出生时其器官发育得更加成熟。研究者们观察到,新生小鼠的心脏在受到损伤后能够重新生成部分心脏组织,这些发现使得研究者们围绕着人类先天性心脏缺陷的潜在治疗方法提出了多种猜想。然而,人们目前尚不清楚人类心肌细胞在胚胎晚期或新生儿发育期间是如何进行增殖和发育成熟的,也不清楚仔鼠心脏的发育规律在多大程度上符合人类心脏的发育规律。人类在出生时暴露于大气环境中较高浓度的氧气,心肌细胞及其再生潜力可能也会受到相同的影响,但是研究者们仍然有必要对妊娠期比小鼠妊娠期更长的大型动物或非人类灵长类动物进行研究,从而确定在人类生命的最初几周内,其心脏的发育或再生是否可能存在着同样的适应能力。
出生时所发生的氧化应激可以促使机体生成一些名为活性氧(reactive oxygen species, ROS)的化学活性分子,并且还可以诱导DNA损伤应答。Puente等人认为这些生理过程是促使仔鼠心肌细胞在高氧环境下发生细胞周期阻滞的刺激物;他们也指出,在利用 ROS清除剂(N-乙酰半胱氨酸)对小鼠进行处理后,可以抑制氧化应激,并且最终能够延长心脏的再生能力,使心脏在小鼠出生后21天内仍能够再生,而正常情况下心脏再生能力的窗口期仅为7天。但是即便如此,延长的心脏增殖窗口期仍然会关闭,这就表明氧化应激的抑制能够延缓心肌细胞发生细胞周期阻滞,但却不能阻碍细胞周期阻滞的出现。在一些小鼠模型中,研究者们可以使细胞周期阻滞的出现推迟1~2周,但是在大多数情况下,心肌细胞最终还是会停止分裂。研究者们目前仍然没有完全弄清楚心肌细胞增殖的重要阻碍机制,而这些机制也是研究者们极其感兴趣的研究领域。
尽管Puente等人已经表明ROS的清除能够延长仔鼠的心脏再生能力,但是他们并没有研究这种ROS清除方法是否能够在成年小鼠心脏受到损伤后促进心脏的再生能力。研究者们已经在人体中进行了试验,利用同一种ROS清除剂来进行抗氧化治疗,从而能够在人类心脏病发作后减少心肌的损伤,但是这种治疗方法的疗效甚微,而且尚未被广泛应用。由于成年动物的心肌与新生动物心肌在代谢和细胞周期调节方面存在差异,因此在氧化应激状态下,成年动物的心肌细胞似乎不可能会对ROS的清除产生增高的再生性应答反应。然而,这肯定是一块值得深入研究的领域。
非常有趣的是,研究者们纷纷推测道,陆生生物对大气环境中较高浓度的氧产生了进化上的演变,从而导致哺乳动物不能再重新生成新的心脏肌肉。斑马鱼栖息在一种相对低氧的环境中,其心脏和肢体的再生能力比哺乳动物的再生能力要强。两栖动物的心脏也能够进行再生,因此尽管可能无法研究大气氧含量或高氧环境对鱼类的影响,但是可以通过调节两栖动物生活环境中的氧含量水平,来验证这种进化假设。
由于陆生蜥蜴的尾巴能够进行再生(尽管新生的尾巴与原来的尾巴并不完全一样),因此最终的确证性研究可能是检测蜥蜴的心脏再生能力。哺乳动物在出生时暴露于大气环境中较高浓度的氧,可能促进了更强大的肌细胞的发育,而这些肌细胞是维持闭合性循环系统所必需的;而此消彼长的是,心肌细胞在心脏受损或成年期心脏疾病时则缺少再生能力。但是通过进一步了解新生哺乳动物身上所发生的环境氧含量改变(例如Puente等人所提供的氧含量改变),就能够揭示病变心脏的复原或修复方法。
原始出处:
Puente BN1, Kimura W2, Muralidhar SA2, Moon J3, Amatruda JF4, Phelps KL5, Grinsfelder D6, Rothermel BA7, Chen R2, Garcia JA2, Santos CX8, Thet S2, Mori E9, Kinter MT10, Rindler PM10, Zacchigna S11, Mukherjee S9, Chen DJ9, Mahmoud AI12, Giacca M11, Rabinovitch PS13, Aroumougame A9, Shah AM6, Szweda LI10, Sadek HA14.
The oxygen-rich postnatal environment induces cardiomyocyte cell-cycle arrest through DNA damage response.Cell. 2014 Apr 24;157(3):565-79. doi: 10.1016/j.cell.2014.03.032.