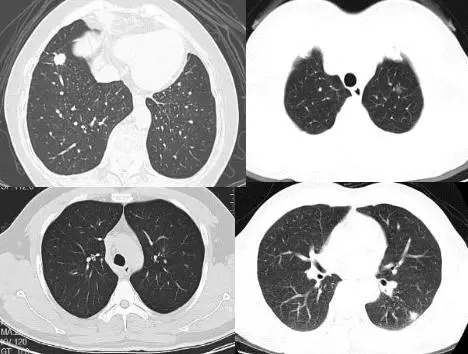
左下图为2016年河北石家庄市发表在Thorac Cancer的一篇文章,其中高峰区域表明石家庄市70岁年龄组的
肺癌发病率已经接近500/100000,也就是1/200,算是世界之最了。我国的男性和女性的
肺癌发病率在亚洲都是第一位的。右下图的五年存活率中,1999年报道中国肺癌的五年存活率只有8%,当时日本为21%,美国为20%,经过20年的时间,我们现在终于接近19.7%了,但还是低于美国和日本20年前的水平。
怎么解决这个问题?
我们要另辟蹊径,按照原来的方法和技术无法改变现状,所以我们要通过物联网医学执行肺结节诊治中国专家
共识和亚太肺结节评估指南,来推动我们的诊治。
2014年9月20日制定中国首个《肺结节诊治中国专家
共识》发表在《中华结核和呼吸杂志》,2018年更新共识。
1、肺结节定义和分类
肺结节定义
影像学示直径≤3 cm的局灶性、类圆形、密度增高的实性或亚实性肺部阴影。可为孤立或多发,不伴肺不张、肺门淋巴结肿大和胸腔积液。局部病灶直径>3 cm者则称为肺肿块。
肺结节可分为以下三类
1、数量分类
单个病灶定为孤立性,孤立性肺结节为边界清楚、密度增高、直径≤3 cm且周围被含气肺组织包绕的软组织影;2个以及以上的病灶定义为多发性,需要与转移性肺肿瘤鉴别
诊断。
2、密度分类
实性肺结节(solid nodule),间质
血管都看不见(左上图),亚实性肺结节(subsolid nodule)包括纯磨玻璃结节(pure ground-class nodule,pGGN)(左下图),还有混杂性结节(mixed ground-glass nodule,mGGN),也称部分实性结节(part solid nodule),表现为间质样改变,中间实性,周围是磨玻璃样。
3、病灶大小分类
在2018年版的专家共识中,我们做了一个创新,首个共识提出大小分类:微小结节(直径<5mm),小结节(直径5-10 mm),肺结节(直径 30 mm以下)。这样分类有助于分级
诊疗。
<5mm的微小结节对于病人来说,半年甚至一两年之内都没有很大的威胁,可以放心的在基层医院
管理;
5-10 mm的小结节可以在有诊治经验的中国肺癌防治联盟肺结节诊治分中心
管理;
≥10 mm的肺结节则应该尽早诊治,如果不能确诊,建议多学科会诊(MDT)。
筛查人群
鉴于我国吸烟及被动吸烟人群比例高、大气污染及发病年轻化现状,高危人群可定义为年龄≥40岁且有以下因素者:
吸烟≥400年支(或20包年),或曾经吸烟≥400年支(或20包年),戒烟时间<15年;
环境或高危职业暴露史(如石棉、铍、铀、氡等接触者);
病史:慢阻肺、弥漫性肺纤维化或既往有肺结核病史者;
既往史:罹患恶性肿瘤或有肺癌家族史者。
欧美国家的筛查人群和我国不同,第一个发在Chest杂志上的ACCP指南明确规定,抽烟30包年,年龄超过55岁,可以进行筛查。但是在《肺结节诊治中国专家共识》却大有不同,这是为什么?
由于我国40岁左右发生肺结节的人越来越多,我国肺结节患病率已经超过1亿,大概1.2亿左右,我国慢阻肺患者才接近1亿,所以肺结节对人体的危害很大。根据我国实际情况把肺结节筛查人群的年龄降到40岁,我国有很多统计学数字,比如现在我们中山医院每年体检十六、七万人,40岁以上人群达到一半,每年会做八、九万的胸部CT,能筛查出一万五、六千个例肺结节病人,其中有1000个左右的早期肺癌病人。
评估手段包括以下六方面
采集与
诊断和鉴别诊断相关的信息,如:年龄、职业、吸烟史;慢性肺部疾病史;个人和家族肿瘤史;治疗经过及转归。
2、影像学检查
胸部CT扫描可提供更多关于肺结节位置、大小、形态、密度、边缘及内部特征等信息,推荐肺结节患者行胸部CT检查(结节处行病灶薄层扫描),薄层(≤1 mm层厚)DICOM文件可用于AI进一步分析。
建议设定低剂量CT检查参数和扫描的范围为:
扫描参数:总辐射暴露剂量为1.0 mSv;kVp为120,mAs≤40;机架旋转速度0.5;探测器准直径≤1.5 mm;扫描层厚5 mm,图像重建层厚1 mm;扫描间距≤层厚(3D成像应用时需有50%重叠);
扫描范围:从肺尖到肋膈角(包括全部肺),扫描采样时间≤10 s,呼吸时相为深吸气末,CT扫描探测器≥16排,不需要注射对比剂。
3、肿瘤标志物
目前尚无特异性生物学标志物应用于肺癌的
临床诊断,但有条件者可酌情进行如下检查,如果在随访阶段发现下述肿瘤标志物进行性增高,需要警惕早期肺癌。
主要推荐以下5项,实际4项就足以:CEA、CYFRA21-1、SCC、Pro-GRP。
胃泌素释放肽前体(pro gastrin releasing peptide,Pro-GRP):可作为小细胞肺癌的诊断和鉴别诊断的首选标志物;
神经特异性烯醇化酶(neurone specific enolase,NSE):用于小细胞肺癌的诊断和治疗反应监测;
癌胚抗原(carcino-embryonic antigen, CEA):目前血清中CEA的检查主要用于判断肺腺癌复发、预后以及肺癌治疗过程中的疗效观察;
细胞角蛋白片段19(cytokeratin fragment,CYFRA21-1):对肺鳞癌的诊断有一定参考意义;
鳞状细胞癌抗原(squarmous cell carcinoma antigen,SCC):对肺鳞癌疗效监测和预后判断有一定价值。
4、功能显像
不建议对所有病人都做功能显像,我做PET-CT主要有这样二个目的。为了鉴别诊断是否为肿瘤,我现在基本使用AI鉴别。多发肺结节需要除外转移性肺癌的时候要做PET-CT,还有就是在手术前做PET-CT,当做术前检查。
5、非手术活检
经胸壁肺穿刺活检术(transthoracic needle biopsy,TTNB) ;
气管镜检查:TBLB、AFB、EBUS-TBLB、虚拟导航气管镜(virtual broncho-scopic navigation, VBN、电磁导航气管镜(electromagnetic navigation bronchoscopy,ENB。
最近几年会推广非手术活检新技术,包括激光共聚焦和气管镜机器人。
6、手术活检
胸腔镜检查:适用于非手术活检无法取得病理标本的肺结节,对术中明确为恶性的肺小结节还可行根治术;
纵隔镜检查:作为确诊肺癌和评估淋巴结分期的有效方法,是目前临床评价肺癌患者纵隔淋巴结状态的金标准,可弥补EBUS的不足。
3、肺结节的评估和处理流程
首先要进行肺结节临床恶性概率评估
这里有6个变量,其中年龄、吸烟史、癌症史,通过询问病史可得出答案。还有3个是放射科医生得出的数据,包括结节的直径、有无毛刺征、位置。
注:ACCP指南中「位于上叶的肺结节肿瘤概率大」并不完全适合我国和大部分亚太地区的国家和地区,因为上叶尖后段也是肺结核的好发部位。
那么,处理流程是怎样的?
8~30mm的实性肺结节处理原则可以参考这张图:
几个原则:第一,要到有经验的医院或医生就诊;第二,可以进行AI分析或者请有经验的专家会诊;第三,多学科会诊(MDT),最好能拿到病理学检查结果。
注:手术并发症风险高的人群中,我们推荐CT扫描监测(当临床恶性肿瘤的概率是低到中等)或非手术活检(当临床恶性肿瘤的概率是中到高度)。
≤8 mm的实性肺结节处理流程
≤8mm的实性结节是最难并且最重要的。中国有1亿多的肺结节,80%是8mm以下的,而且诊断很有意义,比如很多医生都会诊断3cm的肺结节,一般都转移了,术后几个月、几年复发的大有人在,变成「死刑缓期」,1~3年就执行了,所以意义不大。在没有转移的时候进行诊断,大部分在8mm左右或以下。所以我提出一个口号,在2018年版共识中明确提出:10mm诊断,让病人活10年以上,或者根治。
按照如图的流程,我们怎么做精准的诊断?先看病人室友有无肺癌的危险因素,比如抽烟、家族史等。有危险因素的人群,随访的时间就要短一点,还要根据结节的直径大小,结节越小随访的时间就可以越长一点。
再看亚实性肺结节,就是磨玻璃的混杂性的肺结节如何处理?
依然遵循刚才提到的「几个原则」,提醒一下如果有
感染性的可能时,可以使用
抗生素治疗一周左右。
现在多发性肺结节评估与处理原则越来越困难,为什么呢?倒退10年,我们将多发性肺结节大多数为转移性肺癌,但是现在不一样了,现在发现多原发的肺癌越来越多,有的人左上肺叶看到一个结节,是肿瘤,同时右上肺的结节也是肿瘤,左下肺、右下肺都有结节,一共4个原发癌,甚至更多的都有,所以越来越困难。怎么办呢?实际还是有规律可循的:
PET-CT扫描有助于鉴别转移性肺癌;
5~10 mm多发pGGN:3个月再随访,无变化者至少3年内每年1-2次CT随访。如病灶变化,应调整随访周期,如结节增多、增大、增浓, 应除外恶性结节;
新技术辅助诊断:AI有助于鉴别诊断,EBUS、ENB和激光共聚等,可在一次检查中对多个较小的周边病灶活检;
>10个弥漫性结节,很可能伴有症状,可由胸外恶性肿瘤转移或活动性
感染导致,原发性肺癌的可能性相对较小;
但单一主要结节伴有一或多个小结节,需要进行仔细鉴别诊断。
4、执行策略:物联网技术
为什么需要物联网技术?
一般来讲,阅片存在局限性,我原来阅片有一些个人体会,总结了八字真言:可以从外观评估(或称「以貌取人」)和探查内涵(或称「更重内涵」)两个角度判断肺结节的良恶性,外观看分叶征、毛刺征、胸膜凹陷征,有80%~90%诊断肺癌的准确性。但是5mm的结节很少有以上的表现,10mm也不一定有,那我们就要看内涵,包括密度、良性的特征、
血管的生成、气管的结构,但是为水平高低不一的手工业作坊式
诊疗模式,所以我们需要用物联网技术将其提升为国家标准的现代化流水作业工程。
简单来说,物联网包括三大基础流程:全面感知、可靠传输、智能处理,智能处理就是人工智能技术(AI),那么它究竟有没有用呢?
实性结节(边缘似呈分叶状)
这是一个9mm的实性结节,没有人工智能的时候,我阅片肯定不敢确定为肺癌,当时我通过人工智能分析后,肿瘤的概率起码为95%,手术后发现果然是原位癌。
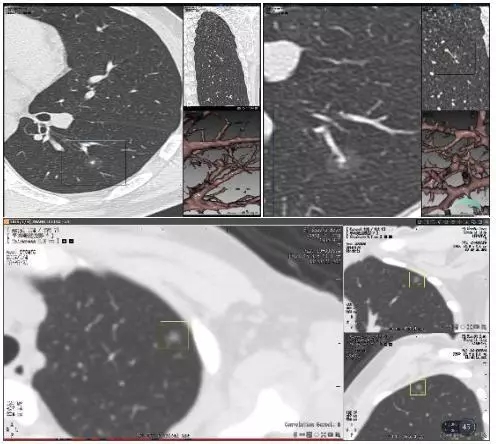
A 实性结节:右肺中叶外侧段见一枚大小约为9.3×8.0mm的不规则结节影,边缘似呈分叶状,边界清晰,周围见胸膜轻度牵拉征象;手术病理提示(右中肺)微浸润腺癌,非粘液型,浸润成分为腺泡型,支气管切缘未见癌累及, EGFR基因第19外显子存在缺失突变。(A:轴状位;B:冠状位 (人工智能检测结果);C:矢状位;D:VR重建)
纯GGO结节薄层CT(内见血管穿行)
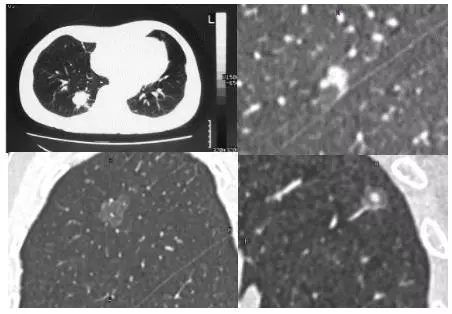
B 纯磨玻璃结节薄层CT影像:左肺上叶前段胸膜下见一无糖代谢增高的磨玻璃结节,大小约为18.0×20.2mm,内部密度欠均匀,内见小血管及小支气管穿过,边界欠清,邻近胸膜牵拉;手术病理提示:(左上肺)微浸润性腺癌,癌组织紧贴脏层胸膜。(A:轴状位;B:冠状位;C:矢状位;D:CPR重建)
混合性结节薄层CT(内见血管穿行)
这是一个典型的混合性结节,煎鸡蛋样改变,周围磨玻璃影,中央实性,9mm结节。
C 混合性结节薄层CT影像:左肺上叶尖后段见一大小约为9.0×8.6mm的混合性结节影,边缘欠光整,见浅分叶,内见血管穿行;手术病理提示:(左上肺楔形)原位腺癌,伴间质纤维增生。(A:轴状位;B:冠状位;C:矢状位;D:VR重建)
人工智能能帮助我们提高阅片技术,阅片水平提高后,不用人工智能,也可以确诊肺癌。
积累经验后,减少AI依赖性(病例1)
患者,男性,44岁,否认吸烟史,无
抗生素治疗。右肺下叶见混合性GGO结节,类圆形,最长径12 mm,体积0.778cm³,平均密度-731HU,边界欠清,边缘欠光滑,内见空泡,见血管长入,见支气管充气征。
积累经验后,可减少AI依赖性(病例2)
还可以预测病人病情的进展,这是2019-03-2会诊病例,患者老年女性。因为当时给这个病人看病的医生说不一定是癌症,2017年后就没有照过CT了。我比较2015与2017CT后,当即告诉患者家属95%概率是肿瘤,马上复查薄层CT即可证实,发现不但是癌症,而且还长大了,里面还有发亮的血管。要是2年前手术绝对是原位癌,现在如果治好了是微浸润性,治不好就是浸润性肺癌。
人工阅片也有限制,AI可弥补不足
随访比较肺结节的外部结构和内部特征,对鉴别具重要意义。
右肺下叶见实性结节,椭圆形,最长径16.6mm,体积0.654cm³,平均密度-151HU,边界清,边缘欠光滑,内见空泡,见血管长入,边缘毛刺、分叶、胸膜凹陷征,未见支气管充气征,未见中心性钙化。
较前体积增大,倍增时间为249天,密度较前增加,基线SUV值为2.4。
将来的人工智能不仅用于影像学,还可以用在液体活检、基因未突变之前有表观遗传学变化的印迹基因阶段。应用物联网技术建立肺结节诊治分中心在全国已经开了730家分中心。
肺结节究竟多重要?
小结
肺结节已经成为我们严重的健康问题,肺结节诊治中国专家共识和亚太指南具有刚性需求和重要临床意义。共识和指南较全面地阐述了肺结节定义、分类、评估方法、诊断要点、孤立性和非孤立性肺结节评估与处理原则,物联网医学辅助评估与管理为达到大医惠众愿景创立了同质化平台。以后需要进一步提升技术和推广,以达到「名医治未病,大医惠众生」效果。
链接:
来源:呼吸界
版权声明:
本网站所有注明“来源:梅斯医学”或“来源:MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有,非经授权,任何媒体、网站或个人不得转载,授权转载时须注明“来源:梅斯医学”。本网所有转载文章系出于传递更多信息之目的,且明确注明来源和作者,不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。同时转载内容不代表本站立场。
在此留言