目前,基于关键临床试验结果获得美国FDA批准的分子靶向药物,其安全性和有效性并不一定符合相关生化靶标。为了应对这些挑战,欧洲肿瘤医学学会(ESMO)转化研究和精准医学工作组制定了ESMO分子靶点临床可操作性量表(ESCAT),旨在支持临床医生根据现有证据确定癌症基因组突变的可靶向性及其作为临床靶标的应用价值。
此外,为了帮助医生和患者区分高效疗法和低效疗法,肿瘤专业协会制定了ESMO-临床效益等级量表(ESMO-MCBS),用于指导医生、患者和卫生技术评估机构选择高价值的治疗方法。最新版本的量表涵盖了随机临床试验和单臂试验,以及基于药物疗效、安全性和生活质量结果的临床获益综合分析。
NGS技术在一次检测中可鉴别数百个基因的突变状态。随着越来越多的NGS方法用于指导癌症治疗决策,一些前瞻性试验已经探索了多基因测序在临床实践中的相关性,但没有显示出与患者预后的显著相关性。此外,FDA批准的癌症靶向药物的基因靶点和替代措施的有效性和价值尚不确定。
哈佛大学医学院等多家单位的研究人员联合在JAMA Oncology发表了题为“Clinical Value of Molecular Targets and FDA-Approved Genome-Targeted Cancer Therapies”的文章,评估了2015年1月1日至2022年12月31日期间,FDA批准的癌症基因靶向治疗药物相关分子靶点的可操作性,并评估了支持癌症基因靶向药物批准的证据及其与临床益处的关联。结果表明,在近期批准的癌症分子靶向治疗中,24个适应症(29%)显示出实质性的临床益处。ESMO-MCBS和ESCAT等框架可以帮助医生、患者等确定具有最大临床潜力的治疗方法。

文章发表在JAMA Oncology
主要研究内容
研究纳入了2015年1月1日至2022年12月31日期间,FDA批准的50个分子靶向药,覆盖84个针对基因组的癌症适应症。
在84个基因组靶向治疗癌症的适应症中,73个(87%)获得优先审查,50个(60%)获得突破性疗法称号。此外,32个(38%)获得加速批准,52个(62%) 获得常规批准。在支持84个癌症基因组靶向适应症批准的关键临床试验中,有45个适应症(54%)是基于1期或2期临床试验数据,有45个适应症(54%)获得单臂临床试验支持,有67个适应症(80%)是基于开放标签临床试验,48个适应症(57%)基于关键试验的亚组分析获得批准。
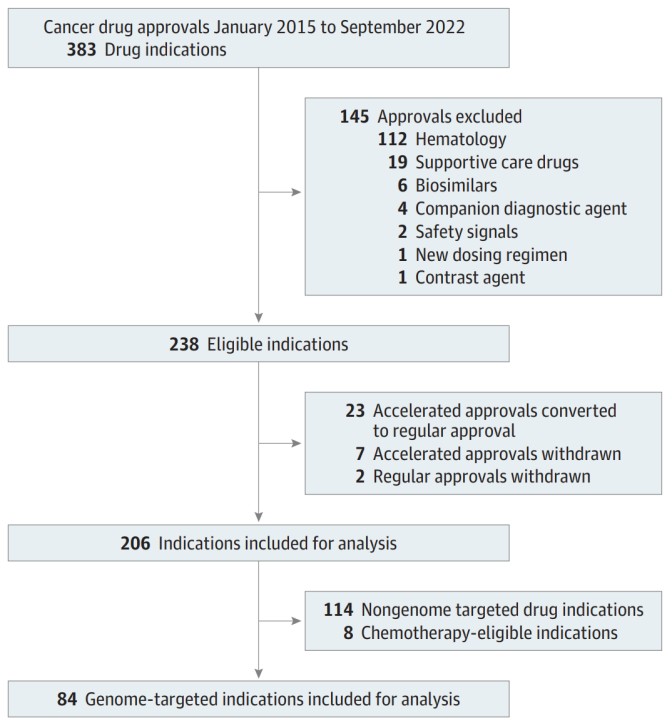
图1. 检索及筛选策略流程图
接下来,当ESCAT应用于84项支癌症基因组靶向适应症批准的临床试验时,38项试验(45%)被评为I-A级靶向性(前瞻性随机化研究);32项(38%)被评为I-B级靶向性(前瞻性非随机研究);13项(16%)被评为I-C类靶向性(篮子试验);1例(1%)为II-A级靶向性(回顾性研究)。
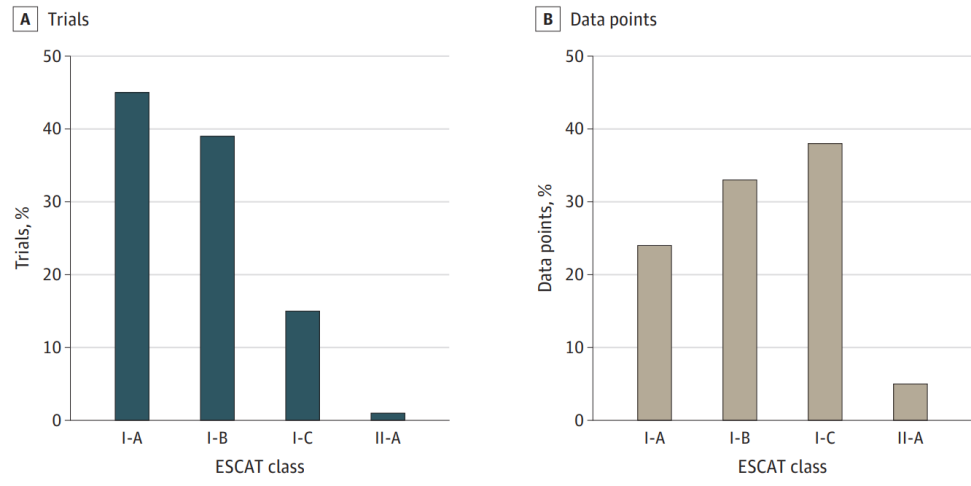
图2. 基于ESCAT对分子靶点进行分类
根据每个适应症,84个主要终点中的46个(55%)为总体缓解率,中位数总体缓解率57%,中位缓解持续时间为11.1个月。
ESMO-MCBS将符合ESCAT类别I-A和I-B级并具有实质性临床益处的分子靶点评定为基于基因组的高获益癌症治疗。在84项支持癌症基因组靶向适应症批准的试验中,24项(29%)达到了ESMO-MCBS的标准,与基于基因组的高效益癌症治疗相关,获得了实质性的临床益处。在38种I-A类基因组靶向药物中,23种(60%)显示出实质性的临床益处;在32种I-B组靶向药物中,只有1种药物是基于符合ESMO-MCBS阈值的试验而获得实质性临床益处的;而在I-C类或II-A类基因组靶向药物中,没有一种药物得到符合ESMO-MCBS阈值的试验支持,即无法获得实质性的临床获益。总体而言,来自ESMO-MCBS的I-A和I-B分类水平的分子靶点与实质性临床获益相关,涵盖了24项试验(29%)。此外,在扩大的临床试验队列中,分析发现实质性临床获益相关的ESMO-MCBS高价值分子靶点的比例为19%。
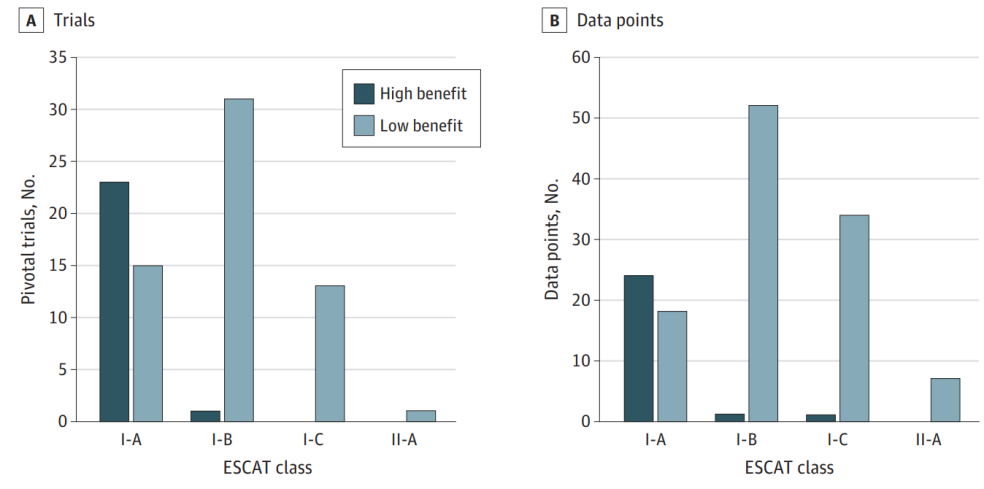
图3. 基于ESCAT区分高效益与低效益分子靶点的分布
结 语
在2015年1月1日至2022年12月31日期间,该队列研究涉及84个适应症,涵盖50个分子靶点,其中约一半是基于单臂试验的数据获批,以缓解率为主要终点。当结合ESMO-MCBS和ESCAT评分对分子靶点进行评估时,高效益分子靶点占支持这些药物的关键临床试验的不到三分之一。
该队列研究表明,对于新的癌症药物,类似ESMO开发的临床获益框架有助于确定提供高临床获益的治疗方法和分子靶点。虽然NGS测序已经帮助越来越多癌症患者获得个性化治疗,但支持药物批准的可靠试验仍应优先于回顾性、探索性分析,其次是必要的批准后研究和监测。总之,该研究数据加强了所有利益相关者持续进行深入研究的必要性,以产生充分的数据,为患者提供高价值的癌症护理。
论文原文:
Tibau A, Hwang TJ, Molto C, Avorn J, Kesselheim AS. Clinical Value of Molecular Targets and FDA-Approved Genome-Targeted Cancer Therapies. JAMA Oncol. 2024. doi:10.1001/jamaoncol.2024.0194.