我国自主研发的原创国家1.1类新药艾维替尼(Avitinib),也在ESMO上公布了首次人体试验结果,初步的结果显示艾维替尼具有良好的安全性,疾病控制率高达90%。
在WCLC上吴一龙教授报告了艾维替尼剂量爬坡和剂量扩增Ⅰ/Ⅱ研究的最新结果:艾维替尼并没有出现严重的高血糖和QT间期延长,最常见的毒性为1/2级的腹泻、皮疹和肝酶升高。300mg bid作为Ⅱ其研究推荐剂量。在300mg时艾维替尼的缓解率为52%,与AZD9291相当。
马来酸艾维替尼是由艾森生物自主研发的国内首个第三代EGFR抗肿瘤靶向抑制剂,拥有全球化合物专利,用于治疗具有EGFR突变或耐药突变的非小细胞
肺癌。它是“十二五”国家重大新药创制重大科技专项支持的原创新药,于2014年9月获国家C
FDA和美国FDA
临床批件。2016年8月25日,马来酸艾维替获国家
CFDA Ⅱ/Ⅲ期
临床批件(批件号:2016L08001、 2016L08002 、2016L08003)。同时,艾维替尼已获得CDE的书面支持,确定了有条件批准的注册临床方案。
根据2018年5月的中国优先审评与条件批准概况一文显示(可在文下留邮箱获取资料),艾森生物在2017年8月和2018年3月两次就基于二期单臂试验批准上市与CNDA/CDE展开Pre-NDA
会议。
经过数年的临床前期研究,2014年9月,艾维替尼获得临床批件,也是中国国内首家获批临床的T790M突变药物。
可喜的是,当下艾维替尼已经在近200例
肺癌患者中探索了治疗的安全性和有效性,取得了令人鼓舞的临床结果。据悉,目前艾维替尼正在开展或即将启动多项关键临床研究,全国近60家三甲医院参与,计划入组现有EGFR靶向抑制剂治疗失败,且具有T790M耐药突变的晚期非小细胞
肺癌患者。
艾维替尼I期临床的主要研究者之一正是吴一龙教授,其临床研究的“主战场”是广东省人民医院。
根据该院最新研究数据显示,艾维替尼最佳有效剂量是300mg,对具有靶点的肺癌病灶缩小有效率超过50%以上,既可减轻第一、第二代EGFR抑制剂治疗而导致的严重皮疹、腹泻等毒副作用,又能克服现有EGFR靶向药物治疗后产生的耐药问题。
“如果这种耐药基因突变的患者在药品I期临床取得成功,意味着未来的确证性临床研究的成功几率很大。”在吴一龙看来,艾维替尼这“初生牛犊”临床研究中,还更具创新型性质。
他分析说,早期临床试验中,I期看安全性,Ⅱ期看疗效,当下临床研究直接进行结构型创新,艾维替尼I期临床中直接结合了Ⅱ期试验,加快药物研究推进,在接下来的关键临床研究中,将进行验证前期药物研究的有效性。目前,艾维替尼正在全国各地对合适的病人,提供免费治疗和检查的机会,以解决药品上市前的临床需求。“如此一来,艾维替尼2到3年的临床研究‘出炉’时间,将大大超过药品5至7年的临床研究时间。”
小知识:
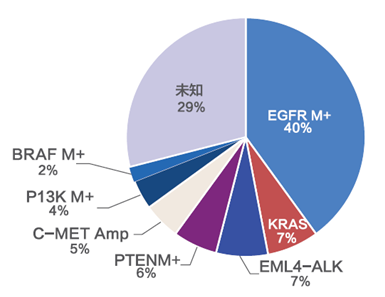
EGFR在中国肺腺癌人群中的突变率
不同靶向药物:
第一代的EGFR-TKI靶向药:易瑞沙、特罗凯、凯美纳
第二代EGFR-TKI靶向药:阿法替尼,达克替尼。
第三代EGFR-TKI靶向药:AZD9291(奥希替尼)、艾维替尼(AC0010)
第四代EGFR-TKI靶向药:EAI045,可用于一代药物耐药且有T790M突变的病人,或者用于AZD9291耐药且有C797S突变的病人。不过尚未上市。
