
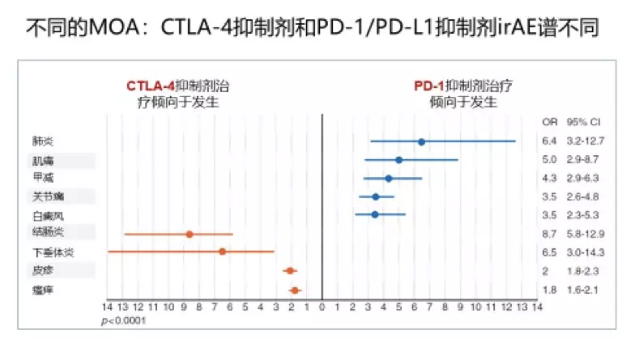
2018年WCLC:Durvalumab有助于维持无法切除的III期非小细胞肺癌的PFS
![]() 0
2018-09-27
点击查看
0
2018-09-27
点击查看
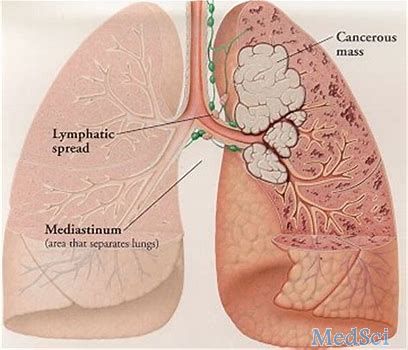
2018年WCLC:Atezolizumab治疗IV期非鳞状非小细胞肺癌的有效性和安全性
![]() 0
2018-09-28
点击查看
0
2018-09-28
点击查看
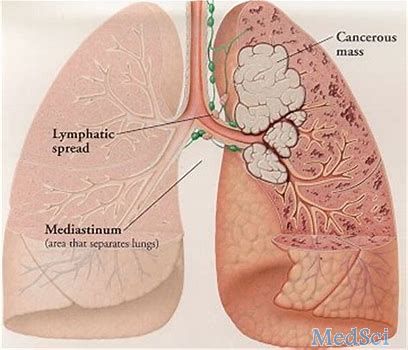
2018 WCLC:张力教授:Keynote-032结果公布,Keynote-033值得期待
![]() 0
2018-09-30
点击查看
0
2018-09-30
点击查看

WCLC 2018:程颖教授谈小细胞肺癌研究进展
![]() 0
2018-09-30
点击查看
0
2018-09-30
点击查看

WCLC 2019:评估脂质体伊立替康(ONIVYDE)作为小细胞肺癌的二线疗法
![]() 0
2019-09-09
点击查看
0
2019-09-09
点击查看

WCLC 2019:mNSCLC中的敏感性或耐药性突变
![]() 0
2019-09-09
点击查看
0
2019-09-09
点击查看
