导读
基于CheckeMate-214和CheckMate-025 III期研究,纳武利尤单抗联合伊匹木单抗被批准为中风险或低风险转移性肾细胞癌的一线方案。纳武利尤单抗单药治疗作为所有风险组的二线治疗。
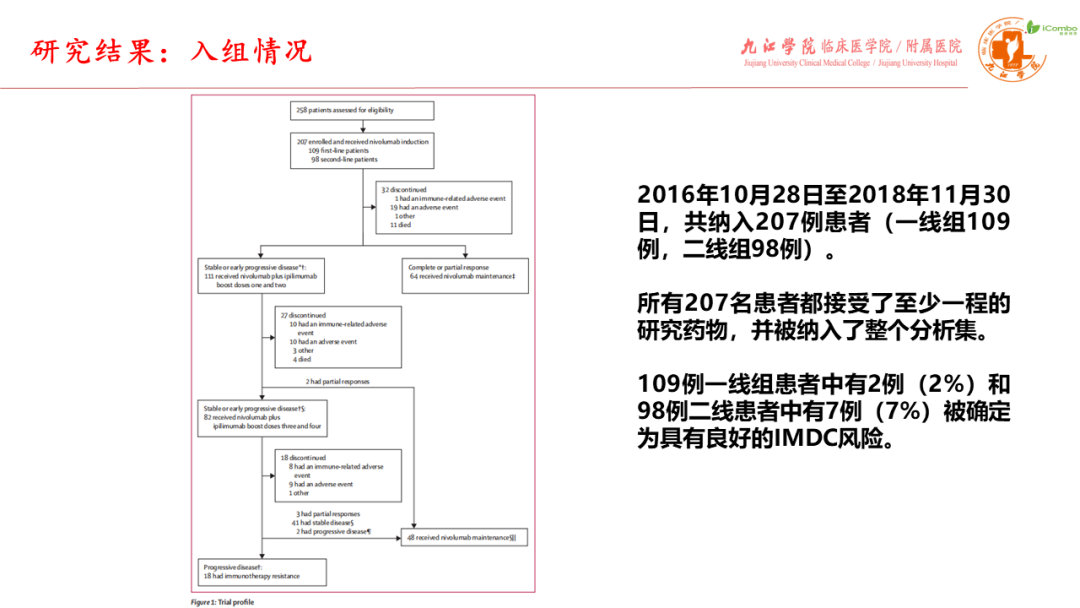
TITAN-RCC研究评估免疫免疫强化治疗作为中风险和低风险转移性透明细胞肾细胞癌患者的一线和二线治疗的有效性和安全性。研究设计为纳武利尤单抗诱导治疗,若在第8周时肿瘤进展或到16周肿瘤无应答者,纳武利尤单抗联合伊匹单抗2-4程,以后纳武利尤单抗维持治疗到进展为止。
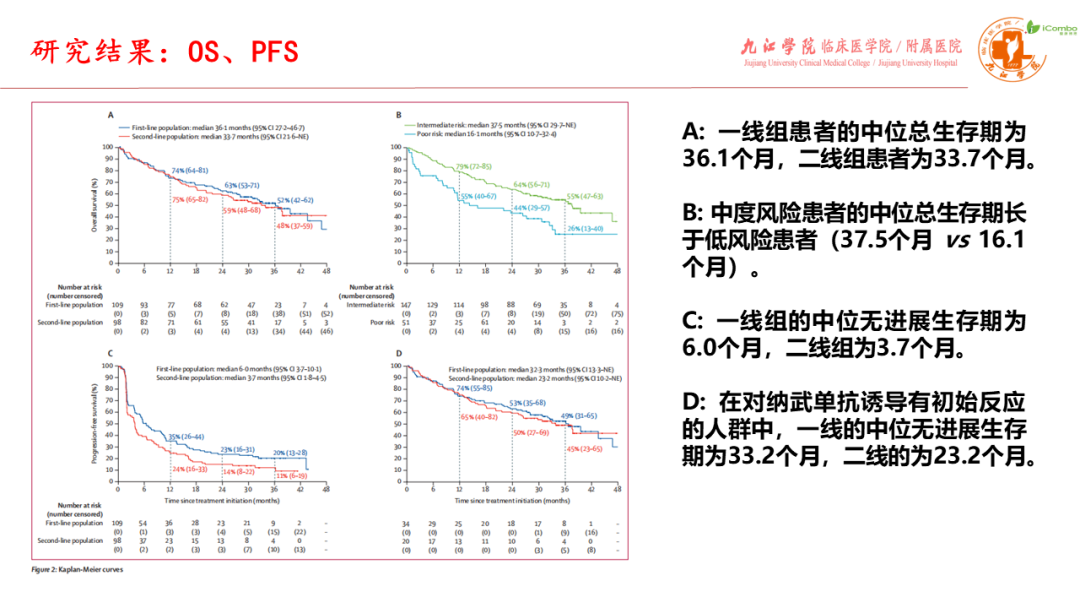
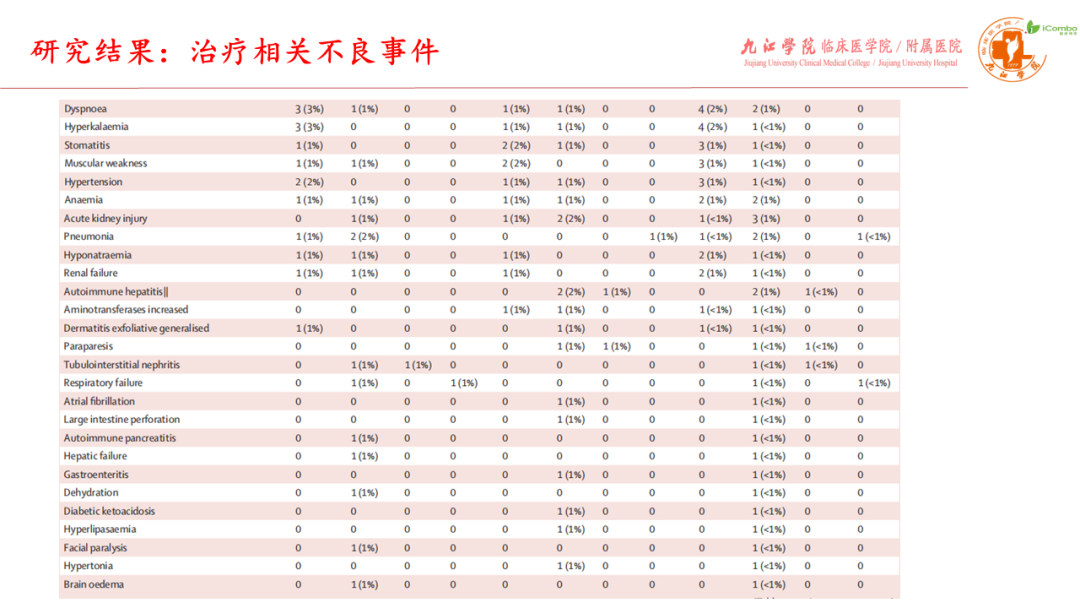
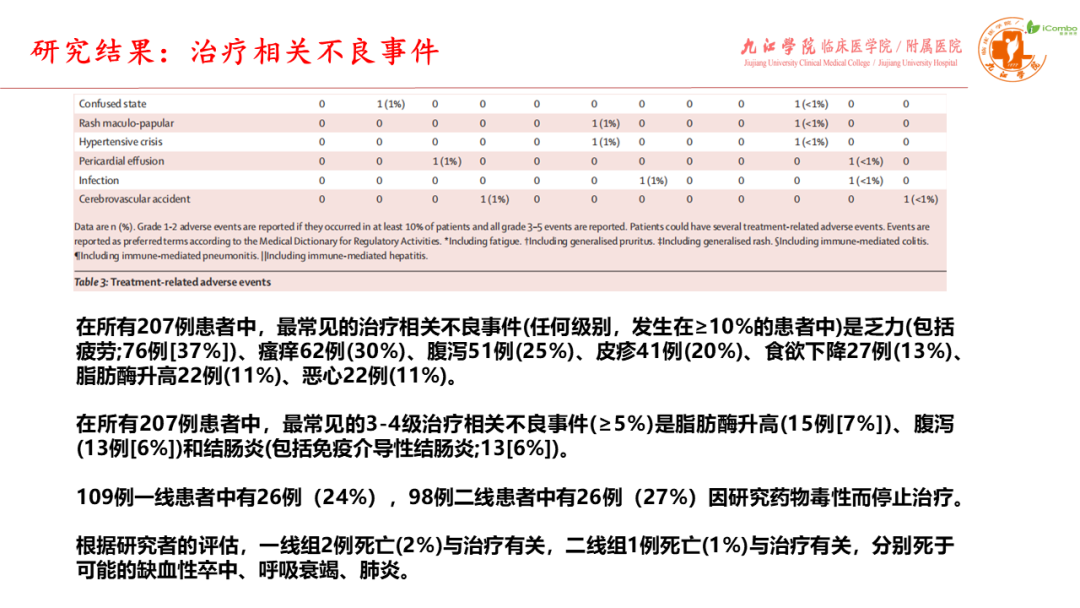
研究入组207例中危或高危晚期肾透明细胞癌患者,其中一线治疗者109例,既往TKI抑制剂或伊维莫司治疗失败的二线患者98例。 纳武利尤单抗诱导后第8或16周时确认的ORR:一线组28%(2% CR),二线组18% (无CR)。纳武利尤单抗±纳武利尤单抗联合伊匹木单抗治疗后,一线组与二线组的确认ORR分别为36%(7% CR)与32%(6% CR)。一线组的中位PFS为6.0个月,二线组为3.7个月。一线组的中位OS为36.1个月,二线组为33.7个月。
结论:与纳武利尤单抗联合伊匹木单抗一线治疗的CheckMate-214方案相比,TITAN-RCC研究客观缓解率和完全缓解率略低,但中位无进展生存期几乎减半,中位总生存期更短。
与二线纳武利尤单药(CheckMate-025)相比,TITAN-RCC方案的疗效有所改善,客观缓解率为32% vs 23%,完全缓解率为6% vs 1%,中位总生存期为33.7个月vs 25.8个月。最常见的3-4级治疗相关不良事件(≥5%)是脂肪酶升高、结肠炎和腹泻。因此,与已批准的纳武利尤单抗联合伊匹单抗相比,总体疗效较差。对于二线治疗,纳武利尤单抗联合伊匹单抗可能是已批准的纳武利尤单抗单药治疗进展的挽救策略( Lancet Oncol. 2023 Nov;24(11):1252-1265. doi: 10.1016/S1470-2045(23)00449-7)。












读书报告 | 荟萃分析纳武利尤联合伊匹木单抗治疗非黑色素瘤的晚期实体瘤
![]() 0
2024-02-29
点击查看
0
2024-02-29
点击查看

Lancet Oncol:在晚期肾细胞癌患者中,纳武利尤单抗单药或联合纳武利尤单抗和伊匹木单抗作为免疫治疗增敏的效果评估(TITAN-RCC 研究)
![]() 0
2024-02-27
点击查看
0
2024-02-27
点击查看
Ann. Oncol | 纳武利尤单抗治疗接受索拉非尼初治或经治的晚期肝细胞癌患者:CheckMate 040 的5年随访数据
![]() 0
2024-03-01
点击查看
0
2024-03-01
点击查看

读书报告 | 吉西他滨联合顺铂和纳武利尤单抗作为肌层浸润性膀胱癌器官保留治疗的2期临床试验
![]() 0
2024-03-12
点击查看
0
2024-03-12
点击查看

Clin Cancer Res:E7389-LF联合纳武利尤单抗治疗晚期胃癌的II期临床研究结果
![]() 0
2024-03-17
点击查看
0
2024-03-17
点击查看
ELCC 2024 :围手术期纳武利尤单抗与新辅助化疗+后续辅助纳武利尤单抗治疗可切除NSCLC患者的健康相关生活质量结果(CheckMate 77T研究)
![]() 0
2024-03-22
点击查看
0
2024-03-22
点击查看
