帕金森病(Parkinson's disease,PD)是一种常见的神经系统变性疾病,老年人多见,平均发病年龄为60岁左右。目前我国大部分帕金森病患者为散发病例,只有少数患者有家族史。帕金森病最主要的病理改变是中脑黑质多巴胺能神经元的变性死亡,由此而引起纹状体DA含量显著性减少而致病。
家族性和散发性帕金森病(PD)在遗传基础方面已经取得了很大的研究进展,但是这种风险的生物学基础和细胞背景仍然不清楚。从现有的研究中,我们了解到,大约1-2%的PD与经典的孟德尔遗传模式有关,而大多数疾病是由一系列复杂的因素驱动的,其中多基因风险似乎发挥了关键作用。许多含有致病突变的基因也在全基因组关联研究(GW-AS)确定的危险位点内,这一事实支持了一种观点,即两种形式都涉及共同的途径。因此,在单基因和非单基因PD中,这些多形基因可能相互作用调节下游共同靶点。
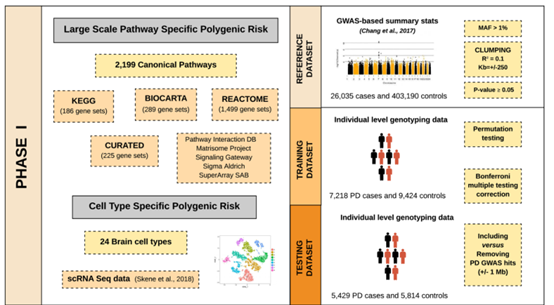
在本研究中,作者团队利用国际帕金森病遗传学联合会(IPDGC)和加速药物合作伙伴帕金森病倡议(AMP-PD)提供的目前最大的遗传和基因表达数据,采用高通量和无假设的方法来确定PD的生物学过程。通过应用大规模的基因集特异性多基因风险评分(PRS)分析来评估共同变异对帕金森病风险的作用,重点放在有代表性的治疗路径的公开注释基因集上。
通过在一组独立的全基因组测序数据中评估罕见变异对帕金森病风险的影响,作者发现了在一系列过程中罕见的破坏性等位基因负担的证据,其中包括神经元传递相关的途径和免疫反应。本研究还通过利用单细胞基因表达数据探索了与表达细胞特异性相关的富集模式,证明了多巴胺能神经元、5-羟色胺能神经元、下丘脑GABA能神经元和神经祖细胞具有显著的危险性。此外,作者团队利用PD患者血液中的转录组数据构建了一个新的网络表达社区图,揭示了炎症信号通路、细胞死亡机制相关过程和线粒体稳态失调的丰富功能。
Bandres-Ciga, S., Saez-Atienzar, S., Kim, J.J. et al. Large-scale pathway specific polygenic risk and transcriptomic community network analysis identifies novel functional pathways in Parkinson disease. Acta Neuropathol 140, 341–358 (2020). https://doi.org/10.1007/s00401-020-02181-3
Nat Neurosci: 帕金森病神经元的表观基因组学分析tet2丢失具有神经保护作用
![]() 0
2020-08-19
点击查看
0
2020-08-19
点击查看

Cell Death Dis:莨菪亭改善多巴胺能神经元的存活情况
![]() 0
2020-09-15
点击查看
0
2020-09-15
点击查看

Cell Stem Cell :重大进展!陈跃军团队发现移植干细胞来源的神经细胞可以改善帕金森病模型的行为学障碍
![]() 0
2020-09-23
点击查看
0
2020-09-23
点击查看
JAMA Neurol :傻傻分不清楚……看起来是帕金森病,其实是罕见神经退行性疾病?
![]() 0
2020-11-12
点击查看
0
2020-11-12
点击查看

Brain:黄志力/王坚团队成功构建帕金森病快动眼睡眠期行为障碍动物模型
![]() 0
2020-11-14
点击查看
0
2020-11-14
点击查看
Nat Genet:阿尔茨海默症和帕金森病的单核苷酸多态性研究, 揭示两种疾病的遗传风险位点的变异
![]() 0
2020-11-25
点击查看
0
2020-11-25
点击查看
