复发或难治性血液系统肿瘤患者的治疗选择有限,预后较差,5年总生存率不到20%。嵌合抗原受体(CAR)-T细胞疗法是治疗血液系统肿瘤的一个令人振奋的突破。既往研究已证实:在CD7阳性癌症中,CAR-T细胞疗法具有临床有效性和安全性。此外,多项临床研究将同种异体造血干细胞移植(HSCT)用于CAR-T细胞治疗后的巩固治疗,以维持长期肿瘤消除并降低复发风险。然而,HSCT前的骨髓消融和移植物抗宿主病(GVHD)预防药物具有毒性作用,可能会消除CAR-T细胞并影响抗肿瘤作用。
目前尚不清楚CAR-T细胞疗法与同种异体HSCT的结合,是否能保持CAR-T细胞功能并改善肿瘤的缓解情况。近期,浙江大学医学院附属第一医院黄河院长团队在NEJM发表了一项研究,其结果显示,在没有进行药物骨髓消融或GVHD预防情况下,序贯CD7 CAR-T细胞治疗和半相合HSCT治疗总体是安全有效的。患者1年总生存率和无病生存率分别估计为68%和54%。尽管存在不良反应但可逆。

截图来源:NEJM
该研究于2021年11月~2023年9月进行,纳入10例复发或难治性CD7阳性肿瘤患者,并将其安排接受“一体化”策略治疗,包括序贯CD7 CAR-T细胞治疗和半相合同种异体HSCT治疗。在CAR-T细胞治疗完全缓解但血液学恢复不完全情况下,患者接受半相合同种异体HSCT治疗,同时不使用药物骨髓消融或GVHD预防药物治疗。10例患者中,9例接受供体来源的CD7 CAR-T细胞治疗,另外1例提供通用CD7 CAR-T细胞治疗。
所有纳入的10例患者中,7例为急性髓系白血病(AML),2例为T细胞急性淋巴细胞白血病(ALL),1例为T细胞淋巴母细胞淋巴瘤(IVA级)。入组时患者中位年龄为56.5岁。从诊断到CAR-T细胞输注的中位时间为13.1个月。所有患者均有骨髓受累。2例患者有髓外病变。
经治疗后,患者1年总生存率估计为68%
在CAR-T细胞治疗后,所有10例患者均完全缓解,不过血液学恢复不完全,其中9例为微小残留病灶(MRD)阴性不完全血液学恢复和1例MRD阳性不完全血液学恢复。9例患者在接受同种异体HSCT后的第28天接受了移植后疗效评估,结果显示这些患者MRD阴性完全缓解。此外,临床诊断显示,2例患者分别在HSCT后3个月和1个月时髓外病变完全缓解。
CAR-T细胞治疗后的中位随访时间为15.1个月(范围为3.1个月~24.0个月)。2例AML患者分别在CAR-T细胞治疗后5.6个月和4.3个月发生骨髓CD7阴性白血病复发。1例患者在接受CAR-T细胞治疗后4.8个月因疾病进展而死亡。至数据截止日期(2023年11月8日),6例患者仍处于MRD阴性完全缓解状态。1年总生存率和无病生存率分别估计为68%(95% CI,43%~100%)和54%(95% CI,29%~100%)。
与此同时,患者在接受同种异体HSCT后,全血细胞减少得以缓解。在HSCT后1个月,9例患者中有7例(78%)具有完全供体嵌合,其中嵌合状态的好坏是判断移植效果好坏的一个重要指标。有1例患者在前3个月内维持混合供体嵌合状态(量化为88.35%),并在HSCT后6个月出现完全供体嵌合。
对于具有完全供体嵌合的患者,研究者观察到其在HSCT后1个月内造血功能成功恢复,中性粒细胞移植的中位时间为11.5天(范围,8~17天),血小板移植的中位时间为12天(范围,8~29天)。有1例患者在HSCT后1个月自体造血功能恢复,这可能是因为CAR-T细胞输注延迟和扩增受损。研究者还观察到免疫细胞的恢复。
CAR-T细胞在体内强劲扩增且具有持久性
研究者在所有患者中均检测到CAR-T细胞在体内强劲扩增。通过定量实时聚合酶链式反应(PCR)测定,达到CAR-T细胞最大扩增的中位时间为16天,最大扩增中位水平为DNA 2.9×105 copies/μg(范围,0.1~6.9)。通过流式细胞术评估的CAR-T细胞最大扩增中位时间为11.5天,最大扩增中位水平为316.5 cells/μL(范围,155.4~6501.9)。
在数据截止日期仍处于MRD阴性完全缓解的6例患者中,5例供体移植患者在最后一次评估时可检测到CAR-T细胞。自体造血功能恢复的患者在输注CAR-T细胞3个月后未检测到CAR-T细胞。在2例CD7阴性白血病复发患者中,疾病复发时流式细胞术检测不到CAR-T细胞,但定量实时PCR仍可检测到。
安全性分析
9例患者(5例为1级,4例为2级)发生了细胞因子释放综合征,中位发病时间为1天,中位持续时间为9.5天。不过这些患者的症状均得到了有效控制。没有免疫效应细胞相关神经毒性综合征病例发生。所有患者均出现4级全血细胞减少。
4例患者发生GVHD。1例患者在CAR-T细胞输注后第7天发生2级皮肤GVHD,经糖皮质激素和止痒药治疗后于第11天完全缓解。3例患者在半相合同种异体HSCT后发生短期2级急性GVHD。未发生慢性GVHD。
5例患者患有不同程度的细菌或真菌感染。1例患者在3.3个月时出现多药耐药血流感染,随后发生颅内感染,在3.7个月时死于脓毒症休克。另1例患者在同种异体HSCT后13天死于脓毒症休克和脑炎。其他患者的感染均通过抗生素被成功治疗。
小结
总的来说,这项研究结果表明,在可能会有严重但可逆的不良反应的情况下,序贯CD7 CAR-T细胞治疗和半相合HSCT治疗总体是安全有效的。
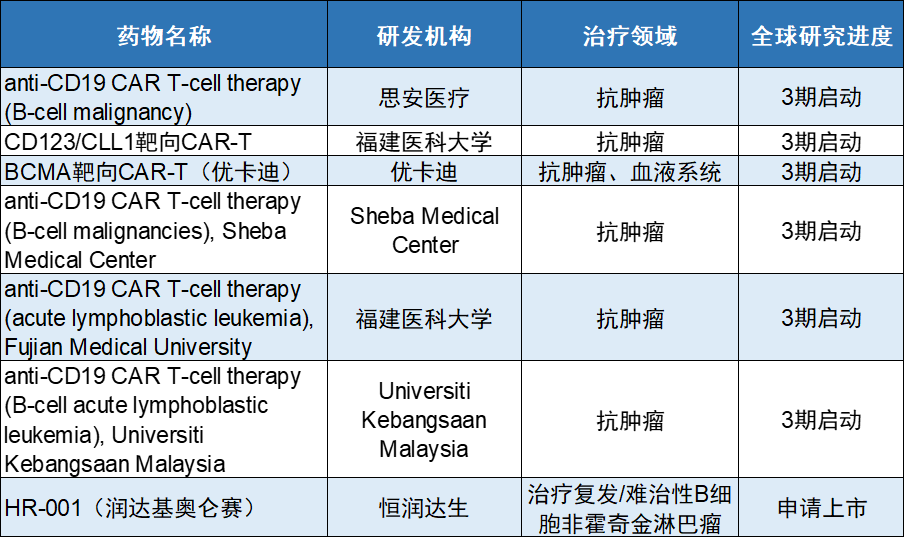
▲2023年以来全球最高状态进入3期且当前活跃/申请上市疗法(信息来源:公开资料,制图:药明康德内容团队)
参考资料
[1] Hu Y, et al., (2024). Sequential CD7 CAR T-Cell Therapy and Allogeneic HSCT without GVHD Prophylaxis. N Engl J Med, doi: 10.1056/NEJMoa2313812.
CAR-T治疗高端B细胞患者有批次
![]() 0
2024-03-28
点击查看
0
2024-03-28
点击查看
【Blood Adv】通过免疫表型监测CAR-T扩增,揭示不同淋巴瘤的扩增与毒性
![]() 0
2024-03-27
点击查看
0
2024-03-27
点击查看
2年无进展生存率超70%!《柳叶刀》子刊:CD30 CAR-T,淋巴瘤治疗新希望
![]() 0
2024-04-15
点击查看
0
2024-04-15
点击查看

AJH:CAR-T治疗复发性PCNSL最大样本研究,证实可诱导持久缓解
![]() 0
2024-04-11
点击查看
0
2024-04-11
点击查看
【Cancer】托珠单抗对CD19 CAR-T治疗B-ALL的影响:中国多中心回顾性研究
![]() 0
2024-04-11
点击查看
0
2024-04-11
点击查看

Haematologica:760例不同亚型LBCL接受CAR-T治疗的结局
![]() 0
2024-04-16
点击查看
0
2024-04-16
点击查看
