引言
近年来,微生物组(microbiome)对人类健康的影响越来越受到关注。继母体微生物组对后代健康影响的研究之后,父体微生物组如何影响后代的健康与适应性逐渐成为研究的新焦点。5月1日发表于Nature的研究“Paternal Microbiome Perturbations Impact Offspring Fitness”探讨了父体微生物组变化对后代健康的潜在影响及其机制。
该研究探讨以下几个科学问题:父体微生物组的改变如何影响后代的健康与疾病易感性(disease susceptibility)?哪些机制能够解释父体微生物组特征到后代的传递?在受孕前对父体微生物组进行干预是否能够改善后代的健康结果?
研究发现,父体微生物组的特定改变可以深刻影响后代的代谢健康和免疫健康。这些影响是通过表观遗传修饰(epigenetic modifications)和生殖系RNA的改变来介导的,这些改变随后会影响后代的基因表达。
该研究强调了受孕时父体健康的重要性,表明父亲的微生物组健康可以显著影响下一代的疾病风险和整体适应性。这为生殖健康的预防策略开辟了新的途径,不仅关注母亲,也应关注父亲。此外,这些见解为全面理解非遗传因素(如微生物组健康)如何以前所未有的方式影响遗传和疾病结果提供了可能,这可能会在管理和预防发育起源疾病方面带来突破。

Highlights
跨代影响的新视角:研究强调了父体健康状态,尤其是微生物组的健康状态,如何通过非遗传方式影响到下一代,这一发现为遗传学和微生物学领域带来了新的理解视角。研究发现微生物群扰动导致小鼠精子中小RNA(miR-141和miR-200a)表达的变化,这些RNA与上皮-间充质转化(epithelial–mesenchymal transition, EMT)及胎盘发育相关。此外,研究还观察到tRNA片段(如tRF-Gly-GCC)的表达上调,这可能与世代间影响相关
表观遗传机制的探索(Epigenetic Mechanisms):研究发现,父体微生物组的变化能通过表观遗传修饰影响后代的基因表达,这些发现有助于深入理解表观遗传如何在没有直接改变DNA序列的情况下传递遗传信息。
生殖健康的全面影响:研究不仅关注母体对后代的影响,还特别强调了父体因素的重要性,这对于生殖健康的研究和公共健康政策具有重要意义。
代谢和免疫健康的联系:研究揭示了父体微生物组如何通过影响代谢途径和免疫反应来调节后代的健康状况,为开发预防性健康措施提供了潜在的靶点。
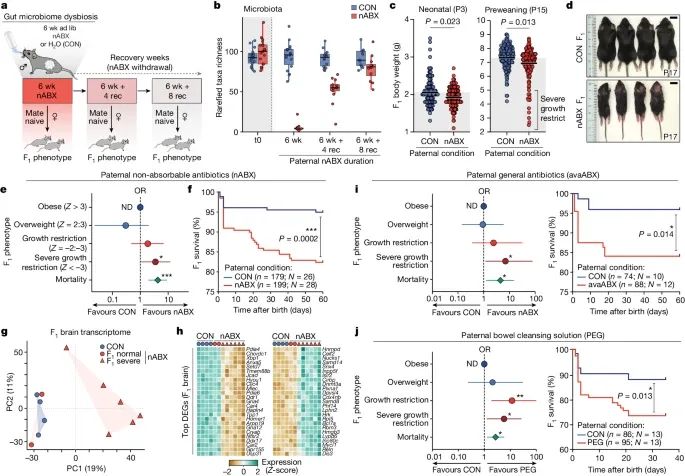
父系肠道菌群失调有可能触发主要的F1表型(Credit: Nature)
Strategies
小鼠模型和样本收集
实验采用了调整微生物组的小鼠模型,通过给予或不给予抗生素(antibiotics)来调整父鼠的肠道微生物组。
收集父鼠的精液样本和后代的组织样本,包括肝脏和睾丸。
微生物组DNA提取与测序
使用改良的DNA提取方法从精液中提取微生物DNA,并通过高通量测序(high-throughput sequencing)分析微生物组的组成。
转录组学分析(Transcriptomics)
对后代的肝脏和其他关键组织进行单细胞RNA测序(single-cell RNA-seq),使用STAR和DESeq2等软件处理数据,进行差异表达分析。
使用特定的TaqMan探针进行miRNA和tRNA的量化,利用实时定量PCR(qPCR)技术。
代谢组学分析(Metabolomics)
通过液相色谱-质谱联用技术(LC-MS)分析父鼠和后代组织中的代谢物,评估微生物组变化对代谢途径的影响。
使用Agilent的质谱仪进行精确的代谢物定量,采用基于数据的代谢物富集分析。
统计分析和数据处理
采用R软件进行统计分析,包括t检验和多变量分析,使用FDR校正处理多重假设测试问题。
使用火山图(Volcano plots)可视化差异表达基因和代谢物的显著性。
表观遗传标记分析(Epigenetic Marking)
通过比较治疗组和对照组的DNA甲基化水平(DNA methylation),探索微生物组如何通过表观遗传途径影响后代。
Behind the Scenes
肠道菌群与人体健康
肠道菌群,也被称为肠道微生物群,是指生活在人类肠道中的微生物的总体,包括细菌、真菌、病毒和原生动物等。近年来的研究显示,肠道菌群与人体健康之间存在着复杂而深刻的联系。
消化与营养吸收:肠道菌群帮助分解那些人类消化酶难以处理的复杂物质,如纤维素。这不仅有助于食物的消化,还能促进必要营养素的释放和吸收,如短链脂肪酸,它们是肠道细胞的主要能量来源。
免疫系统调节:肠道菌群在维持和调节人体免疫系统中扮演关键角色。一方面,它们帮助建立免疫耐受,防止对食物或环境中的无害物质过敏反应。另一方面,它们也可以激活免疫细胞,帮助身体抵御病原体。
影响心理健康:越来越多的研究表明,肠道菌群通过“肠-脑轴”影响人的心理健康。例如,一些肠道菌能产生神经递质,如血清素和多巴胺,这些物质是影响情绪和行为的关键因素。研究发现,肠道菌群失衡与抑郁症、焦虑症等心理疾病有关。
慢性病风险:肠道菌群的不平衡也与多种慢性疾病的风险增加有关,包括肥胖、2型糖尿病、心血管疾病等。例如,某些菌群组成的变化可能影响机体的能量平衡和炎症状态,进而影响这些病症的发展。
新生儿与婴儿发育:肠道菌群的建立始于出生之时,初生儿的菌群组成受分娩方式、哺乳和早期接触的抗生素等多种因素影响。健康的肠道菌群对婴儿的免疫系统发育和整体健康都极为重要。
父体微生物组的变化影响后代健康
该研究通过综合分析父体微生物组的改变如何影响后代的健康和发展,得出了父体微生物组变化通过表观遗传机制(epigenetic mechanisms)影响后代健康的结论。
研究首先通过给予雄性小鼠不同的抗生素或渗透性泻药来人为改变其肠道微生物组(gut microbiome)。这一步骤旨在模拟环境因素如何通过肠道微生物组影响父体的生理状态。
研究着重观察了改变父鼠微生物组后,其精子中小RNA(small RNA)的变化,以及这些变化如何通过精子传递给下一代。精子中的小RNA被认为可以携带表观遗传信息,影响后代的基因表达。
通过测定后代中特定基因的DNA甲基化(DNA methylation)状态,研究评估了父体微生物组变化对后代基因表达的影响。DNA甲基化是一种重要的表观遗传修饰,能够调控基因的活性。
通过使用高通量测序数据,研究应用统计模型来评估父鼠微生物组变化与后代健康状况之间的相关性。采用的统计方法包括方差分析和回归模型,确保了结果的可靠性和科学性。
研究观察到,受影响的后代表现出低出生体重、生长限制和早期死亡的风险增加。这些表型变化与父鼠微生物组的改变有直接关联。
通过这些详细的实验操作和分析,研究揭示了一个新的机制:父体的环境和生理状态,特别是肠道微生物组的状态,可以通过表观遗传路径影响到下一代,这一过程可能涉及到精子中的小RNA和DNA甲基化状态的改变。
微生物组与代谢健康的关联
该研究通过一系列实验,收集了关于父体微生物组变化如何影响后代代谢健康的数据,研究中,对受试的父鼠及其后代进行了详细的生理和代谢参数测定。通过比较接受不同微生物组处理的父鼠(如给予非吸收性抗生素和渗透性泻药)与未处理的对照组,分析了后代的出生体重、生长速度和存活率。
后代的低出生体重、生长受限和早期死亡率的增加与父鼠微生物组的改变直接相关。
通过分析改变微生物组的父鼠精子中的小RNA(small RNA)负载,研究揭示了这些小RNA在精子中的变化模式。这些小RNA被认为是影响后代基因表达的表观遗传因子。
对后代的DNA进行甲基化分析,特别是在关键的代谢调控基因区域,比较了来自不同处理的父鼠的后代之间的甲基化差异。这些数据显示,父鼠微生物组的改变导致后代在某些基因的甲基化模式上发生了显著变化,这些基因通常与代谢健康相关。
通过液相色谱-质谱联用技术(LC-MS)分析了父鼠及其后代体内的代谢物,研究发现父鼠微生物组的改变与后代体内特定代谢物的变化之间存在显著关联。这些代谢物主要涉及能量代谢和免疫反应。
表观遗传修饰的影响
该研究通过全基因组双硫酸盐测序(Whole-Genome Bisulfite Sequencing, WGBS)对父鼠精子的DNA甲基化进行了详细分析,揭示了精子中DNA甲基化变化与微生物组(microbiome)扰动之间的联系。
研究中,对处理和未处理的父鼠精子样本进行了DNA甲基化的测定。使用50个CpG位点为单位,对甲基化水平进行量化,这种方法可以细致地反映出基因组范围内甲基化的分布和变化。
研究中识别了21个显著的差异甲基化区域(DMRs),这些区域主要位于CpG岛。通过使用读取深度敏感的逻辑回归(logistic regression),对这些区域的甲基化变化进行了统计分析,P值小于0.05且甲基化水平变化超过20%被认为是显著的。
通过火山图(Volcano Plot)展示了甲基化变化的效应大小和统计显著性,从而直观地标识出那些在父鼠微生物组受扰动后,精子中甲基化水平发生显著变化的基因区域。
同时,通过基因组追踪(genome track)图展示了具体DMR的甲基化水平,进一步证实了微生物组变化与甲基化模式变化之间的直接联系。
这些数据不仅展示了父体微生物组变化对精子DNA甲基化具有深刻影响,而且揭示了这些甲基化变化可能通过影响后代的基因表达来调节其生理和代谢功能。
父体环境因素的整合作用
该研究详细分析了环境因素,特别是饮食和抗生素暴露,如何通过改变父体肠道微生物组(gut microbiome)进而影响精子的表观遗传状态(epigenetic state)和功能。这些环境因素通过微生物组介导的途径间接调控生殖细胞的表观遗传标记,影响后代的健康和发展。
环境因素对肠道微生物组的影响
抗生素和特定饮食习惯可以显著改变肠道微生物的组成和功能。抗生素通过减少肠道中的微生物多样性和丰度,改变微生物群落结构,而特定的饮食成分(如高脂肪或高纤维)可以增加或减少特定微生物的比例。
微生物组变化对精子表观遗传的影响
研究发现,肠道微生物组的变化能通过分泌代谢产物或调节宿主的免疫和激素水平间接影响精子的表观遗传标记。例如,微生物产生的短链脂肪酸(short-chain fatty acids, SCFAs)被认为可以通过血液循环到达生殖器官,影响精子中的DNA甲基化(DNA methylation)模式。
表观遗传状态与后代健康的联系
通过精子传递的表观遗传标记(如DNA甲基化和小RNA)可以在没有改变基因序列的情况下影响后代的基因表达。这意味着父体通过环境暴露改变的表观遗传标记可以跨代影响后代的表型和疾病易感性。
这些发现不仅加深了我们对环境因素如何通过微生物组和表观遗传途径影响后代健康的理解,也为开发新的预防和干预策略提供了科学基础。例如,通过调节饮食或使用特定的益生菌(probiotics)来优化生殖年龄人群的肠道微生物组,可能有助于改善后代健康。
后代健康的多重分子机制
脂质代谢物的变化
研究发现,由于父体肠道微生物组的扰动,特定的脂质代谢物在精子中的含量发生了显著变化。这些代谢物包括甘油磷脂(glycerophospholipids)和类固醇生成相关的代谢物(steroidogenesis-related metabolites),它们在精子的能量供应和信号传导中扮演关键角色。通过转录组分析和代谢组学研究,观察到这些脂质代谢物的变化与精子的功能和生存能力直接相关。
瘦素的影响
瘦素是一种主要由脂肪细胞产生的激素,但也在精子中表达,对能量平衡和生殖功能至关重要。研究显示,肠道微生物组的改变通过影响瘦素的系统性水平和在精子中的表达来影响精子的生理状态。通过ELISA验证,发现抗生素诱导的菌群失调显著降低了瘦素在血液和睾丸中的水平,暗示瘦素可能在肠-生殖腺轴(gut-germline axis)中发挥调节作用。
小RNA
研究还发现精子中的小RNA谱发生了重要变化,这些小RNA,如miR-141和miR-200a,对精子的表观遗传调控和后代的基因表达模式具有潜在的调控作用。通过高质量的小RNA文库分析,研究指出特定的小RNA在精子中的丰度发生变化,可能影响精子的成熟和功能,以及它们将如何影响下一代的发展。
父体肠道微生物组的重要性
对后代体重和生长的影响:研究显示,父体肠道菌群的紊乱可以导致新生小鼠体重显著降低,并增加严重生长受限(SGR)的易感性。这表明父亲在受孕前的菌群健康状况可以影响其后代的初期生长轨迹和整体健康。
可逆性和恢复效应:研究中的一个有趣发现是,对后代的负面影响,如低体重和高死亡率,是可逆的。父体肠道菌群的恢复,即使在显著紊乱后,也会导致后代健康生长模式和生存率的恢复。这种可逆性强调了父体肠道菌群在影响后代结果方面的动态和重要作用。
对后代死亡率的影响:研究结果显示,父体肠道菌群的失调与后代死亡率增加直接相关。这种关系在经历严重生长限制的后代中表现得尤为明显,这进一步与父体的菌群健康状况有关。
对后代健康的概率性影响:父体肠道菌群以概率性方式影响后代健康,表明虽然不是所有后代都同样受影响,但随着父亲肠道菌群紊乱程度的增加,不良健康结果的风险也在增加。
对公共健康政策的潜在影响
增强生育前健康的重视:传统上,孕前和孕期健康关注往往集中在母亲身上。这项研究强调了父亲在受孕前的健康,尤其是肠道菌群健康,对后代的长期健康影响同样重要。公共健康政策可能需要调整,增加对准父母双方的健康指导和支持,尤其是在生育计划阶段。
开展父亲健康教育和干预措施:政策制定者可以考虑实施针对父亲的健康教育项目,强调营养、肠道健康以及其对后代健康的可能影响。这可能包括提供关于如何通过饮食、生活方式改善肠道菌群的信息。
研究与政策制定:这项研究还突显了需要更多研究来探索父亲健康与子代健康之间的联系。公共健康政策应当支持这类研究,以便基于证据制定更全面的生育健康政策。
整合医疗服务:鉴于父亲的健康状况直接影响到下一代,公共健康政策可以考虑如何更好地整合男性健康服务,特别是在生殖健康和预防医学领域。
公众意识提升:通过媒体和公共健康宣传,增加公众对父亲在孕前和孕期健康中作用的认识,这可以帮助改变公众对生育健康的传统观念,促进男性更积极地参与到生育前准备中。
潜在的局限性
模型选择:研究主要使用了小鼠模型进行实验,虽然小鼠作为模型动物在生物医学研究中具有广泛应用,但其生理和遗传特性与人类存在差异。因此,研究结果的人类适用性(applicability to humans)需要谨慎考虑,未来研究需要在更多种生物模型上验证这些发现的普适性。
数据解读的复杂性:虽然研究使用了生物信息学和统计方法来分析数据,但在解释复杂的生物过程和多变量相互作用时,仍可能存在解读上的局限。例如,在表观遗传标记的分析中,DNA甲基化和小RNA的数据解析需要高度精确的生物信息学支持,任何技术或计算误差都可能影响最终的解释。
控制变量的难度:在探讨环境因素(如饮食和抗生素使用)对肠道微生物组及其通过表观遗传机制影响后代的研究中,完全控制所有相关的环境和遗传变量是一个挑战。此外,实验中使用的抗生素和特定饮食对微生物组的影响可能具有特异性,不同类型和剂量的抗生素可能产生不同的效应。
潜在的研究方向
微生物群与遗传因素的互作机制 (Interaction Mechanisms between Microbiome and Genetic Factors)
未来研究可以更深入地探索微生物群与宿主遗传因素如何相互作用,尤其是它们如何通过表观遗传机制 (epigenetic mechanisms) 影响生殖健康和后代发展。研究这一领域可以揭示新的调控生殖和发育的生物学路径。
临床应用与干预措施 (Clinical Applications and Interventions)
考虑到微生物群扰动对生殖健康的潜在影响,开发针对性的临床干预措施可能非常有价值。这包括开发新的益生菌治疗方法或调整饮食习惯来优化微生物群,从而改善生育能力和胎儿健康。
跨物种的比较研究 (Cross-Species Comparative Studies)
扩展到非模型生物的研究可以提供更广泛的生物学见解,有助于理解微生物群扰动在不同生物体中的作用机制。这种跨物种的研究方法能够揭示更普遍的生物学规律和潜在的治疗靶点。
原文链接
Argaw-Denboba A, Schmidt TSB, Di Giacomo M, Ranjan B, Devendran S, Mastrorilli E, Lloyd CT, Pugliese D, Paribeni V, Dabin J, Pisaniello A, Espinola S, Crevenna A, Ghosh S, Humphreys N, Boruc O, Sarkies P, Zimmermann M, Bork P, Hackett JA. Paternal microbiome perturbations impact offspring fitness. Nature. 2024 May 1. doi: 10.1038/s41586-024-07336-w. Epub ahead of print. PMID: 38693261.
https://www.nature.com/articles/s41586-024-07336-w