结直肠癌在我国的发病率呈逐年上升的趋势,世 界卫生组织国际癌症研究机构(International Agency for Research on Cancer,IARC)数据显示,我国 2020 年结直 肠癌的新发病例数为 56 万例,因结直肠癌死亡病例达 29 万例 。 约 25%的结直肠癌患者在诊断时已出现远 处转移,此外,25%的患者在治疗过程中发生转移,晚期 患者预后较差,5 年生存率不足 15%。 分子标志物检 测是筛选靶向治疗获益人群的前提,近年来随着检测 技术的飞速发展,高通量测序,也称为下一代测序( next generation sequencing,NGS),因其在通量、成本及效率 等方面的综合优势,在肿瘤基因突变检测中展现出越 来越广阔的应用前景。 然而 NGS 检测技术流程复杂, 对实验室环境条件、人员能力及质量管理要求高,任何 一个环节出现问题,均会影响检测结果的准确性,进而影响临床决策。
为保证临床诊疗工作的准确性和规范性,本共识由临床医师结合结直肠癌实际诊疗需求发起,业内诸多检测公司参与,病理及检验专家指导,从结直肠癌 NGS 检测的临床角度及实验室流程质控角度共同起草中国专家共识,以指导 NGS 检测技术在结直肠癌诊疗中的规范应用。
1,生物标志物在结直肠癌中的临床意义
目前较明确的肠癌相关遗传性疾病主要有 3 类:Lynch 综合征、家族性腺瘤性息肉病 ( familial adenomatous polyposis,FAP)和黑斑息肉病(P⁃J 综合征)。 同时《中国临床肿瘤学会 ( CSCO) 结直肠癌诊疗指南 2020 版》 针对遗传性结直肠癌筛查和基因诊断制定了原则。

FAP 推荐进行 APC 外显子测序/片段缺失测序,有突变提示 FAP 或衰减型 FAP(AFAP);无突变 则推荐行 MUTYH 外显子测序 / 片段缺失测序,有突 变提示 MUTYH 相关息肉病(MUTYH⁃associated pol⁃ yposis,MAP)。 对于无任何已知的息肉病综合征基因 的致病性变异,首选多基因突变检测,多基因 Panel 应包括所有息肉和结直肠癌相关基因。
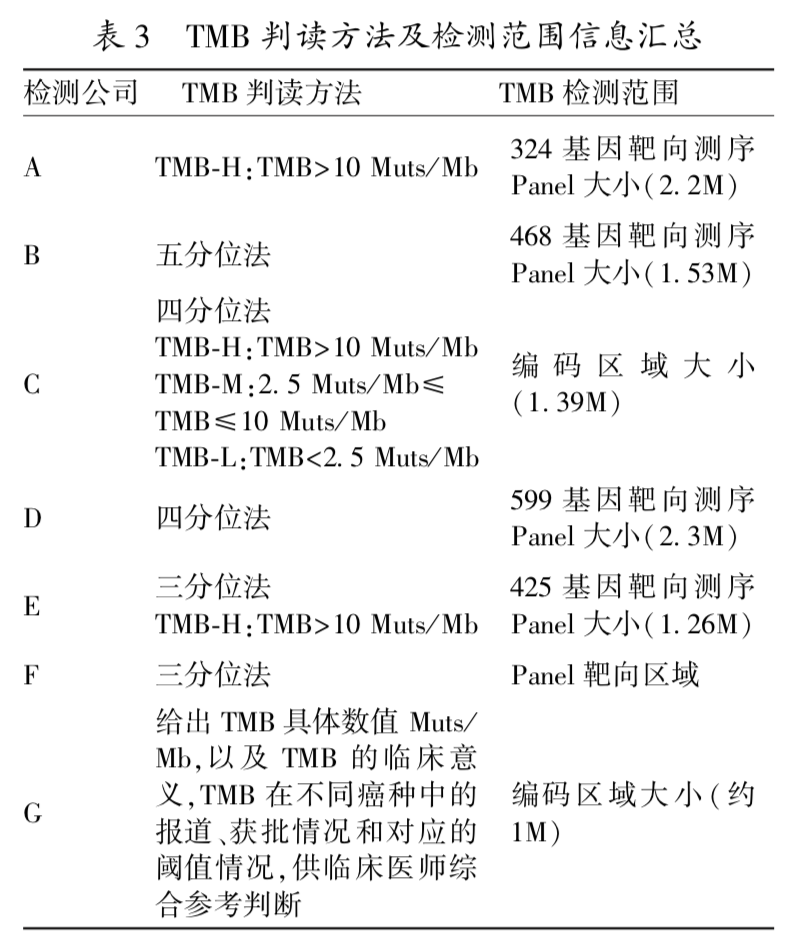
结直肠癌中常见 TMB 判读方法及检测范围汇总
TMB 检测有助于帮助筛选免疫治疗潜在获 益的患者,显著提升晚期恶性肿瘤患者的客观缓 解率和总生存期。 MSI⁃H/dMMR 通常也伴随 TMB⁃H,MSI⁃H 肿瘤样本中有约 83%表现为 TMB⁃H,且有 97%的样本 TMB≥10 Muts/ Mb。 在临床研究和实践过程中,TMB 的评估判读标准 在不同癌种中存在差异,而不同靶向测序 Panel 的 TMB 检测体系之间 TMB 阈值不能通用。
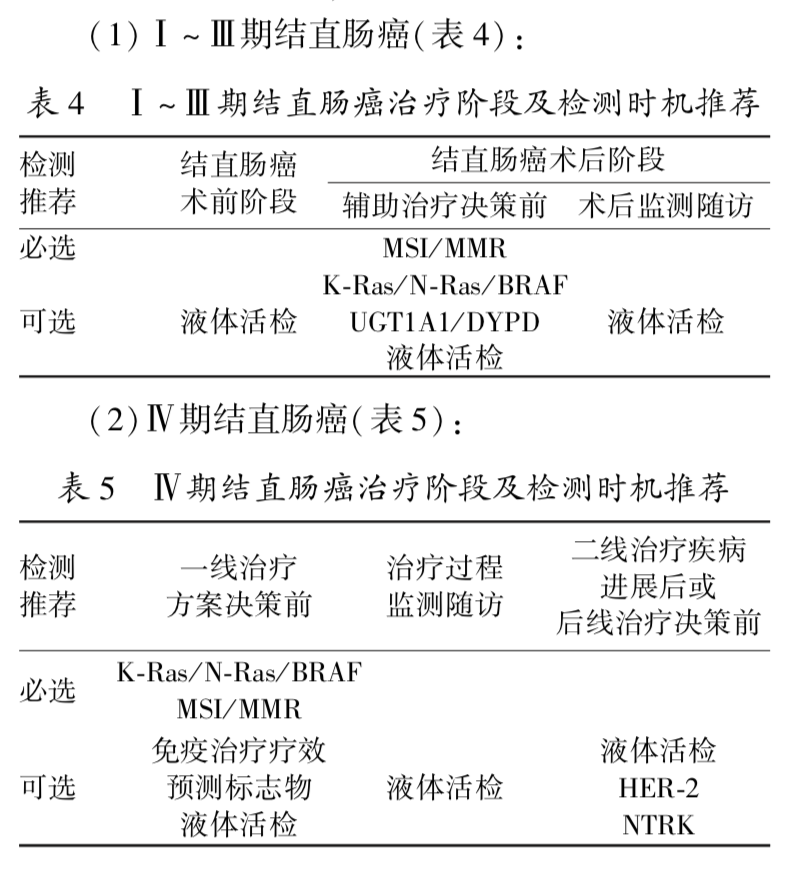
患者制定相关治疗方案的过程,结合结直肠癌生物标志物相关临床意义,建议检测作如下推荐 :
2,样本处理及转运
FFPE 样本为保证核酸质量,手术或活检
组织应在离体 30 min 内浸入到 100 ml 的 4%甲 醛溶液中进行固定,避免使用酸性及含有重金属 离子的固定液。 其中,大标本固定时间为 6 ~ 48 h,不超过 72 h;小活检体可固定 6 ~ 12 h。 对 其中 1 张 FFPE 样本进行切片染色,并在显微镜 下观察肿瘤细胞的含量和数量。 若肿瘤含量不 足,则实验室需要对通过富集后符合质量要求的 标本进行评估,或者制备成 FFPE 细胞学蜡块后 进行核酸提取。 值得注意的是,开展 NGS 检测前 应通过 HE 染色评估肿瘤细胞含量,至少满足肿 瘤细胞含量在 20%以上。
手术或活检的新鲜组织样本
新鲜组织可提取到高质量的核酸。 新鲜组织应在离体 30 min 内 将其保存于液氮罐或者-80 °C 冰箱中,防止 RNA 等 核酸降解。 如需评估肿瘤细胞含量,可采用冷冻切 片染色体方法,若肿瘤细胞含量不足,可通过标记 肿瘤区域进行富集。 新鲜组织可在液氮、-80 °C 冰 箱或稳定剂中长期保存。
血浆样本
对于存在于血浆中的循环 DNA, 即 ctDNA,取样时可使用专用的 ctDNA 保存管采血, 采血后轻柔颠倒 8 ~ 10 次,确保采血管中的 ctDNA 保存液与血液充分混匀,常温转运保存即可,严禁 冻融血液;到达实验室后,分离血浆,提取游离 DNA[26] 。 也可使用一次性 EDTA 抗凝真空采血管, 采集 8 ~ 10 ml 全血,冷藏运输,2 h 内分离血浆,提 取游离 DNA,如需保存,请置于-80 °C 冰箱中,并避 免反复冻融。
样本运送规范
送标准操作规范( SOPs) 以确保运送过程中各类样 本的安全性和过程的可控性(详见第 4 节)。 石蜡 材料可以常温运输,血液样本需要在干冰条件下运 输,核酸样本需在 4 °C或冷冻条件下运输。
3,报告解读及标准模板
NGS 临床报告包含内容
基因检测的临床报 告应当包括:(1)基础信息:实验室名称、实验操 作人员、报告审核人员、联系方式。 (2)受检者的 基本信息:应包括受检者姓名、性别、出生日期、 接受检测的日期、检测的目的和受检者的临床指 征等。 (3)样本的信息:样本类型,如 DNA、外周血、唾液、新鲜组织、FFPE 组织等;采集时间和采 集部位、样本编号、送检时间、检测报告时间和样 本主要质控情况,如 DNA 质量评估以及测序质 量评估等。 (4)检测项目:基因 Panel 的检测位 点及 检 测 范 围、 检 测 仪 器、 检 测 试 剂, 是 否 为 NMPA 批准使用的检测试剂以及 NMPA 获批的 基因位点信息,或实验室自建检测( laboratory de⁃ veloped tests,LDTs) 试剂、检测方法、检测范围、检 测下限(LoD)等。 (5)检测结果及变异解读:对 基因变异的检测结果进行解读,如检出的基因 型、变异结果、染色体变化情况、检测结果的致病 性分级、药物信息及临床意义、变异解读引用的 参考文献等。 (6)标注检测方法的实验室内部验 证结果,检测局限性及不确定性,进一步检测的 建议。
基因变异的命名
对基因变异的描述应遵循 一定的原则和规范,推荐使用人类基因组变异协会 命名指南(www.hgvs.org),转录本的选择建议采用基因座参考基因组序列数据库( Locus Reference Ge⁃ nomic, https:/ /www.lrg⁃sequence.org) 界定的转录本或者多个国际数据库公认的主要转录本。 对遗传性结直肠癌相关基因变异的说明,建议以美国医学遗传学学院( American College of Medical Genetics and Genomics,ACMG;https:/ / www.acmg.net)指南为标准,在检测结果中列出具体的变异位点信息,包括基因名称、所参考的人类基因组版本号、转录本参考序列版本号、核苷酸变异、氨基酸变异、外显子 / 内含子序号、等位基因杂合性、染色体编号及坐标等等。
临床意义的解读和批注
对于肿瘤体细胞突变,采用分级处理的方式 综合伴随诊断、临床指南、数据库或文献证据,可 以将肿瘤体细胞基因突变分为临床意义明确(I 级)、有潜在临床意义(II级)、临床意义不明确(III 级) 和良性或可能良性突变( IV级) 。 实验室需要建立分类及分级和报告的 SOPs,SOPs 应至少包括两 个方面:(1) 对体细胞基因突变进行分级的流程; (2)在日常检测中报告哪一级或哪几级突变位点。 分级的流程应有记录,包括证据来源的指南、文献、 数据库、证据等级、分级结果等。 临床证据决定突 变位点分级,可根据《高通量测序技术临床规范化 应用北京专家共识》发表的体细胞突变位点和临 床证据分为以下 4 级。

对胚系突变的检测
除了中外诊疗指南及 重要参考文献外,另有 Online Mendelian Inheritance in Man (http:/ /omim.org)和美国 ACMG 可参考。 ACMG 指南将变异位点致病性的等级分为致病、疑 似致病、临床意义未明、疑似良性和良性 5 个等级。 报告中应列出与遗传性结直肠癌(如 FAP、Lynch 综 合征等)相关的致病以及疑似致病变异,并对变异 的致病性进行分析解读[28] 。
意义不明位点的处理
无论是肿瘤体细胞 突变,或是胚系突变,都存在意义不明位点。 实验 室需制定相关政策用来确定是否报告或者不报告 临床意义不明的位点,并附上说明和参考数据库, 并且要在报告中注明本实验室出具临床报告的 规则。
DPYD 检测结果
中等代谢型患者,应基于 活性分值降低起始剂量;慢代谢型应避免使用氟尿嘧 啶及其前体药物。 UGT1A1 检测结果中,UGT1A1∗28 和∗6 为纯合变异型或双杂合变异型的患者应降低 伊立替康的剂量,推荐剂量为 150 mg / m2 。
低丰度突变结果的处理
对样本进行 NGS 检 测时如出现较低丰度的突变结果( 通常组织学样本低于 5%,血液样本低于 1%或低于检测 LoD)时,建 议综合评估 NGS 实验平台性能、测序深度以及肿瘤 细胞比例等因素综合考虑。 特别对于靶向治疗相 关的基因建议使用其他检测方法进行进一步验证 确认(如 Sanger,dPCR 等)。
知情同意
建议提供患者手写或者在线版的知情书。
报告模板
实验室应根据检测项目,给出对应 的检测报告模板(表 7),并形成 SOP 文件。 模板中 应明确列出检测报告中应提供的信息,如患者基本 信息、样本信息、检测信息、检测结果、结果解释、实 验室信息、检测方法的局限性以及其他内容等。
原始出处
中国抗癌协会肿瘤靶向治疗专业委员会.结直肠癌分子检测高通量测序中国专家共识 .临床肿瘤学杂志 2021 年 3 月第 26 卷第 3 期 Chinese Clinical Oncology,Mar. 2021,Vol.26,No.3