随着基因治疗技术的迅速发展,人们对于治疗基因相关疾病的方法和效果越来越感兴趣。然而,评估基因治疗策略的有效性往往需要进行大量的动物实验,而常规的小鼠模型由于其与人类生物学特征的差异,限制了其在基因治疗研究中的应用。因此,为了更准确地评估基因治疗在人类身上的效果,建立一种人源化小鼠模型显得尤为重要。

腺相关病毒(AAV)是一种常用的基因治疗载体,经过多年的载体开发和临床试验,两种不同的AAV血友病基因疗法(Hemgenix和Roctavian)已获得FDA批准。临床前开发的一个重要教训是,实验动物模型很难预测人类 AAV 转导和体内药理学。尽管目前评估的所有 AAV 血清型在实验动物模型中都显示出亲肝性,但肝脏和其他器官中的摄取、入核、脱壳、第二链合成以及转基因表达/沉默方面存在差异。
人肝嵌合小鼠允许在体内验证 AAV 在原代人肝细胞中的作用。这些人源化小鼠实现了高人嵌合性,可用于评估体内人肝细胞的 AAV 转导效率。
在这项研究中,作者描述了一种人类肝脏嵌合非转基因TIRFA小鼠模型,通过将肝脏人源化与AAV受体(AAVR)相结合,克服了这一翻译障碍消融,使小鼠细胞不允许 AAV 转导。使用人肝嵌合 TIRFA 小鼠,研究人员证明与野生型 AAVR 人源化小鼠相比,临床使用的 AAV 血清型在原代人肝细胞中的转导有所增加。此外还证明了 AAV 在人畸胎瘤来源的原代细胞和肝癌组织中的转导,展示了人源化 TIRFA 小鼠的多功能性。
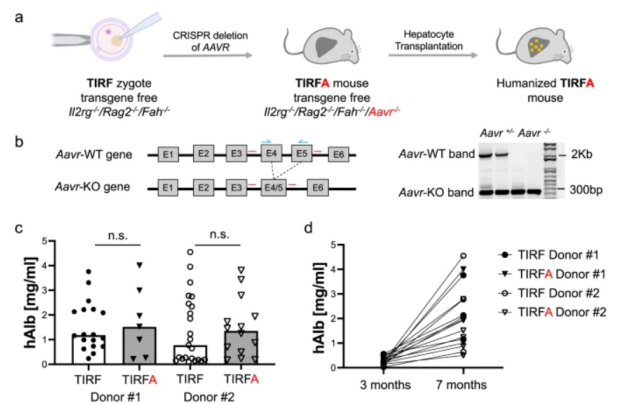
为了充分利用 TIRFA 小鼠的人源化,研究人员生成了人类畸胎瘤模型,该模型可从所有三个胚层产生人体组织。这样的模型应该能够在任何所需的人体组织中验证 AAV 的向性。同样,研究人员将患者来源的人类肝癌组织移植到人源化 TIRFA 肝脏中,并以相同剂量注射 AAV9-tdTomato 载体。正如预期的那样,研究人员在人类原代肝细胞和人类肝癌样本中检测到了 tdTomato。
总之,该研究引入了一种多功能小鼠模型,可以在体内选择性地研究 AAV 的趋向性和生物学特性。结果证明,AAV 载体在人肝嵌合 TIRFA 小鼠中静脉注射时,可以更容易地转导人肝细胞而不是鼠肝细胞,并且可用于评估其他人类细胞和靶组织。TIRFA小鼠克服了当前实验动物模型所带来的重大限制,并且应该能够预测肝脏定向AAV基因疗法的体内药理学以及在人类环境中研究AAV生物学。
原始出处:
Barzi, M., Chen, T., Gonzalez, T.J. et al. A humanized mouse model for adeno-associated viral gene therapy. Nat Commun 15, 1955 (2024). https://doi.org/10.1038/s41467-024-46017-0
Nature:基因治疗的价格应该平民化!
![]() 0
2023-05-01
点击查看
0
2023-05-01
点击查看

全球首个结晶样视网膜变性基因疗法I/II期临床入组完成
![]() 0
2023-09-21
点击查看
0
2023-09-21
点击查看

Nat Med:最新临床试验表明基因治疗早期过程可能导致血液干细胞的癌症相关突变
![]() 0
2023-12-19
点击查看
0
2023-12-19
点击查看

杨仁池教授:从长效凝血因子和非因子治疗到基因治疗,血友病治疗正走向治愈
![]() 0
2024-01-09
点击查看
0
2024-01-09
点击查看

Lancet:全球首个!复旦大学舒易来等多团队合作开发新的治疗方法,首次使耳聋患者的听力恢复
![]() 0
2024-01-25
点击查看
0
2024-01-25
点击查看

Lancet:舒易来教授发表全球首个遗传性耳聋基因治疗临床试验结果
![]() 0
2024-01-27
点击查看
0
2024-01-27
点击查看
