NEJM:Larotrectinib对TRK融合阳性肿瘤治疗效果显著
![]() 0
2018-02-22
点击查看
0
2018-02-22
点击查看

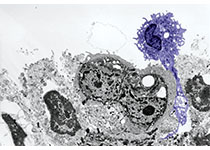
Lancet oncol:Larotrectinib用于携带TRK融合基因的肿瘤患儿,疗效明显且耐受性好
![]() 0
2018-03-30
点击查看
0
2018-03-30
点击查看
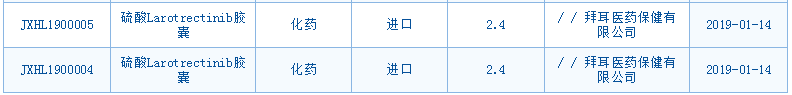
超快!Loxo和拜耳的不限癌种靶向药larotrectinib在中国申报临床获受理
![]() 0
2019-01-14
点击查看
0
2019-01-14
点击查看

超快!Loxo和拜耳的不限癌种靶向药Larotrectinib在中国申报临床获受理
![]() 0
2019-01-14
点击查看
0
2019-01-14
点击查看
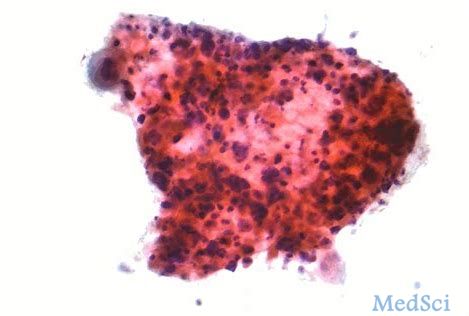
拜耳公布larotrectinib治疗NTRK基因融合阳性转移性非小细胞肺癌患者的亚组分析结果
![]() 0
2019-04-12
点击查看
0
2019-04-12
点击查看
加拿大卫生部批准VITRAKVI®(larotrectinib)治疗NTRK基因融合的晚期实体瘤
![]() 0
2019-07-31
点击查看
0
2019-07-31
点击查看
