嗜酸性粒细胞是影响T细胞介导的抗肿瘤免疫的重要免疫效应细胞。然而,嗜酸性粒细胞的低频率和抑制活性特点限制了癌症免疫疗法的发展。
在本研究中,南洋理工大学浦侃裔教授等人报道了一种嗜酸性粒细胞活化的半导体聚合物纳米颗粒(SPNe),用于改善光动力学肿瘤免疫原性,调节嗜酸性粒胞趋化性,并重振T细胞免疫以激活癌症光免疫治疗。在局部NIR光照射后,SPNe可以产生1O2以引发肿瘤的免疫原性细胞死亡并诱导二肽基肽酶4(DPP4)抑制剂西他列汀的特异性激活。随后对DPP4的抑制增加了肿瘤内CCL11水平,从而促进了嗜酸性粒细胞的趋化性和活化。SPNe介导的光免疫疗法与免疫检查点阻断协同作用,极大地促进了肿瘤的浸润和嗜酸性粒细胞和T细胞的活化,有效抑制了肿瘤的生长和转移。因此,本研究提供了一种通用的聚合物纳米平台,用于调节癌症免疫疗法的特异性免疫细胞。相关工作以“Eosinophil-activating Semiconducting Polymer Nanoparticles for Cancer Photo-immunotherapy”为题发表在Angew。

【文章要点】
如图1所示,SPNe是由嗜两性半导体聚合物(PCPDTODBT-PEG-TK-西他列汀)自组装而成。这种聚合物则是通过将二肽基肽酶IV(DPP4)抑制剂(西他列汀)与聚乙二醇(PEG)通过1O2可裂解接头(硫酮)偶联,并进一步与半导体聚合物(PCPDTODBT)偶联而合成的。在全身给药后,SPNe可以通过增强的渗透性和滞留作用在肿瘤部位积聚。
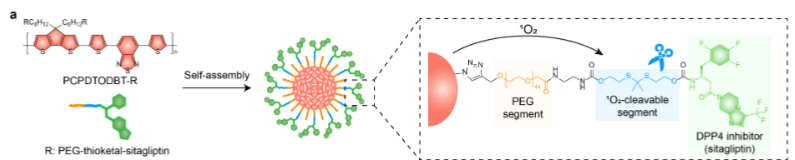
图1 SPNe的设计
聚焦近红外光照射肿瘤部位后,SPNe能够产生细胞毒性1O2杀死肿瘤细胞并诱导免疫原性细胞死亡(ICD),导致损伤相关分子模式(DAMP,包括高迁移率组蛋白B1(HMGB1)、IL-33、ATP等)和肿瘤相关抗原的释放,以及树突状细胞(DC)的成熟,增强肿瘤免疫原性。随后,产生的1O2可解离硫缩酮连接体以诱导西他列汀的释放,西他列丁可以抑制DPP4活性,并抑制DPP4介导的嗜酸性粒细胞募集和激活化学引诱剂(CCL11)的降解,导致肿瘤浸润性嗜酸性粒胞的上调。在与免疫检查点抑制剂(抗CTLA-4抗体)组合后,细胞毒性T淋巴细胞(CTL)可以通过增加IFN-γ分泌进一步活化,以提高嗜酸性粒细胞的活性。结果,这种激活嗜酸性粒细胞的SPNe可发挥协同的光免疫治疗作用来抑制肿瘤进展和转移(图2)。
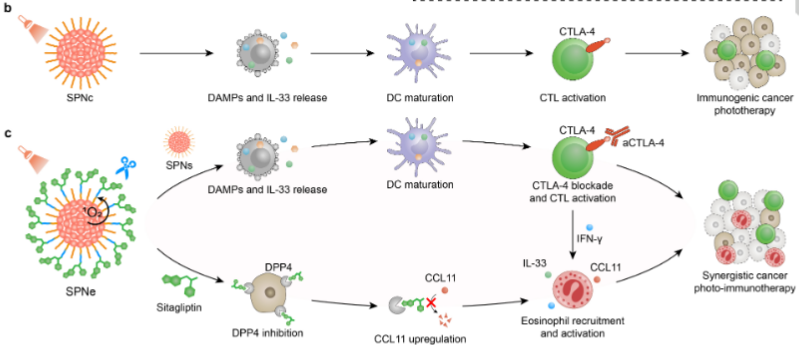
图2 SPNe介导的免疫原性癌症光疗法
原文链接:
https://onlinelibrary.wiley.com/doi/10.1002/anie.202405358
上海交大/华师大合作Nature Sustainability:癌症诊断方法新突破!几分钟内,诊断多种癌症!
![]() 0
2024-04-24
点击查看
0
2024-04-24
点击查看

【热点解读】2023 AFSEP建议:癌症和多发性硬化
![]() 0
2024-04-24
点击查看
0
2024-04-24
点击查看

Nat Metab:癌症导致的体重减轻,竟由「乳酸」驱动?北京大学团队找到“提高癌症患者生存期”的新方法
![]() 0
2024-04-24
点击查看
0
2024-04-24
点击查看

Nature:刷新认知!科学家首次证明,没有基因突变也会发生癌症
![]() 0
2024-04-28
点击查看
0
2024-04-28
点击查看

最新Nature大子刊:意外的发现,可促进抗肿瘤组织驻留T细胞!
![]() 0
2024-05-04
点击查看
0
2024-05-04
点击查看

青岛大学付钦瑞ACS Nano:过渡金属基纳米酶:合成、治疗作用机制及其在癌症治疗中的应用
![]() 0
2024-05-05
点击查看
0
2024-05-05
点击查看
