诺华公司今日宣布,美国食品药品监督管理局(FDA)授予了Kymriah®(tisagenlecleucel)再生医学高级疗法(RMAT)认定,以治疗复发难治(r / r)滤泡性淋巴瘤(FL)。Kymriah®(tisagenlecleucel)是一种FDA已经批准的CAR-T细胞疗法。复发难治FL则有可能成为Kymriah的第三个适应症。
诺华全球药物开发主管兼首席医学官John Tsai说:“这一认定将支持Kymriah的发展,Kymriah可以潜在改善某些滤泡性淋巴瘤患者的生存时间”。
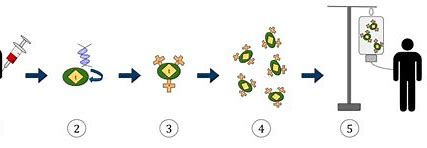
滤泡性淋巴瘤(FL)是非霍奇金淋巴瘤(NHL)的第二种最常见形式,是一种惰性淋巴瘤,约占NHL病例的22%。尽管有新的治疗方法可以改善总生存期,但FL被认为是一种无法治愈的恶性肿瘤。在复发性FL患者的整个生命周期中,他们可能会接受5-12线先前治疗,在大多数情况下,复发难治FL患者往往会耗尽治疗选择。
原始出处:
https://www.firstwordpharma.com/node/1717470
Blood:滤泡性淋巴瘤采用本达莫司汀联合利妥昔单抗治疗后早期病程进展提示高转化风险
![]() 0
2019-07-16
点击查看
0
2019-07-16
点击查看
Blood:早期和晚期滤泡性淋巴瘤的基因表达差异
![]() 0
2019-10-14
点击查看
0
2019-10-14
点击查看
Blood:二代测序揭示N-糖基化位点对滤泡性淋巴瘤发生发展的重要作用
![]() 0
2020-01-14
点击查看
0
2020-01-14
点击查看
Blood:局限性和晚期滤泡性淋巴瘤的基因表达差异!
![]() 0
2020-02-01
点击查看
0
2020-02-01
点击查看
TAZVERIK(tazemetostat)治疗滤泡性淋巴瘤:FDA已批准其NDA
![]() 0
2020-02-15
点击查看
0
2020-02-15
点击查看

英国NICE推荐将来那度胺与利妥昔单抗联合用于治疗滤泡性淋巴瘤
![]() 0
2020-03-02
点击查看
0
2020-03-02
点击查看