这种特殊的疾病,本科学习时多次在书本理论上见到。但由于发病率低,在
临床上难得一见,极易误诊。
一、脸色差,查出严重贫血、肾衰
这是一个叫小馨(化名)的4岁女孩,平素由外婆抚养,父母对病史陈诉不清。
2天前由他人提醒家长“患儿面色差”就诊,伴有中低热,热峰38.5℃。小女孩还有点咳嗽,父母以为只是普通感冒,在当地就诊。
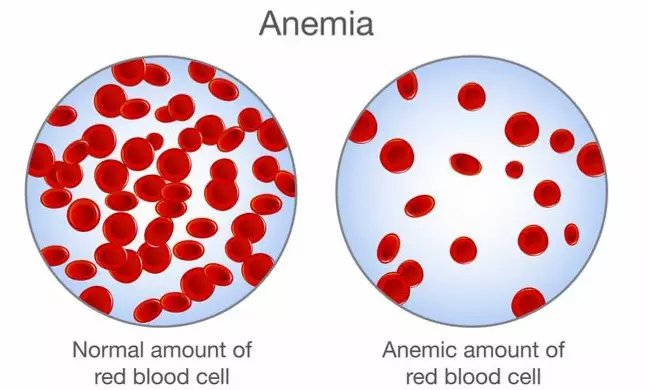
但一查血常规,却令所有人吓出一身冷汗——血色素竟然只有45 g/L(该年龄段Hb正常应>110 g/L)!脏器生化血肌酐451.6 umol/L,尿素氮512.9 umol/L。
鉴于病情危重,家属要求转至我院就诊。
图一:贫血
就诊后很快被收入急诊观察室,查体仅发现精神稍倦怠,皮肤黏膜苍白,呼吸心率稍快,肺部没有闻及干湿啰音。
入观
诊断:1.重度贫血;2.肾功能衰竭;3.支气管炎。
二、严重贫血是什么原因?
只有2天的病程,小馨的血色素就下降这么快,血跑哪里去了?
这是我们首先面临的棘手问题——小馨为何出现如此严重的贫血?
患儿没有呕血、黑便,
消化道出血引起的血色素下降可能性不大;没有咯血,且肺部未闻及明显湿啰音,肺部大出血可能性也不大;也没有手术史或外伤创伤病史,显然由于外伤所致的出血可能性也不大。
在
临床上,遇到短时间大量失血,且没有明显的
消化道和呼吸道出血及外伤史时,也一定要特别注意几个腔隙的出血、积血的可能,如胸腔、腹腔和盆腔。
而颅腔内出血,如果出血量较大,会有明显的神经系统症状和体征。况且由于颅脑空间有限,不太可能有太多血积于颅腔。后来的头颅CT也验证了医生的判断。
而其他腔隙出血常见于外伤、凝血功能异常等疾病。患儿无上述病史,查体也不支持这一判断。因此,出现腔隙出血的可能性不大。
贫血,短期血色素下降,除了要考虑出血的原因之外,还要考虑溶血性贫血、造血障碍。
患儿2天病程,无皮肤黏膜黄染,肝功能正常,尿胆红素、尿胆原、血胆红素均阴性,因此不考虑急性溶血性贫血。
而造血障碍,多为亚急性或慢性,病程较长,常有血象2系或3系下降。患儿只有红系异常,并不符合这种情况。
三、病史陈诉不清,如何去伪存真?
如上分析,患儿急性失血、溶血性贫血和造血障碍的可能性不大,再回看血常规示为小细胞低色素性贫血。
我们知道,急性失血或溶血性贫血多为正细胞正色素性贫血。而小细胞低色素性贫血多见于缺铁性贫血或慢性失血,而之所以还是第一时间考虑急性失血、溶血性贫血是基于以下3个原因:
其一,广东地中海贫血和蚕豆病的发病率非常高,这两类贫血常表现为小细胞低色素性贫血,在两广地区(广东广西)非常常见;
其二,患儿血色素已经下降至接近极重贫血,这么严重的贫血病程才2天,应当首选排除急性病因;
其三,急诊处理疾病的原则,应优先考虑急危重症的情况。
图二:重病史,去伪存真,方能初步预判
在询问病史时,医生有新的发现:小馨平素由外婆抚养,父母对小馨的情况一问三不知,病史询问困难。
此后补充病史,患儿2016年学校体检当时Hb正常,现在何时出现Hb下降、何时出现不适症状均难以考究。
病史可疑:
其一,如此低的血色素(假设从正常的血色素110 g/L下降至32 g/L),急诊评估仅为II级,临床表现并不突出(只是精神稍倦怠、发热、面色苍白),这和急性病程不相符;
其二,当询问患儿咳嗽、咳痰、咯血、尿色、尿量、毒物接触史等情况时,监护人的回答模棱两可。
医生大胆推断:小馨的病程肯定不止2天!
尽管病程的判断,对于临床医生的诊治思路有重大影响,但仍无法解释患儿贫血的病因。即便患儿是亚急性或慢性贫血,那贫血发生的原因又是什么?
四、肾衰是什么原因?与贫血有关?
患儿肾功能示血尿素氮、血肌酐均明显升高。
按照美国慢性肾功能不全(CKD)分级,达到了CKD 4级水平(准确分期依据GFR,初步判断可根据血肌酐水平),即肾功能衰竭期(即血肌酐超过445 umol/L,尿素氮超过20 mmol/L)。
尿液分析显示,尿潜血阳性,尿红细胞138个/HP,尿蛋白弱阳性(判断蛋白尿水平,不应以尿常规几个+为依据,而应以24 h尿蛋白为判断依据)。
那么,患儿的贫血是否为红细胞大量从尿液中流失所致的呢?
我们知道,IgA肾病临床以肉眼血尿或镜下血尿为主要表现,尿液分析红细胞常为几千个,但都很少出现如此严重的贫血。而患儿无肉眼血尿,仅为镜下血尿,如果单纯从尿液失血角度来看可能性并不高。
患儿存在血尿、蛋白尿,生化示低蛋白血症(血白蛋白29.5 g/L),没有明显水肿,也没有
高血压。生化示血肌酐及尿素氮明显升高,肾功能衰竭急剧恶化。
如果短时间内出现明显少尿,那我们有理由相信患儿发生了急进性或急性肾小球肾炎的可能。但很遗憾,由于病史询问不清,很难确定患儿是否有少尿的情况。
尽管从这个角度理解患儿肾功能衰竭的原因并非不可能,但如前所述,急进性肾小球肾炎及血尿并不能很好解释患儿出现严重贫血的原因。
那么,患儿的血到底从哪里丢失了呢?
五、突然病情恶化,从气道涌出鲜血
患儿伴有咳嗽等呼吸道
感染的症状,入观时很快行胸腹平片检查。
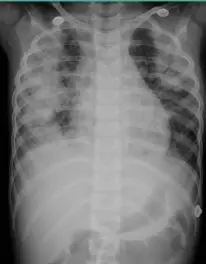
胸片提示双肺多发斑片渗出性病灶,腹部未见异常。阅片发现患儿双肺肺纹理增粗,双侧纹理可见界限不清的细网状、网粒状阴影。
患儿的呼吸道症状不突出,肺部查体也没有明显闻及杂音,肺部病变却较为突出。这种症状和检查的分离现象提醒我们,患儿的病情可能没有那么简单。
再结合患儿病史询问不清的情况,及其他脏器失血的可能性不高,那么患儿会是肺部慢性失血吗?
患儿入观不到2个小时,即出现烦躁不安,面色苍白加重,伴咯血、量大,经皮血氧饱和度进行性下降至70%~80%,心率增快。立即予清理呼吸道、呼吸机辅助通气、镇静镇痛及输血止血等治疗。
那么,患儿为何短时间内病情突然出现加重?出现咯血及肺部大出血的原因是什么呢?
急进性肾小球肾炎,进展迅速可能并发心力衰竭,出现急性肺水肿。患儿会不会出现上述情况呢?
患儿在咯血之前,肺部并未闻及湿啰音,也没有其他器官灌注不足、
血液回流障碍的征象(如肝大、下肢水肿、颈静脉充盈等),而且患儿为咯大量的血而非粉红色泡沫痰。后来的心脏彩超仅提示右房右室稍大(胸片心胸比大致正常),射血分数正常,更是进一步验证并非心力衰竭所致的病情变化。
六、胸片透露了可能的病因
患儿胸片示存在可疑界限不清的细网状、网粒状阴影,且和原本呼吸道症状体征分离的现象,并突然出现咯血、肺出血,提示我们患儿可能为肺含铁血黄素沉着症。
图三:患儿入观后拍的胸片,透露了可能的病因
肺含铁血黄素沉着症(pulmonary hemosiderosis),是一组肺泡毛细
血管出血性疾病,常反复发作,并以大量含铁血黄素积累于肺内为特征。
发病分两种情况:其一为暴发性起病多见,以反复咳嗽、气促等急性呼吸道症状伴咯血或呕血;其二仅以贫血伴嗜睡、衰弱而就诊。
图四:肺含铁血黄素沉着症常见的原发性和继发性病因
肺含铁血黄素沉着症,由于反复发作,肺泡广泛出血,可以出现肺内“铁扣押”,从而导致严重贫血。
但是,患儿出现低蛋白血症和肾功能衰竭的原因又是什么呢?
肺出血和肾炎,我们想到了本科《内科学》那个不起眼的疾病——肺出血-肾炎综合征!
七、肺出血-肾炎综合征≠Goodpasture综合征
肺出血-肾炎综合征,以肺出血和肾衰竭为主要临床表现,患者常首先有贫血表现,同时伴有气促、咳嗽并很快进展为咯血,还常伴有轻度发热。
值得一提的是,很多内科学教科书或文献,将肺出血-肾炎综合征等同于Goodpasture综合征,其实不够严谨。
肺出血-肾炎综合征可见于Goodpasture综合征、ANCA相关性
血管炎、系统性红斑狼疮(SLE)、系统性硬化病(SSc)和冷球蛋白血症等。
(一)Goodpasture综合征
Goodpasture综合征,狭义的肺出血-肾炎综合征,是一种少见疾病,其特征是反复咯血、肺部浸润、血尿和急性肾小球肾炎。
好发于中青年男性,男女比例为3~4:1,好发年龄为15~35岁。
发病前10%~30%的病例有上呼吸道
感染症状,病情发展迅速,预后凶险。患者常因咯血窒息、呼吸衰竭或肾功能衰竭而死亡。
(二)ANCA相关性血管炎
抗中性粒细胞胞浆抗体(ANCA)主要由感染、药物、二氧化硅等抗原物质刺激机体产生的针对中性粒细胞胞浆颗粒成分和单核细胞溶酶体的一类自身抗体。ANCA相关性血管炎(AASV)主要包括韦格纳肉芽肿病(Wegener’s granulomatosis)、显微镜下多动脉炎、Churg-Strauss综合征和FSNGN等一类疾病。
由于小儿AASV临床表现缺乏特异性,ANCA血清学检查又与多种自身抗体存在交叉反应。因此,极易误诊为系统性红斑狼疮(SLE)、Goodpasture综合征和类风湿性关节炎。
SLE虽然多见于女性,但绝大多数在青春期发病,与雌激素水平密切相关,肾脏病理可鉴别。
Goodpasture综合征主要是由于抗基底膜抗体(anti-GBM)随着
血液循环到达肾小球滤过膜和肺泡膜与GBM结合产生原位
免疫复合物沉积于毛细血管壁而引起血管炎,血清anti-GBM的测定有助于鉴别AASV与Goodpasture综合征。
此外,肾脏病理活检Goodpasture综合征可见anti-GBM,而AASV则没有。
图六:Goodpasture综合征
患儿血管炎四项核周型ANCA阳性(+)、髓过氧化物酶抗体阳性(+),抗肾小球基底膜抗体 阳性(+)。血清anti-GBM的测定有助于鉴别AASV与Goodpasture综合征,因此患儿为Goodpasture综合征。
Goodpasture综合征诊断需具备三个条件:肺出血、肾小球肾炎及抗GBM抗体阳性。
有研究表明,anti-GBM滴度和ANCA抗体均阳性的患者通常比单纯GBM抗体阳性的患者预后更差,死亡率更高。
Goodpasture综合征死亡率高,如不能及时、正确诊断治疗,迅速进展为终末期肾病或死于肺出血窒息,存活者也很少能完全恢复肾功能。
近年来,应用血浆置换、
免疫吸附、泼尼松治疗和免疫抑制剂的“三联疗法”取得了较大进步。
特别致谢
本病例据广州市妇女
儿童医疗中心急诊科(珠江新城院区)病例讨论整理,特别感谢朱翠平主任对病例的分析和指导,感谢所有参与讨论的医师的积极发言。
来源:医学界儿科频道
版权声明:
本网站所有注明“来源:梅斯医学”或“来源:MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有,非经授权,任何媒体、网站或个人不得转载,授权转载时须注明“来源:梅斯医学”。本网所有转载文章系出于传递更多信息之目的,且明确注明来源和作者,不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。同时转载内容不代表本站立场。
在此留言