BCMA/CD19 CAR-T
高危新诊断多发性骨髓瘤(NDMM)患者在标准治疗下往往预后不佳,需要新的有效的一线治疗来提高临床疗效。CAR-T细胞治疗作为肿瘤治疗免疫时代划世纪的新疗法,已在复发难治MM展示了良好的疗效和安全性。GC012F是一种自体BCMA/CD19双靶点CAR-T细胞疗法,开发于新型快速制备平台FasTCAR,可实现次日制备,研究证实治疗复发/难治性多发性骨髓瘤安全有效,但其作为适合移植的高危NDMM患者的一线治疗尚未得到充分探索。
海军军医大学第二附属医院(上海长征医院)血液病科杜鹃教授团队开展一项I期研究,评估了GC012F在高危NDMM患者中的安全性、有效性和药代动力学。结果近日发表于《JAMA Oncology》。

研究方法&结果
该研究为单臂、开放标签I期队列研究,纳入至少符合一个高危因素的NDMM患者。高危特征包括:诊断时R-ISS II期或III期;LDH水平高于正常上限;FISH检测到高危染色体异常(HRCA),即del(17p)、t(4;14)、t(14;16)或1q扩增≥4个拷贝[amp(1q21)];浆细胞瘤;属于Ig D或E亚型;或符合mSMART 3.0的高危标准。
患者接受2个周期的诱导治疗,然后输注GC012F (1×105细胞/kg、2×105细胞/kg、3×105细胞/kg三个剂量水平)。主要目的为评估GC012F在不同剂量水平下的安全性、有效性和药代动力学。
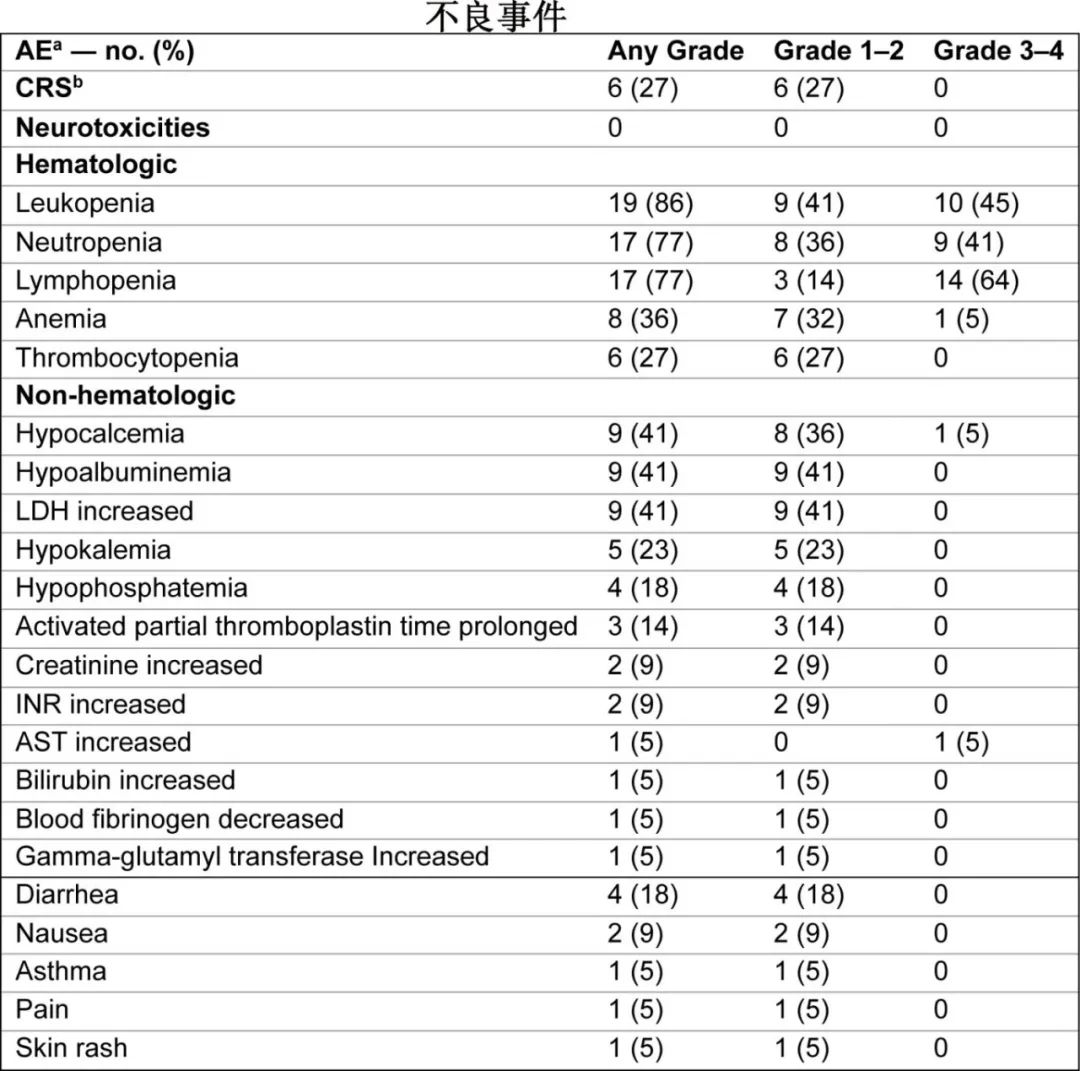
研究共纳入22例患者接受GC012F治疗并纳入安全性分析集,其中6例出现轻-中度细胞因子释放综合征(1-2级),未报告神经毒性。≥3级不良事件包括淋巴细胞减少(14例[64%])、白细胞减少(10例[45%])和中性粒细胞减少(9例[41%])。
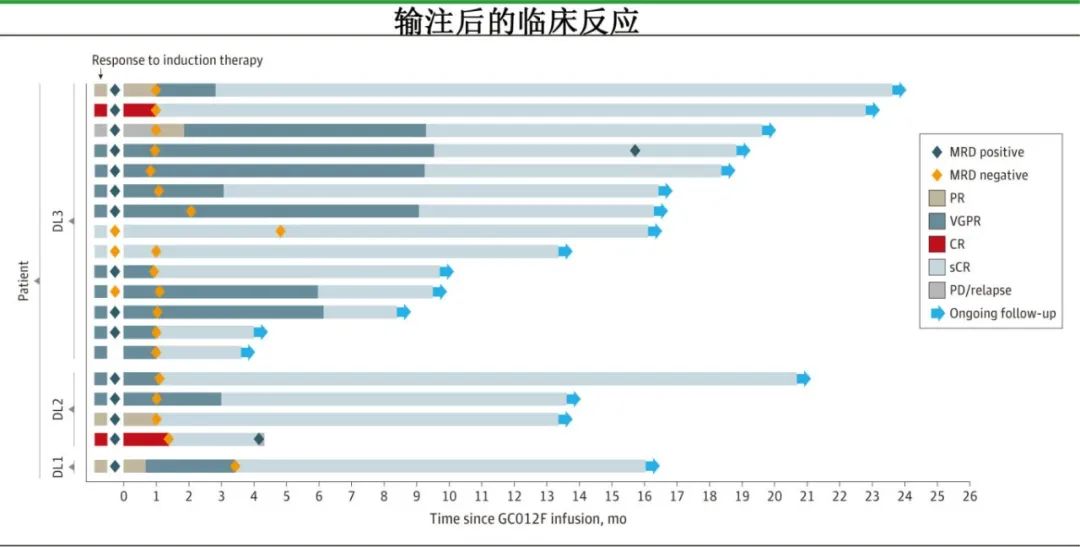
19例患者纳入疗效分析集,总缓解率为100%,所有患者均达到了严格意义上的完全缓解和MRD阴性,且在不同的剂量水平上疗效均一致。GC012F起效较快,至首次达到严格意义上的完全缓解的中位时间为84天(范围26-267天),至MRD阴性的中位时间为28天(范围23-135天)。中位缓解持续时间、无进展生存期和总生存期均未达到。
CAR-T细胞扩增稳健,中位峰值拷贝数(Cmax)为60652拷贝/μg基因组DNA,中位至Cmax的时间为10天,中位持续29天。中位曲线下面积(AUC0-28)为289685,且不同剂量水平间无差异(P=0.77)。Cmax和AUC0-28与CRS无显著相关,但接受治疗的CRS患者的Cmax高于未治疗的CRS患者(137404 vs 30691拷贝/μg基因组DNA;P=0.01)和无CRS组(137404 vs 62131拷贝/μg基因组DNA;P=0.04)。GC012F的扩增与DOR、PFS和OS无显著相关性。
总结
该研究结果在国际上首次证实,将CAR-T治疗的治疗模式前移,不仅因NDMM患者良好的T细胞活力提高了CAR-T制备的成功率,临床疗效显著,优于目前临床常规一线方案,而且安全性高,CRS反应率低。BCMA/CD19双靶点CAR-T细胞疗法在初治高危MM患者具有潜在的临床应用价值和应用前景,期望为治愈骨髓瘤的目标带来新突破。
参考文献
Qiang W, Lu J, Jia Y, et al. B-Cell Maturation Antigen/CD19 Dual-Targeting Immunotherapy in Newly Diagnosed Multiple Myeloma. JAMA Oncol. Published online July 25, 2024. doi:10.1001/jamaoncol.2024.2172
Nature Medicine:利用血浆蛋白质组学提升疾病早期诊断:从多发性骨髓瘤到肺纤维化的精准预测
![]() 0
2024-07-25
点击查看
0
2024-07-25
点击查看

【AJH】多发性骨髓瘤伴CNS受累的大型真实世界研究
![]() 0
2024-07-24
点击查看
0
2024-07-24
点击查看

Blood Cancer J | 多发性骨髓瘤中不同剂量来那度胺耐药性的影响:一项回顾性研究
![]() 0
2024-07-28
点击查看
0
2024-07-28
点击查看

Blood Cancer J: Dara-KRd治疗初诊多发性骨髓瘤:无需移植,深度缓解且持久
![]() 0
2024-07-25
点击查看
0
2024-07-25
点击查看
多发性骨髓瘤蓝皮书重磅发布!近七成医生认为提高治疗方案效果是迫切之需
![]() 0
2024-07-28
点击查看
0
2024-07-28
点击查看
【柳叶刀血液学】多发性骨髓瘤T细胞衔接双特异性抗体的耐药机制及克服策略
![]() 0
2024-07-26
点击查看
0
2024-07-26
点击查看
