辉瑞公司今天宣布,美国FDA已批准其EUCRISA®(crisaborole)软膏的补充新药申请(sNDA),将EUCRISA(Crisaborole)软膏适应症扩展至3个月大的轻中度特应性皮炎患儿。EUCRISA先前已获批准用于成人和2岁及以上的儿童。该补充批准使EUCRISA成为第一个也是唯一适用于3个月大的轻中度AD患儿的局部处方药。
加州大学圣地亚哥分校皮肤科和儿科教授Lawrence Eichenfield博士说:“患者家庭每天需要花费数小时缓解孩子的湿疹症状,这是艰辛的,并且会给整个家庭造成伤害。EUCRISA的批准为这些非常年幼的患者提供了潜在的缓解方法”。
AD是一种慢性皮肤病,其特征在于皮肤发炎和皮肤屏障缺陷,在美国约有1800万人和约11%的儿童受到影响。
原始出处:
https://www.firstwordpharma.com/node/1710324
苏州康乃德生物医药的IL-4Rα单抗CBP-201治疗特应性皮炎,在1b期临床研究中展现出巨大的潜力
![]() 0
2020-01-09
点击查看
0
2020-01-09
点击查看
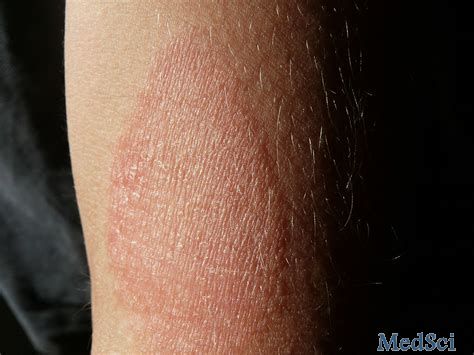
JAK抑制剂baricitinib在III期特应性皮炎研究中显著改善皮肤炎症
![]() 0
2020-01-28
点击查看
0
2020-01-28
点击查看

特应性皮炎的治疗进展:ruxolitinib乳膏制剂效果良好
![]() 0
2020-01-29
点击查看
0
2020-01-29
点击查看
Incyte的JAK1/JAK2抑制剂ruxolitinib乳膏治疗特应性皮炎的第二个III期临床成功
![]() 0
2020-02-20
点击查看
0
2020-02-20
点击查看
III期JADE Compare试验:JAK1抑制剂abrocitinib治疗特应性皮炎取得积极结果
![]() 0
2020-03-19
点击查看
0
2020-03-19
点击查看

Lancet:润肤剂和食物均不能降低婴幼儿特应性皮炎风险
![]() 0
2020-03-21
点击查看
0
2020-03-21
点击查看
