肿瘤是对人类健康有着巨大威胁的遗传病,也是疾病研究领域的重要问题。虽然导致肿瘤的原因多种多样,但是癌基因突变的累积是肿瘤发生的最为重要的原因。单个癌基因的突变激活并不会产生肿瘤,癌基因的激活与抑癌基因信号通路的紊乱相互配合,才会发生恶性转化的过程。
在众多癌基因中,Ras家族是一类编码小GDP结合蛋白的原癌基因。Ras经上游信号激活后,通过信号转导并激活其下游通路,会给细胞带来较强的增殖信号。
而在众多的抑癌基因编码的蛋白质中,p53蛋白一直是研究人员关注的焦点。它是一种压力应激蛋白,也是转录因子。由于p53能够监测细胞内各种压力应激信号,并引起相应的周期阻滞,细胞凋亡等效应,从而维持细胞基因组的稳定性,因而p53蛋白被誉为“基因组卫士”。
在癌症免疫药物研究领域,RAS和p53蛋白是两个一直未能攻克的靶点。一方面,出现在这两个蛋白上的突变在癌症患者中最为常见,RAS和p53蛋白在许多肿瘤中都发生了突变。另一方面,RAS和p53又都是细胞内蛋白,传统的小分子药物很难有效靶向RAS和p53。
近日,在顶尖科学期刊Science和Science Immunology上发布的两项最新研究中,由约翰-霍普金斯大学(Johns Hopkins University)学者领衔的研究团队成功研发出靶向RAS和p53突变体的双特异性抗体疗法。

双特异性抗体是药物研发领域的热点之一,通常的单克隆抗体只能与一个抗原结合,而双特异性抗体能够与两个不同的抗原结合,从而扩展抗体的功能。它们能够识别携带RAS基因突变或者TP53基因突变的肿瘤细胞,并且激发T细胞消灭携带这些突变的肿瘤细胞。
其中一种重要类型被称为T细胞接合器(T cell engager),这种双特异性抗体的一端与肿瘤细胞表面的特异性抗原相结合,另一端与能够激活T细胞受体(通常为CD3)并与之结合,从而将T细胞募集到肿瘤细胞附近,激活它们杀伤肿瘤细胞。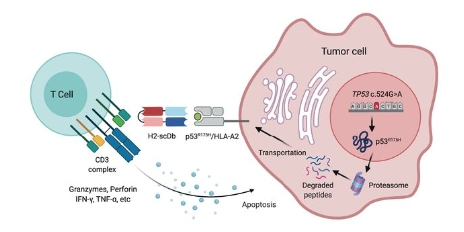
双特异性抗体通过激活T细胞杀死癌细胞的示意图
虽然RAS和p53是细胞内蛋白,但是它们在细胞内被降解后生成的多肽片段能够与人类白细胞抗原(HLA)蛋白构成复合体,并且在细胞表面呈现。
为了靶向突变体RAS和p53蛋白片段,研究人员设计了双特异性抗体。标准抗体具有两个相同的臂,但是双特异性抗体的双臂并不完全相同,其中一臂与T细胞受体激活,另一臂与癌细胞表面蛋白连接,桥接细胞并激活免疫细胞以攻击癌细胞。
该研究的挑战在于肿瘤细胞表面的突变体RAS和p53蛋白片段极为稀缺,仅有10个拷贝。研究团队花费了超过5年的时间发现了一种能够与癌细胞结合但不与健康细胞结合的双特异性抗体。
首先,研究人员构建了一个抗体片段库,以筛选那些能抗原结合的抗体。然后,他们将这些片段转化为不同的双特异性抗体,最终发现一种称为“diabody”的双特异性抗体能够成功激发T细胞的免疫反应。

靶向突变p53-HLA复合体的双特异性抗体H2-scDb在小鼠模型中显著缩小肿瘤体积
研究结果表明,这种双特异性抗体能够显著抑制肿瘤的生长。在研究员Suman Paul领导的第三项研究中,同一类型的缩小双靶抗体在小鼠身上也能对抗一种涉及T细胞的白血病。
诚然,这种疗法在进入临床试验之前还需要进一步优化,由于缺乏抗体的Fc区,它们的稳定性不高,在血液中很容易被清除,导致患者可能需要长时间持续接受输注来维持双特异性抗体的有效治疗浓度。
德克萨斯大学阿灵顿分校的免疫学家乔恩·韦丹兹说:尽管研究人员正在开发其他治疗癌症的药物,但这些药物不能进入免疫系统,而且随着肿瘤的抗药性增强,它们很可能在1年内停止工作。双特异性抗体可以凝聚广泛的免疫反应,具有更大规模的战斗潜力。
总而言之,通过构建能够同时靶向受体和T细胞的双特异性抗体,药物能够有效地到达靶点,在细胞表面表达水平极低的情况下仍然能够激活T细胞反应并消灭癌细胞。
初始来源:
doi:10.1126/science.abh3174
Cell Death Diff:HPV介导HP1γ核转运促进p53降解驱动宫颈癌发生
![]() 0
2020-04-14
点击查看
0
2020-04-14
点击查看

Sci Signal:p53受癌细胞中的有氧糖酵解作用的调控
![]() 0
2020-06-03
点击查看
0
2020-06-03
点击查看

Blood:Vav1突变在成熟T细胞肿瘤发生中的贡献
![]() 0
2020-10-04
点击查看
0
2020-10-04
点击查看
Nat Commun:c-Myc激活泛癌表达的lncRNA MILIP失活p53并诱导癌症的发生
![]() 0
2020-10-16
点击查看
0
2020-10-16
点击查看

Cell Death Differ:TRIM28–RLIM–MDM2–p53通路影响肺癌的发生发展
![]() 0
2020-12-27
点击查看
0
2020-12-27
点击查看

Nat Commun:BRD4介导p53抑制作用是急性髓性白血病的联合治疗靶标
![]() 0
2021-01-18
点击查看
0
2021-01-18
点击查看