病例回顾
患者女性,70岁,因腹胀、腹围增大2月余就诊。
病史:既往有“2型
糖尿病、
高血压”病史多年,30年前因“阑尾炎”行阑尾切除术,15年前因“胆囊结石”行胆囊切除术;8年前因“子宫内膜癌”在外院行子宫及双附件切除术,术后常规化疗,5年内多次常规检查未有阳性发现;否认“肝炎、结核”等传染病史,无烟酒嗜好。
体格检查:血压148/90mmHg,腹部膨隆,见多条手术疤痕,腹壁静脉未见曲张,腹肌软,脐周及上腹压痛阳性,无反跳痛,肝脾肋下未触及,移动性浊音阳性,双下肢无水肿。
入院后完善相关检查:
① 血常规:白细胞:11.23*10^9/L、中性细胞比率:85.8%、血红蛋白:104g/L、血小板:121*10^9/L。
② 血生化:总蛋白:73.5g/L、白蛋白:33.3g/L、球蛋白:40.2g/L、肝脏代谢酶指标、肾功能、电解质均正常。
③ 肿瘤标志物:CA125:299.50U/ml,CA-199:66.1U/mL、AFP+CEA+CA153:均正常。
④ 心电图:1.窦性心律;2.部分T波异常。
⑤ 腹部彩超:肝硬化、脾大、腹水、胆囊缺如。
⑥ 心脏彩超:1.左房扩大;2.升主动脉近端增宽;3.左室舒张功能减低。
确诊过程迷雾层层
对于这样一个腹水待查病例,
诊断上似乎没有悬念:肝硬化并腹水形成。常规予以利尿、控制水和钠盐摄入等对症治疗。
接下来需要明确肝硬化的病因以及腹水的性质。
病毒性肝炎是我国肝硬化的主要病因,占50%~60%,其它病因还有慢性酒精性肝病、非酒精性脂肪性肝病、长期胆汁淤积、自身
免疫性肝炎等。腹水的病因多样,肝硬化门脉高压是腹水形成的主要病因,约占所有腹水成因的85%,而腹水的出现标志着肝硬化患者从代偿期进展到了失代偿期。其它的非肝病病因包括恶性肿瘤(如腹膜转移癌)、腹膜结核、心功能不全、急性
胰腺炎、肾病综合征等。
顺着思路,紧接着又完善了相关检查。
病毒性肝炎标志物:乙肝七项、甲、丙、戊肝抗体均为阴性。
腹水常规:透明度:浑浊,颜色:黄色,李凡他实验:++,白细胞计数2400x10^6/L、L:0.8、N:0.2。
腹水生化:总蛋白:55.9g/L、葡萄糖:1.29mmol/L、乳酸脱氢酶:415IU/L、腺苷脱氨酶测定:24.1U/L。腹水分析提示为渗出液。
因患者既往有多次手术史,还需要行腹部CT检查以进一步评估病情。
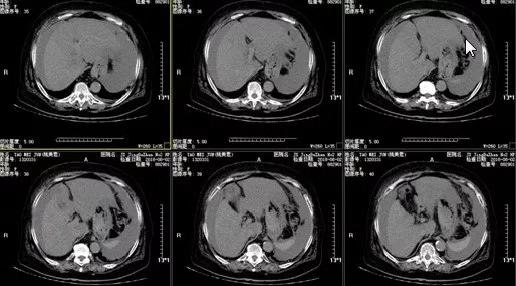
腹部+盆腔CT结果示:
1.肝硬化,脾大,腹水;
2.胆囊未见显示;
3.子宫附件未见显示;
4.大网膜结节样增厚,建议进一步检查除外转移瘤。
此时肝硬化的病因仍不明确,但病情有了重要线索:大网膜结节样增厚使我们联想到了腹膜转移癌。追踪腹水病理,病理科医师口头报告:发现异型细胞,考虑上皮性来源。
腹水的病因呼之欲出,为进一步明确
诊断,建议PET-CT,患者及家属表示同意。
PET-CT结果:子宫内膜癌术后子宫及附件缺如,大小网膜、肠系膜及腹膜、右下腹壁皮下软组织广泛种植转移,双肺内多发转移,全身多区域淋巴结转移;大量腹水。而此时,腹水病理结果也出来了:查见腺癌细胞。
免疫组化结果:CK19(+),PAX-8(+),ER(+),P16(+),Hep1(+),CK20(-),CK7 (-),CDX-2(-),TTF-1(-),Villin(-),Calretinin(-),p53(+++,突变型),Ki-67(约50%+)。
结合病史及免疫组化,考虑浆液性乳头状癌,来源于妇科(子宫)可能性大。
免疫组化,即免疫组织化学检测,是目前肿瘤精准
诊疗的重要检测手段。免疫组化技术发展至今,已经有上百种肿瘤细胞特异性表达抗体的发现和应用。通过不同肿瘤细胞所表达的特异性抗体,病理医生可以更清楚地了解肿瘤细胞的来源、类型、恶性程度及预后等,以确保病理诊断的准确性。
CK19:细胞角蛋白19,上皮性肿瘤标记,单层上皮和间皮标记,常用于腺癌诊断,肝细胞不表达,胆管上皮阳性反应,可鉴别肝癌和胆管癌。
CK20:细胞角蛋白20,
胃肠上皮、移行上皮Merkel细胞来源标记,用于
胃肠道腺癌、卵巢黏液性肿瘤、皮肤Merkel细胞癌诊断,鳞癌、
乳腺癌、
肺癌、子宫内膜/卵巢非黏液性肿瘤、神经内分泌肿瘤常阴性。
CK7:细胞角蛋白7,上皮来源标记,通常在腺癌中表达,腺上皮和移行上皮细胞表达,非上皮来源细胞无表达。在卵巢、乳腺和肺的腺癌呈阳性反应,而胃
肠道的腺癌阴性。
PAX-8:主要表达于甲状腺、肾导管组织、副中肾管组织及相关肿瘤中,对转移性肿瘤的来源有一定的判断意义。对于转移性腺癌,形态符合浆液性癌时,PAX-8可鉴别间皮瘤来源,还是女性
生殖系统来源的浆液性癌,前者阴性,后者阳性,但不能鉴别是卵巢、输卵管、还是子宫来源。
ER:雌激素受体,内分泌细胞标记,肿瘤组织阳性率越高,肿瘤对内分泌治疗越有效,预后越好。
P16:P16蛋白,上皮性肿瘤标记,用于宫颈癌预后判断,阳性表达者预后差。
CDX-2:CDX2是一种肠特异性的核转录因子,是肠上皮形成和分化的关键调节蛋白。在
消化道肿瘤中主要表达在小肠及结直肠,作为肿瘤原发部位的鉴别指标。联合CK7、CK20和CDX2的免疫组化标志物能提高结直肠腺癌诊断的准确性。
Villin:绒毛蛋白,正常分布于肠上皮和肾近曲小管上皮的刷状缘,与CDX-2联合应用,可以明确转移性腺癌的来源,两者均阴性基本排除胃肠道肿瘤来源,两者均阳性,则肿瘤可能起源于胃肠道。
Hep1:肝细胞抗原,标记正常肝细胞和高分化肝癌细胞,低分化肝细胞癌多弱阳性或阴性。
TTF-1:甲状腺转录因子-1,表达于甲状腺腺上皮和肺的上皮细胞,用于大多数肺小细胞癌、腺癌、少部分大细胞癌、大多数非典型神经内分泌肿瘤诊断,而肺鳞癌及绝大多数典型类癌阴性。
Calretinin:钙网素,正常中枢和外周神经组织表达丰富,正常或肿瘤性间皮可有表达,可用于间皮瘤和腺癌(+<5%)的鉴别。
p53:一种抑癌基因,与浆液性乳头状癌的发生和发展有着密切的关系,分为野生型(Wtp53)和突变型(Mtp53)。突变型Mtp53能够被免疫组化测定,突变后则丧失了启动细胞凋亡的能力。突变型p53高表达,提示细胞高度增生、分化程度差、恶性程度高、预后不良。
Ki-67:细胞增殖标志,阳性率越高,提示肿瘤增殖越快、分化差、浸润转移快、预后差,是公认的肿瘤预后指标。
至此,腹水的病因已经明确,但随之问题来了:患者8年前不是已经行子宫及双附件切除术吗?术后多次全腹CT检查均未有阳性发现,而现在免疫组化又提示肿瘤来源于子宫可能性大!患者8年前的术中情况及术后病理究竟是什么情况?难道术前肿瘤已经转移扩散?
带着以上疑问,费了不少周折,终于查阅到了相关资料。患者当时术前CT评估,未发现有腹腔淋巴结肿大及转移灶。
术前诊断:子宫内膜癌。
手术方式:子宫切除术+双附件切除术。
术后巨检:宫腔后壁见一大小约1.5cm*0.5cm结节,大部分突向宫腔,伸入浅肌层(0.5~0.7cm)。
镜检:内膜腺体异常增生,瘤细胞核大深染,见核分裂像,呈乳头状,腺管状结构浸润约1/3肌层。
诊断:
1.子宫内膜癌Ⅰ级,浸润肌层约1/3层深度,周边内膜呈中-重度不典型增生;
2.宫颈阴性;
3.双侧卵巢及输卵管阴性;
4.腹腔血性冲洗液见大量红细胞及少许间质细胞。
由于条件受限,当时并未做免疫组化。我们尝试去借阅当时的病理切片,因种种原因,最终还是无功而返。
根据以上描述,可以看出当时术前肿瘤转移可能性小。但现在腹水病理及免疫组化又提示浆液性乳头状腺癌,结合既往病史,考虑来源于子宫可能性大。而子宫内膜浆液性乳头状癌属于Ⅱ型子宫内膜癌,
临床上较为少见,其恶性程度高,早期即有深肌层浸润、宫旁播散、脉管间隙浸润以及淋巴转移的倾向,即使无明显肌层浸润也有可能发生腹腔播散。
由此我们可以推测,尽管术前和术后患者评估情况较好,但其实发现肿瘤时,癌细胞已经离开了宫腔,发生了腹腔播散。
紧接着问题又来了:子宫内膜浆液性乳头状癌侵袭性强,预后差,其复发转移多集中于术后5年内;而该患者术后5年常规随访未有特殊不适及阳性发现,直至8年后才以腹水为主要表现,出现腹腔广泛种植转移,双肺及全身多区域淋巴结转移。
为什么癌细胞沉默8年之久又开始快速分裂增殖,形成新的肿瘤?
肿瘤细胞睡着了?
或许,肿瘤休眠可以很好地解释这一现象。
肿瘤休眠是指肿瘤细胞在人体内长期存在而没有明显生长的一种状态。早在20世纪40年代,Wilis等人研究发现了肿瘤休眠现象并命名;后来,Hadfield 等人再次进行了较为详细的描述。
这两篇文献都源于在研究中观察到肿瘤细胞有丝分裂周期停滞和细胞增殖抑制。另有学者将这一现象描述为细胞沉默,沉默即非增殖状态,是一种稳定状态。
临床上,对于复发率很高的肿瘤,如乳腺癌、前列腺癌和
胰腺癌等,研究人员发现,无论是手术切除,还是化疗放疗,这些癌症依然有转移复发的风险,所以关键的问题是,这些癌细胞究竟来自何方?
休眠细胞的长期存在被认为是癌症卷土重来的根源。越来越多的研究表明,休眠细胞在其发育早期即脱离了母体肿瘤,并分散到达体内新的部位。但是,在进入其它组织或器官之后,这些细胞将处于休眠状态,它们可以逃过人体免疫细胞及靶向治疗药物或常规抗肿瘤药物的“追杀”,患者可无任何临床症状和不表达可检测到的肿瘤分子标记 。一旦身体的某种平衡状态被打破,在周围微环境适宜的条件下 ,休眠细胞就会被唤醒激活,开始活跃地分裂,肿瘤就会复发转移。
2016年,美国西奈山伊坎医学院和德国Regensburg大学在Nature在线发表的两篇论文揭示:即使在原发性肿瘤形成之前,具有某些分子改变的乳腺癌细胞即可扩散到其他器官,先长时间保持休眠,然后被唤醒导致肿瘤转移。
近年来,临床肿瘤治疗的方法主要包括手术治疗、针对处于增殖状态的肿瘤细胞的放疗和化疗,并且取得了一定的效果。但是处于休眠状态的分散的肿瘤细胞如果被唤醒激活,将促进肿瘤复发,加速肿瘤患者结局恶化。
随着肿瘤休眠机制深入地研究,研究人员开始转变观念:靶向分散在体内的恶性休眠细胞,通过调节肿瘤细胞中的某些信号途径、恢复机体被破坏的免疫系统或抑制肿瘤
血管生成使休眠细胞维持休眠状态,或者在休眠状态下将其消灭,这将成为肿瘤治疗的新策略,但其具体机制仍需进一步研究。
每一个患者的病情都有值得学习的地方,本例腹水待查的病例引发了我们对肿瘤细胞休眠的思考。有时去诊治,常常去思考,总是去归纳,临床医生唯有从平常的工作中不断地去归纳总结,才能提升自己的临床思维层次,提高自己的临床决策能力。
来源:医学界消化肝病频道
版权声明:
本网站所有注明“来源:梅斯医学”或“来源:MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有,非经授权,任何媒体、网站或个人不得转载,授权转载时须注明“来源:梅斯医学”。本网所有转载文章系出于传递更多信息之目的,且明确注明来源和作者,不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。同时转载内容不代表本站立场。
在此留言