FAT1基因突变在多种人类癌症中被频繁检测到, 特别是在鳞状细胞癌(SCCs)中。FAT1的突变一直与不良的临床结果和治疗抗性相关。在由化学致癌物7,12-二甲基苯并[a]-蒽(DMBA)与12-O-十四碳酰抗坏血酸-13-乙酸(TPA)(以下简称DMBA/TPA)组合诱导的皮肤SCCs中,Fat1在约20%的情况下发生突变,这和在人类SCCs中的情况类似。

FAT1基因编码的是一个原粘连蛋白,目前,我们对于FAT1突变控制肿瘤的发生和发展的作用和分子机制还不太了解。最近,研究人员在Nature杂志发文,其使用皮肤鳞状细胞癌和肺部肿瘤的小鼠模型,发现Fat1的缺失会加速肿瘤的发生和恶性进展,并促进上皮到间质的混合转变(EMT)表型。
研究人员还在FAT1突变的人鳞状细胞癌中发现了这种混合EMT状态。Fat1被删除的皮肤鳞状细胞癌呈现出肿瘤干性和自发性转移的增加。
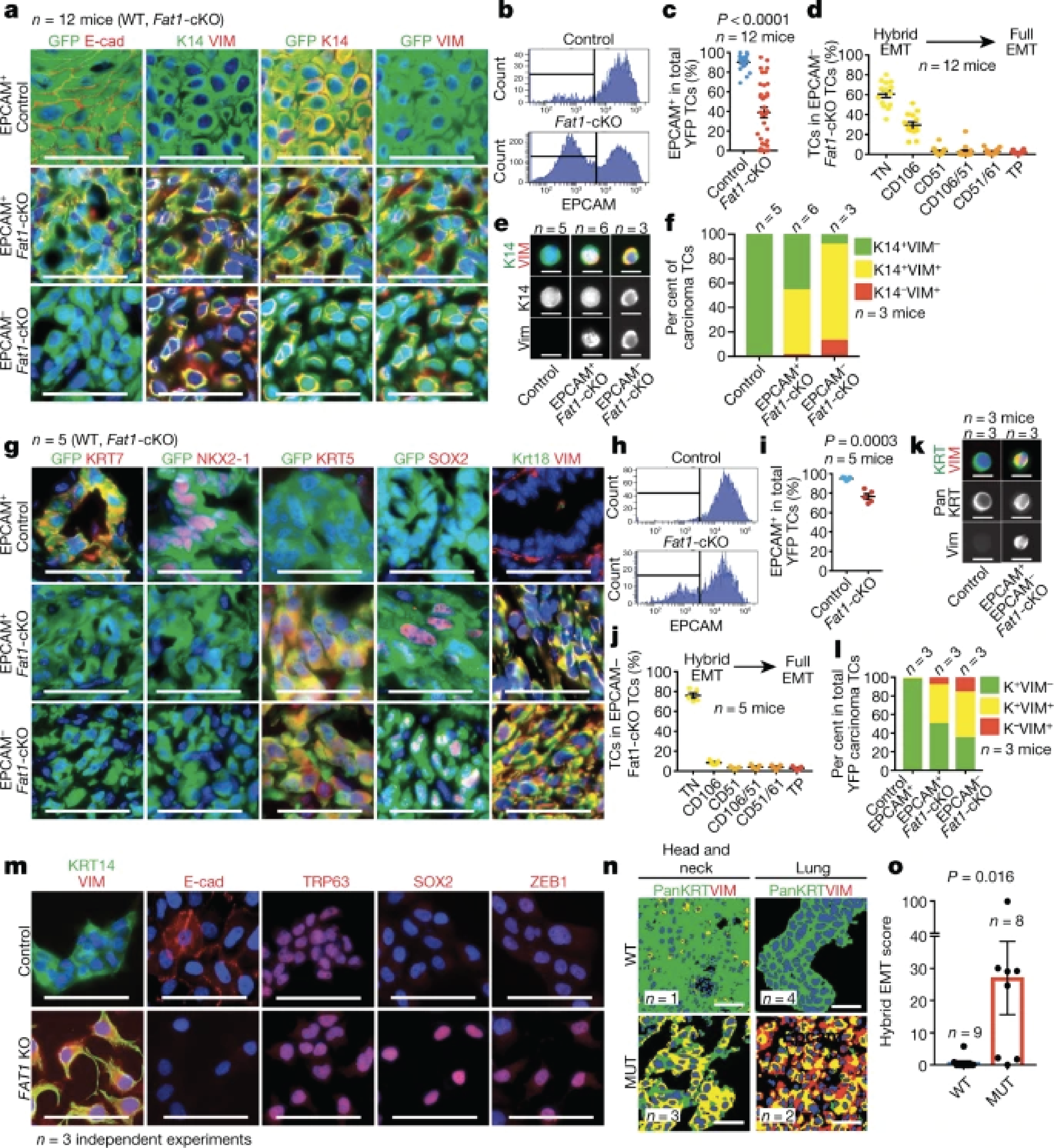
研究人员进一步进行了转录和染色质谱分析,结合蛋白质组分析和机理研究,发现FAT1功能的丧失激活了CAMK2-CD44-SRC轴,促进了YAP1核转位和ZEB1的表达,刺激了间质状态。这种功能的丧失也会使EZH2失活,促进SOX2的表达,从而维持上皮状态。
因此,该研究综合分析发现了FAT1缺失肿瘤的耐药性和脆弱性,这对癌症治疗有重要意义。该研究揭示,在小鼠和人类鳞状细胞癌中,FAT1功能的丧失通过诱导混合EMT状态促进肿瘤的发生、进展、侵袭性、干性和转移。
原始出处:
Ievgenia Pastushenko et al. Fat1 deletion promotes hybrid EMT state, tumour stemness and metastasis. NATURE (2020).