瑞士生物技术公司Anokion SA近日宣布,美国食品药品监督管理局(FDA)已批准抗原特异性药物ANK-700治疗多发性硬化症(MS)的IND申请。Anokion计划在今年年底之前启动针对MS患者的多中心I期临床试验。

Anokion首席医学官Simon Cooper表示:“多发性硬化症仍然是一种毁灭性疾病。不幸的是,可用的干预措施的获益十分有限,而且往往无法解决导致疾病恶化的潜在机制。通过利用肝脏中的天然免疫耐受途径,ANK-700旨在通过一种潜在的转化方法对免疫系统进行重新整合”。
在临床前模型中,Anokion已证明其有效的肝靶向技术诱导的耐受性T细胞机制可有效预防或减少MS的病理反应。在MS的小鼠模型中,靶向肝脏的髓磷脂少突胶质细胞糖蛋白(MOG)抗原诱导致病性T细胞无反应和缺失,从而在活动性疾病中被耐受时,可以保护免受疾病发作的影响。
原始出处:
https://www.firstwordpharma.com/node/1760213?tsid=4
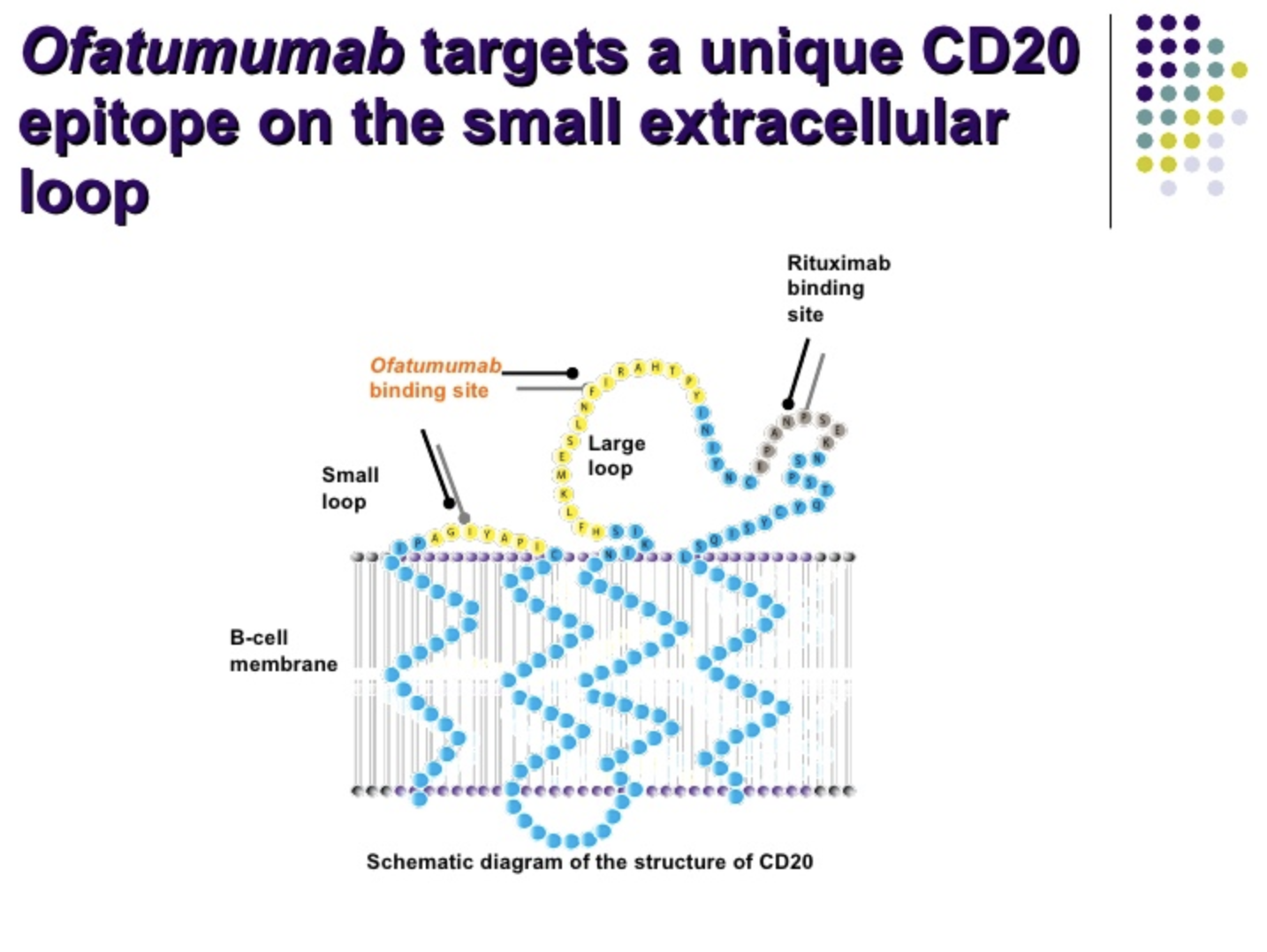
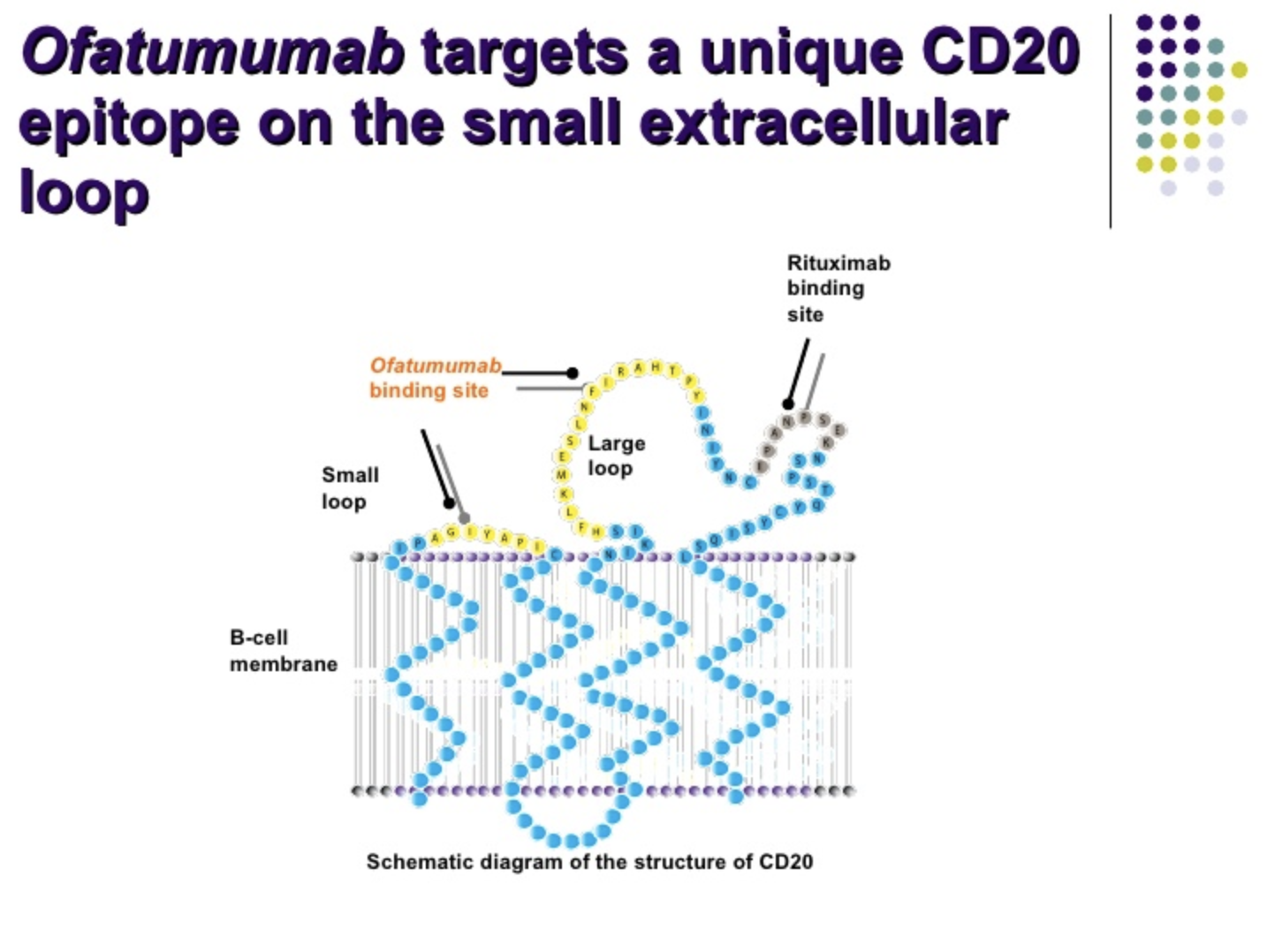
NEJM:诺华每月注射一次的奥法木单抗ofatumumab在多发性硬化症患者中展现优越疗效
![]() 0
2020-08-06
点击查看
0
2020-08-06
点击查看
JAMA Neurol:继发性进行性多发性硬化症患者持续接受免疫治疗可降低残疾进展风险
![]() 0
2020-08-10
点击查看
0
2020-08-10
点击查看
Acta Neurol Scand:多发性硬化症患者补充维生素D3是否会增加其疾病的复发风险?
![]() 0
2020-08-16
点击查看
0
2020-08-16
点击查看

FDA批准也是**一个多发性硬化症患者自行注射的B细胞疗法Kesimpta(ofatumumab),只需每月注射一次
![]() 0
2020-08-21
点击查看
0
2020-08-21
点击查看
NATURE:肠道微生物可以加剧多发性硬化症
![]() 0
2020-08-27
点击查看
0
2020-08-27
点击查看

EBV特异性T细胞免疫疗法ATA188治疗多发性硬化症:所有剂量组均取得积极结果
![]() 0
2020-09-11
点击查看
0
2020-09-11
点击查看
