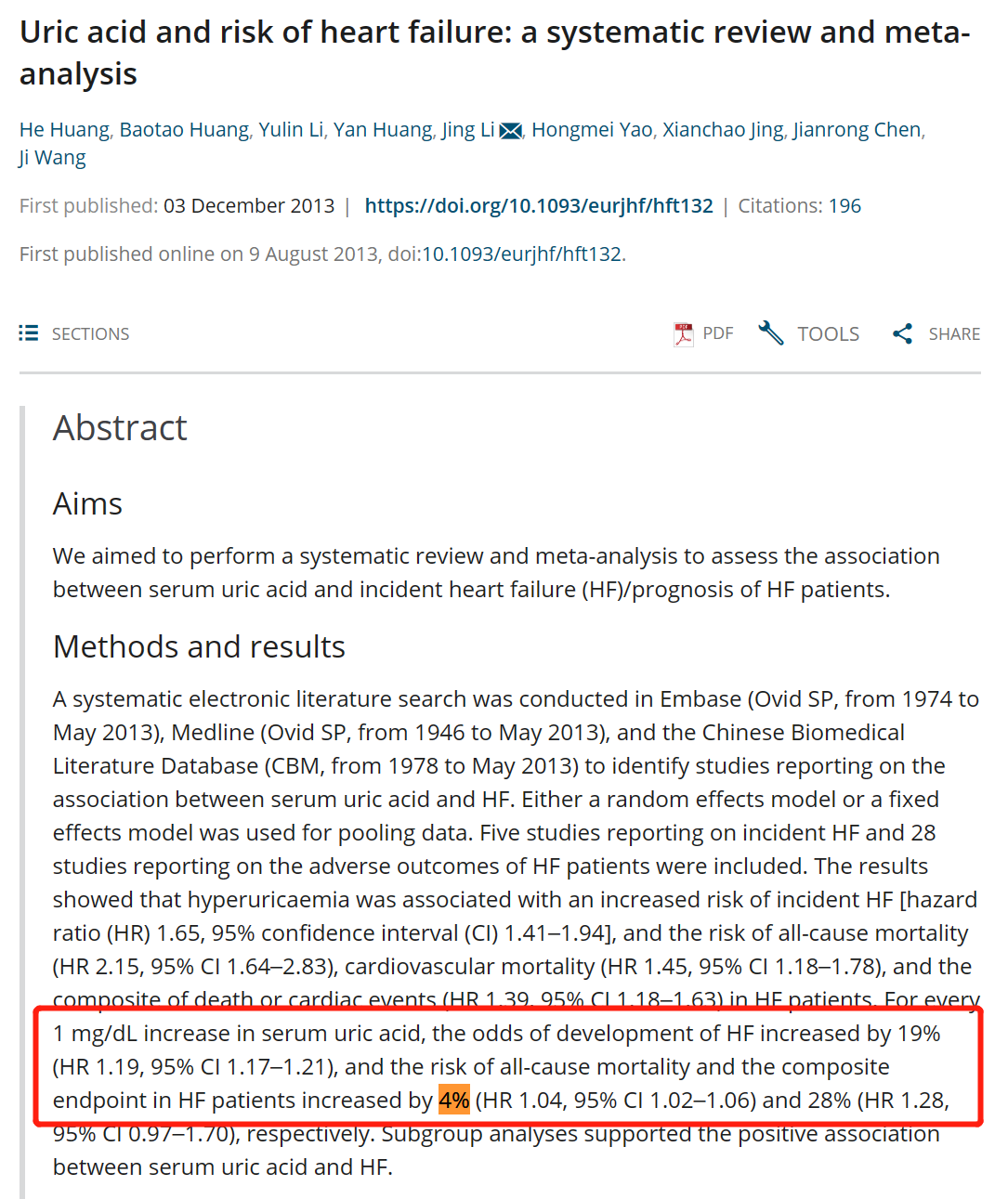
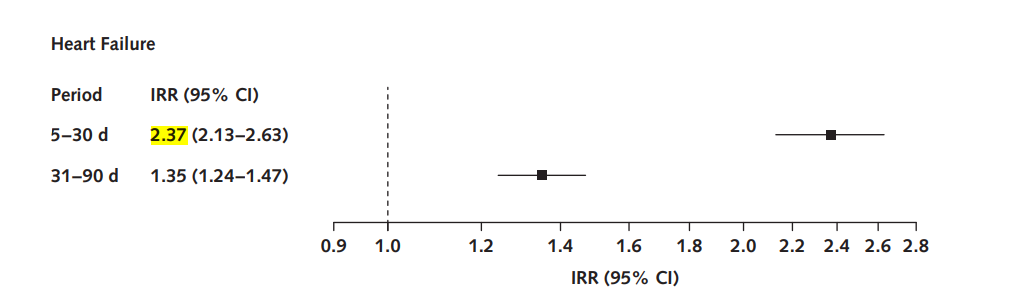
痛风是由于嘌呤代谢紊乱使血液中过多的尿酸析出,导致单钠尿酸盐结晶并沉积在关节部位所致的炎症反应。主要的临床表现为反复发作性关节红、肿、热、痛及关节的功能障碍,尿酸盐结晶可沉积在关节及周围软组织导致痛风石形成慢性关节炎,甚至出现关节畸形、残疾。痛风不仅给患者带来巨大的痛苦,也给家庭及社会带来极大的经济负担。 急性痛风治疗的抗炎镇痛药物主要包括秋水仙碱、非甾体抗炎药(NSAIDs)、激素、IL-1 拮抗剂等。欧洲抗风湿病联盟(EULAR)和美国风湿病学会(ACR)的痛风指南将小剂量秋水仙碱、NSAIDs 和激素列为一线治疗药物。但我国指南为了防止激素滥用的情况,以及反复使用激素药物导致痛风石溃烂风险的增加,将激素药列为二线治疗药物。当存在一线药物治疗禁忌或难治性痛风时,可使用 IL-1 拮抗剂治疗。 高尿酸血症和(或)痛风患者常伴随心血管疾病。研究显示,痛风患者中约有 74%的患者合并高血压,14%的患者存在心肌梗死病史。心血管疾病相关的治疗药物极大地限制了急性痛风治疗药物的选择,今天小编给大家盘点一下,心血管疾病患者痛风发生的危险因素和急性期抗炎治疗方案。 高血压会导致肾小球动脉硬化、肾血管阻力增加、肾功能受损,尿酸的排泄会慢慢减少,随之而来的是血尿酸水平逐渐升高,大幅增加痛风发作风险。同时高血压患者服用的降压药物对血尿酸水平及痛风发作都有影响。 一项大型巢式对照研究纳入了近一万三千人,结果显示,接受β受体阻滞剂、血管紧张素转换酶抑制剂、血管紧张素受体拮抗剂(氯沙坦除外)治疗组的痛风风险分别是对照组的 1.48 倍、1.24 倍和1.29倍(下图),而接受钙离子拮抗剂和氯沙坦治疗的高血压患者,痛风风险降低 13%和19%(下图)。 心力衰竭 心力衰竭患者体内黄嘌呤氧化酶活性增强,尿酸合成增 加,血尿酸水平升高。与此同时,心力衰竭伴随的肾功能受损可减少尿酸排泄,升高血尿酸水平。血尿酸每增加1mg/dl,心力衰竭患者全因死亡率增加 4%。 与缬沙坦相比,沙库巴曲缬沙坦降低血尿酸0.38mg/dl,并将启动降尿酸治疗的概率降低32%; SGLT2抑制剂减少尿酸重吸收,增加尿酸排泄,降低血尿酸水平; 新型心力衰竭治疗药物维利西呱治疗12周后血尿酸水平明显下降,且尿酸的下降程度与维利西呱药物剂量正相关; 保钾利尿剂不增加痛风风险; 而袢利尿剂和噻嗪类利尿剂发生痛风的相对危险度分别为2.64和1.70,两者同时使用发生痛风的相对危险度高达4.65。 那么,心血管患者在急性痛风发作时如何选用治疗药物呢? 秋水仙碱 秋水仙碱是急性心包炎的一线治疗用药,能改善症状,减少复发。它会干扰微管蛋白的组装和聚合,阻止NLRP-3等炎症小体激活、中性粒细胞等炎症细胞趋化、IL-1β等细胞因子生成,进而减少急性痛风的炎症反应 。该炎症通路和心血管炎症相似,提示秋水仙碱对心血管系统发挥抗炎作用。 随机对照试验 LoDoCo 和 LoDoCo2 研究显示,在稳定型冠心病患者中随机使用低剂量秋水仙碱(0.5mg/d)和安慰剂,平均随访至少2年,秋水仙碱组发生心肌梗死、缺血性卒中、心血管死亡等主要心血管终点事件风险显著低于安慰剂组。鉴于秋水仙碱为心血管疾病患者带来获益,急性痛风合并心血管疾病患者可考虑使用秋水仙碱治疗。 韩国的一项队列研究对 10 万余例心肌梗死患者随访2.3年发现,NSAIDs增加心血管事件风险近7倍(HR= 6.96,95%CI:6.24~6.77,P<0.001)。 真实世界研究表明,NSAIDs 的心血管风险在药物使用 1 周内即可发生,1 个月内风险最高,风险与药物使用剂量正相关 。因此,急性痛风的心血管病患者应避免使用 NSAIDs。 一项大型队列研究纳入262万例因皮肤疾病或呼吸道疾病短时间(小于14d)使用激素的患者,中位治疗剂量10mg/d,中位治疗时间3d,结果显示在接受治疗 1 个月内不良反应发生率最高,心力衰竭风险增加(RR=2.37,95%CI:2.13~2.63)。 但中短期使用激素(中位剂量50mg/d,治疗时间小于2周)未造成液体潴留,且能降低血尿酸和肌酐水平,改善肾功能,增加尿量。因此,建议急性痛风合并心血管病患者慎用激素,不推荐血栓或缺血事件高危的患者使用激素治疗。 IL-1β 是急性痛风和心血管炎症通路上共同的关键细胞因子,目前常见两种 IL-1 拮抗剂:卡那单抗和阿那白滞素。 卡那单抗显著降低急性痛风发作风险约 50%,提示卡那单抗是痛风和心血管病共病患者的治疗选择;同时,也有不少研究验证了阿那白滞素的安全性。 虽然生物制剂可能带来继发感染的风险,且药物价格成本高,但 IL-1 拮抗剂通过靶向炎症通路治疗急性痛风合并冠心病、心力衰竭、复发性心包炎、心肌炎等心血管疾病的有益作用不容小觑。 参考文献 [1] 朱丹,董曾荣,杨奕,等. 急性痛风炎症的自发缓解机制. 中华风湿病学杂志,2021,25(05):346-350. DOI:10.3760/cma.j.cn141217-20200408-00145 [2] 韩晶晶,陈夏欢,刘梅林. 心血管疾病患者急性痛风的治疗选择. 中国心血管杂志,2022,27(01):75-79. DOI:10.3969/j.issn.1007-5410.2022.01.014 [3] Kang DO, An H, Park GU, et al. Cardiovascular and Bleeding Risks Associated With Nonsteroidal Anti-Inflammatory Drugs After Myocardial Infarction. J Am Coll Cardiol. 2020;76(5):518-529. doi:10.1016/j.jacc.2020.06.017 [4] Nidorf SM, Eikelboom JW, Budgeon CA, Thompson PL. Low-dose colchicine for secondary prevention of cardiovascular disease. J Am Coll Cardiol. 2013;61(4):404-410. doi:10.1016/j.jacc.2012.10.027 [5] Huang H, Huang B, Li Y, et al. Uric acid and risk of heart failure: a systematic review and meta-analysis. Eur J Heart Fail. 2014;16(1):15-24. doi:10.1093/eurjhf/hft132 [6] Yao TC, Huang YW, Chang SM, Tsai SY, Wu AC, Tsai HJ. Association Between Oral Corticosteroid Bursts and Severe Adverse Events : A Nationwide Population-Based Cohort Study. Ann Intern Med. 2020;173(5):325-330. doi:10.7326/M20-0432 [7] Waljee AK, Rogers MA, Lin P, et al. Short term use of oral corticosteroids and related harms among adults in the United States: population based cohort study. BMJ. 2017;357:j1415. Published 2017 Apr 12. doi:10.1136/bmj.j1415 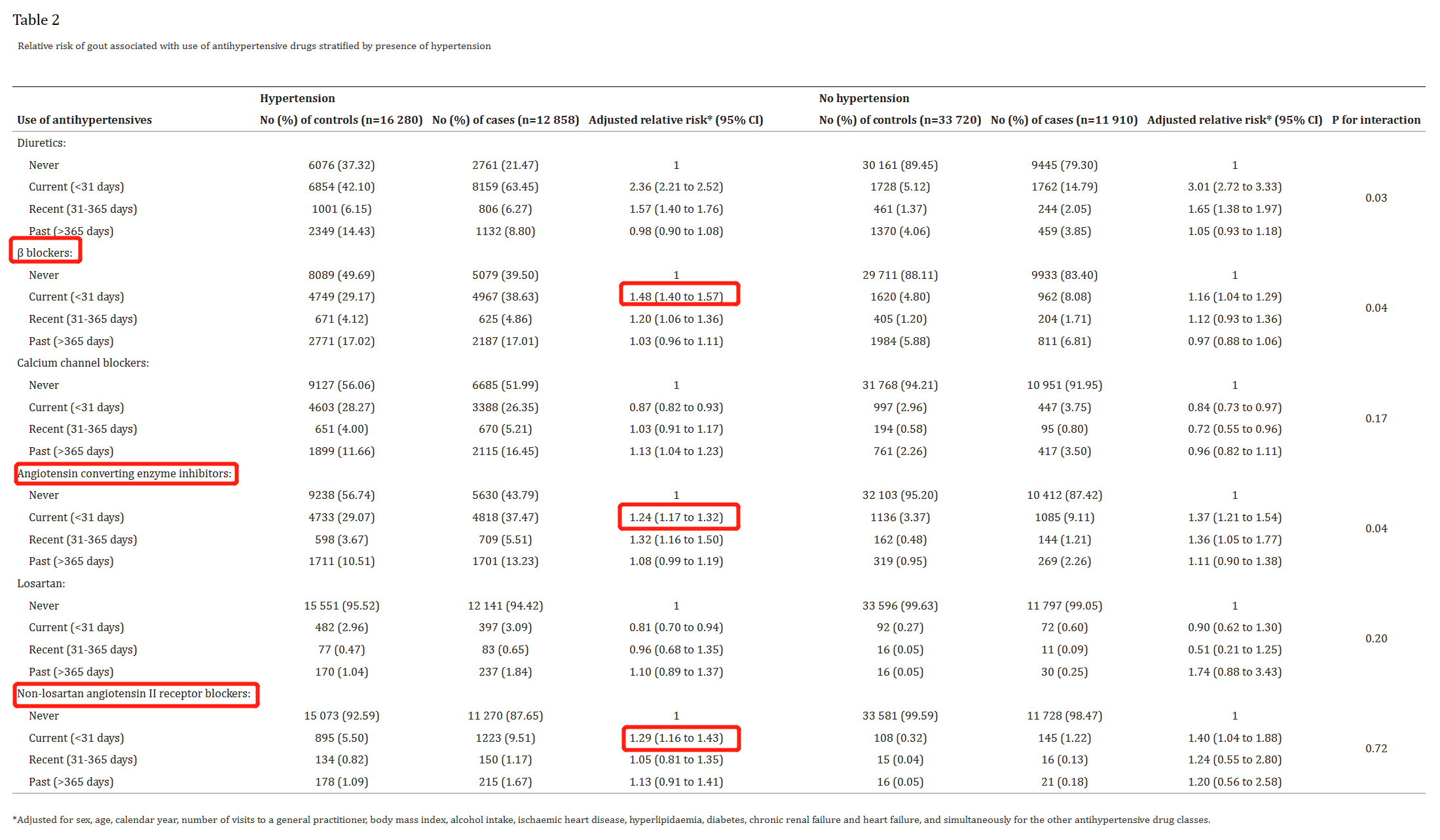



GRK2 在血管平滑肌中的过度表达导致不适当的高血压和急性心力衰竭
![]() 0
2023-05-15
点击查看
0
2023-05-15
点击查看
任务转移高血压和糖尿病筛查和转诊的原则:一项探索农村地区患者、社区卫生工作者和卫生保健专业人员看法的定性研究
![]() 0
2023-05-15
点击查看
0
2023-05-15
点击查看
心脏生物标志物在高血压急症诊断中的作用
![]() 0
2023-05-15
点击查看
0
2023-05-15
点击查看
Hypertension:强化降压可改善老年高血压患者左心室肥厚
![]() 0
2023-06-02
点击查看
0
2023-06-02
点击查看

顶尖学者一线领航,聚焦高血压治疗综合管理的个体化策略及病例分享
![]() 0
2023-06-06
点击查看
0
2023-06-06
点击查看

Hypertension:绝经妇女雌激素治疗给药途径和配方与高血压风险之间的关系
![]() 0
2023-06-10
点击查看
0
2023-06-10
点击查看
