病例介绍
患者男,23岁大学生,主诉发热伴咳嗽咳痰1月余。
2018年3月底:
患者出现发热,体温最高39℃,伴咳嗽咳痰,少许黄粘痰,有盗汗,略纳差乏力,无咯血;有肌肉胀痛,无咽痛,无鼻塞流涕,当地医院查胸片提示双下肺多发感染,阿莫西林抗感染1周后症状无好转。
4月2日至省级医院就诊:
胸部CT:双肺多发磨玻璃影及斑片影,双下肺显著,双侧腋下多发小淋巴结;
血常规:白细胞(WBC)正常,L:0.86×109/L,L% 15.22%,N% 79.41%;
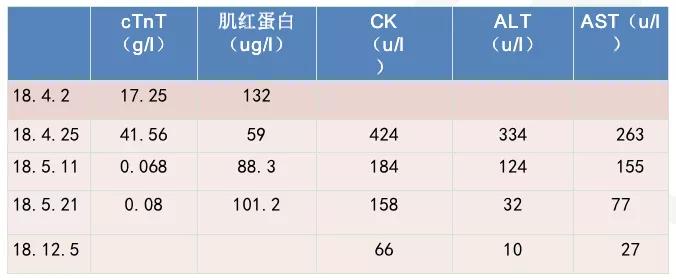
心肌标志物:肌钙蛋白(cTnT):17.25 ng/L,肌红蛋白:132 ug/L;
肿瘤标志物:CEA:5.76 ng/ml,CYFRA21-1:6.08 ng/ml,NSE:21.63 ng/ml;
Tspot:阳性;G试验、GM试验、隐球菌未见异常。
支气管镜检查:各支气管腔通畅,粘膜充血水肿,见较多白色分泌物,余未见异常。
支气管镜检查冲洗液:行细菌、真菌、结核菌检查均阴性。
住院期间外院具体诊断不详,予以甲强龙静滴(具体用法不详),患者体温正常后出院,并予强的松30 mg qd治疗。
4月15日患者再次出现发热,伴肌肉疼痛加重,仍有少许咳嗽咳痰,乏力较前加重,遂再次前往省级医院就诊:
血常规:WBC正常,L:0.57×109/L,L% 8.2%,N% 88.8%;
心肌标志物:cTnT:41.56 ng/L,肌红蛋白:59 ug/L;
抗核抗体(ANA)、抗可溶性抗原(ENA)、抗中性粒细胞抗体(ANCA):阴性;
尿常规:尿蛋白+/-;
生化:谷丙转氨酶(ALT):335.6 U/L,谷草转氨酶(AST):263.4 U/L,乳酸脱氢酶(LDH):630 U/L,肌酸激酶:424 U/L。
予以甲强龙40 mg抗炎,并保肝治疗后,患者仍有间断发热,遂于5月11日来我院就诊。
入院时查体:
T 37.1℃,SO2 97%(不吸氧),神清,精神萎,气平,皮肤粘膜无黄染,脸部及胸前、上肢见散在红色皮疹,全身浅表淋巴结无肿大,双肺叩诊清音,听诊双肺呼吸音粗,双下肺少许湿罗音,未闻及干啰音。
问题1:综合患者的病史特点,可以考虑哪些疾病可能?
1. 感染性疾病:病毒、真菌、结核/非结核分枝杆菌病(NTM);
针对以上考虑的疾病可能,在入院后对患者进行了更加全面的检查:
出凝血功能 :活化部分凝血活酶时间(APTT) 32.1秒;D-二聚体 2.93 mg/L。
血沉:24 mm/H;高敏C反应蛋白(H-CRP):6.5 mg/L;降钙素原(PCT): 0.18 ng/ml。
血常规:WBC 4.85X10^9/L;Hb123 g/L;N% 82.5%;L% 12.8%;E% 0.6%。
特定蛋白:免疫球蛋白M 7.30 g/L;补体C3 0.77 g/L。
生化:蛋白电泳Alb 54.3%;蛋白电泳α1 5.6%;蛋白电泳γ 21.6%;ALT 124 U/L;AST 155 U/L;γ-GT 143 U/L;LDH 566 U/L;前白蛋白<0.08 g/L;葡萄糖 7.2;钙 2.13 mmol/L;CK 184 U/L,肾功能正常。
肿瘤标志物:CEA 13.8 ng/mL;Cyfra21-1 3.7 ng/mL;NSE 23.3 ng/mL;SCC 0.7 ng/ml。
细胞免疫:T淋巴细胞CD3 84.8%;自然杀伤细胞(CD56+16)3.1%;余正常。
心脏标志物:心肌肌钙蛋白T 0.068 ng/ml(<0.03 ng/ml);肌红蛋白 88.3 ng/ml(28-72ng/ml)。
T-spot,G试验,隐球菌夹馍抗原、呼九联、CMV:均阴性。
自免肝相关抗体:抗可溶性肝/肝胰抗原抗体:(-);抗肝溶质抗原I型抗体:(-);抗肝肾微粒体I型抗体:(-);抗线粒体M2亚型抗体:(-)。
自身抗体:抗核抗体:颗粒 1:100 ,其余结果均阴性。
获得性免疫缺陷综合症(HIV)、快速血浆反应素试验(RPR)、丙型肝炎病毒(HCV) : 均为阴性。
胸部CT:两肺上叶也可见磨玻璃影及斑片影,但还是以下肺为主。

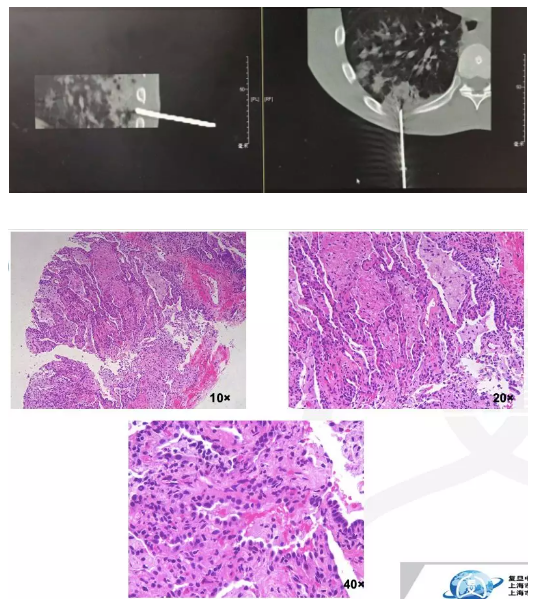
右下肺穿刺:送检肺泡组织,肺泡上皮轻度增生,肺泡间隔少量淋巴细胞浸润,肺泡腔内大量泡沫样组织细胞沉着及纤维素性渗出物,考虑炎性病变。
肺组织送细菌、真菌、结核菌培养均阴性。
问题2:病例介绍到这里,您认为诊断是什么?
1. 结核
2. 病毒
3. 药物热
4. 自身免疫疾病
结核较少引起肌肉损伤,影像学特点不典型,并且复查T-spot为阴性,所以结核可能性小;整个疾病病程较长,且病毒检测均为阴性,所以病毒感染也可以排除;患者发热规律不符合药物热的可能,因为停药后体温并无下降,且皮疹无消退。
那么会是自身免疫疾病么?虽然患者存在多系统损伤,但是激素治疗的效果差,且自身抗体阴性。
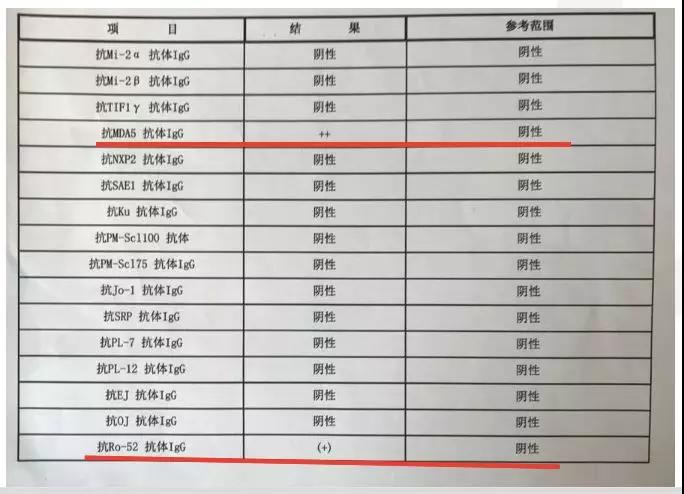
不过我们注意到患者的身上有典型皮疹:眼眶周围皮疹,上胸、颈后背、掌指关节、指间关节伸侧皮疹。另外,患者的肌肉疼痛与体温无关,检查发现肌酸激酶明显升高,抗体检查结果显示MDA-5抗体、Ro-52抗体阳性。
问题3:MDA-5抗体阳性有什么意义?
MDA-5抗体与皮肌炎相关,且可以作为无肌病皮肌炎临床诊断的生物标记物。对于皮肌炎总体死亡率来说,MDA-5阳性与不良预后相关。
MDA-5抗体阳性的患者发生间质性肺疾病(ILD)的风险也更高,包括高死亡率的快速进展性ILD。因此,临床医生必须识别患者的皮肤表现,才能密切监测患者的肺部状态,尤其是不能进行普遍的自身抗体检测时。
所以最终诊断:皮肌炎。
问题4:什么是皮肌炎?
皮肌炎(Dermatomysitis, DM)是横纹肌非化脓性炎症性肌病,是皮肤和肌肉的弥漫性炎症性疾病,为系统性自身免疫病之一。其临床特点是四肢近端、肩周、颈周、髋周肌群进行性无力。
皮肤炎的病理特征包括以下几点:
皮肤可出现液化和空泡变性;
肌肉束间隔及血管周围炎:以B细胞及CD4+T淋巴细胞浸润为主;
毛细血管床减少:纤维蛋白血栓和毛细血管闭塞密度减低、剩余的扩张;
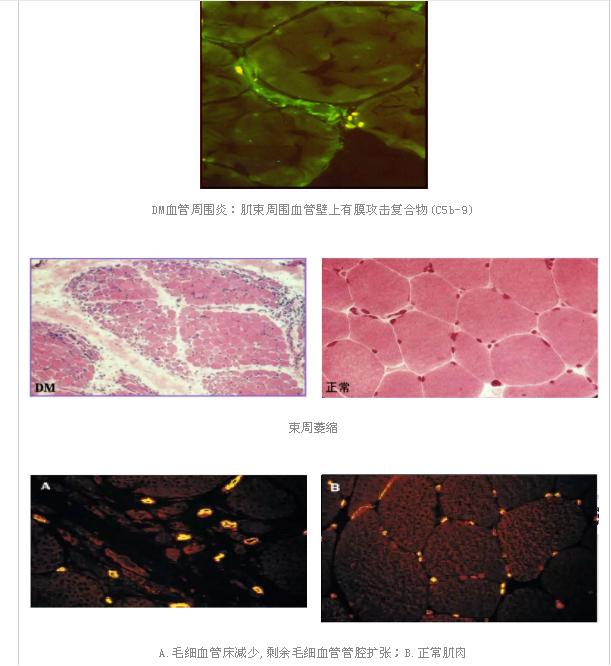
A.毛细血管床减少,剩余毛细血管管腔扩张;B.正常肌肉
皮肌炎的临床表现主要体现在以下几点:
肌肉病变:对称性四肢近端肌肉,肌无力以近端明显。晚期可出现肌萎缩;50%患者肌肉有压痛;罕见暴发型表现为横纹肌溶解,肌红蛋白尿,肾功能衰竭。
呼吸系统:呼吸肌受累,表现为呼吸困难、吸入肺炎肺泡炎和肺间质病变;胸膜炎及胸水罕见。
典型皮疹:Gottron皮疹;向阳皮疹;V区皮疹;披肩征。
其他:技工手;钙质沉着;皮肤异色症;“手枪套征” (Holster sign) 。
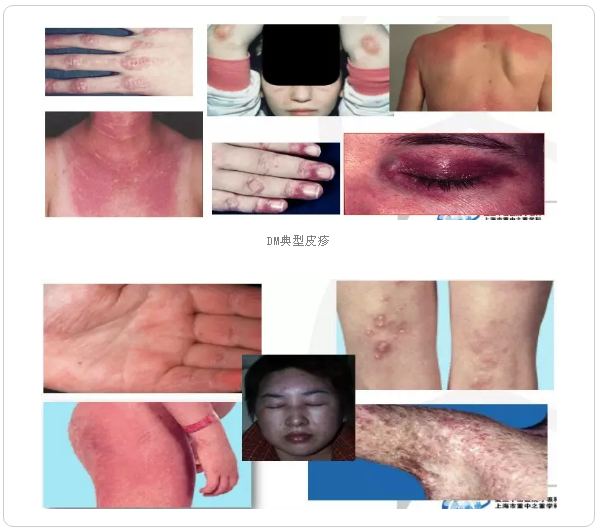
DM典型皮疹
皮肌炎的发现95%-99%伴有肌肉来源的酶活性上升,如CK、AST、ALT、LDH、醛缩酶(ALD)。同时肌电图提示肌源性损害,典型表现低波幅,短程多棘波,敏感性高但特异性差。
另外肌炎特异性抗体阳性,也提示皮肌炎可能,主要包括以下几种:
抗Mi-2抗体:抗原220~240kDa核蛋白复合物,阳性率5~20%,多见于典型DM(特异抗体),提示病情轻,不易合并肿瘤,多有“V”形区和甲周红斑,对激素反应好,5年存活率90%。
抗155/140和抗CADM-140:为DM特异性抗体,前者与恶性肿瘤有关,后者与临床无肌病性皮肌炎和快速发展的间质性肺炎相关。
其他:ANA、RF、抗scl-70、抗SS-A、抗SS-B、抗PM-Scl、抗Ku、抗肌肉成分的抗体:肌红蛋白、肌球蛋白、肌钙蛋白、原肌球蛋白等,但均不特异。
问题5:如何诊断皮肌炎?
这里主要介绍1975年Bohan&Peter诊断标准:
1. 对称性肢带肌和颈前屈肌无力;
2. 肌活检有肌炎的证据;
3. 血清肌酶升高,尤其是肌酸激酶;
4. 典型的肌炎肌电图表现;
5. 皮肌炎的典型皮疹:淡紫色眶周水肿性红斑;Gottron’s 丘疹。
符合所有1-4条即可确诊为多发性肌炎(PM);符合第5条及1-4中的任意3条即可确诊DM。
问题6:如何治疗皮肌炎?
一般性治疗:
首选糖皮质激素治疗:泼尼松1-2 mg/(kg.d);严重者200 mg以上。如何合并ILD,可大剂量甲强龙 0.5-1g/d冲3 d,待病情(肌力和CK)控制后逐渐减量,注意个体化。
用药到病情最大程度改善约需1-6个月,一般2-3个月减至pred 0.1 mg/(kg.d)后仍需维持数月或数年,疗程一般不应少于2年。
注意:激素可引起肌病(CK不高),应与肌炎复发鉴别。
免疫抑制剂:
甲氨蝶呤(MTX 10-15 mg/w)和硫唑嘌呤(AZA,2 mg/(kg.d))均须定期观察血象和肝功能情况。对于PM/DM中的激素抵抗和难治性PM/DM,需联合使用免疫抑制剂强化治疗:激素+MTX/AZA+CsA/CTX。
大剂量静脉丙球冲击(IVIg):
IVIg对改善重症DM/PM的呼吸肌、吞咽肌受累有效。
其他药物:
氯喹(250-500 mg/d)对DM皮损有一定疗效。
蛋白同化激素能促进肌肉蛋白合成,减少尿肌酸的排泄。
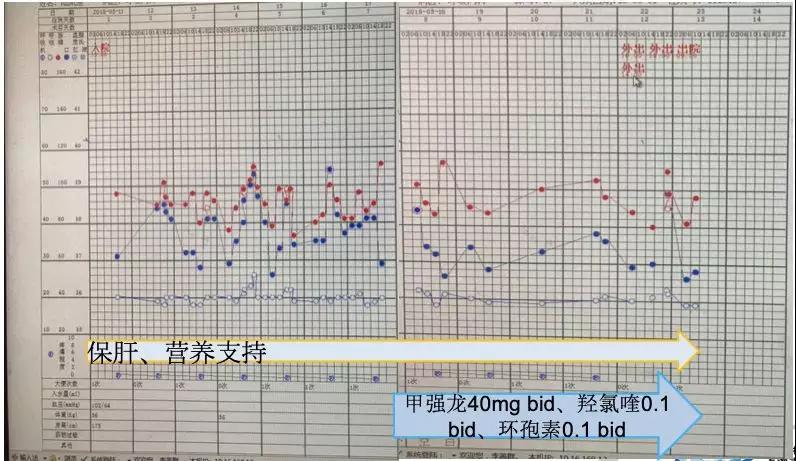
而对于本例患者,入院后我们给予了保肝、营养支持,从5月17日起给予甲强龙40 mg bid、羟氯喹0.1 bid、环孢素0.1 bid。
到5月21日检查CK、肝功能正常,遂让患者出院。12月5日复查,各项指标均正常。
最后小结:
重视病史采集及体格检查,不轻易放过阳性症状及体征。
发热伴肺间质性改变,需要鉴别累及多系统的疾病。
治疗反应与初步诊断不符时,不要盲目调整治疗方案;需重新进行诊断与鉴别,明确诊断后调整治疗方案。
专家点评

金美玲教授
在自身免疫相关性肺间质性疾病(CTD-ILD)中,皮肌炎合并肺间质性病变是一种来势凶猛、进展迅速、预后差的疾病。皮肌炎常有发热、肌痛、乏力等症状,并伴有典型皮疹,累及呼吸系统时出现咳嗽、气喘,如合并间质性肺炎,会出现呼吸困难进行性加重。
该病起病时症状复杂,累及多系统,早期表现不典型时诊断有一定的难度,往往会延误疾病早期诊断,从而导致疾病进行性进展。肺部表现可先与肌病症状,肺实质累及程度和严重性与肌病病程、全身改变无明显相关性。
该例患者起病时因发热、咳嗽,肺部阴影,被收治在呼吸科,抗感染治疗无效,检查发现皮疹,肌酶升高、肝酶升高,加用激素治疗后热退、症状改善。后又出现症状反复,进一步检查发现肌炎相关抗体阳性,明确诊断为皮肌炎合并肺部病变。按照皮肌炎治疗原则加大激素用量,同时加用环孢素后患者症状缓解、各项指标好转。
该病例在诊治过程中有以下几点需要引起重视:
CTD-ILD越来越常见,很多以肺部表现为首发症状被收治在呼吸科,呼吸科医师要对该类疾病非常熟悉,并以整体观对待该类疾病,重视其全身表现,特别是皮肤、肌肉、关节症状,不放过任何一个细节。
该例患者起病时心肌酶明显升高,提示有心脏受累。但是病例叙述过程中呼吸科临床医师对心脏似乎关注度不够。心脏受累患者预后差,要引起重视。
皮肌炎合并肺部病变总体预后差,治疗复杂,疾病容易反复,该病例在加大激素和加用环孢素后疾病有所控制,但后续的治疗仍然很复杂,需要呼吸科和风湿免疫科团队联合管理。
专家简介

金美玲教授
医学博士,主任医师,博士生导师
复旦大学附属中山医院呼吸科气道疾病中心主任,肺功能室主任
中国医师协会变态反应分会副会长,上海医学会呼吸分会哮喘学组副组长,中华医学会呼吸分会哮喘学组委员,中国研究型医院学会生物治疗学专业委员会常务委员,中国研究型医院学会罕见病分会理事,中国医师协会呼吸医师分会哮喘与变态反应工作委员会委员,上海医师协会整合医学分会委员。

张龙富
徐汇区中心医院呼吸与危重症医学科主治医生
现为复旦大学附属中山医院呼吸与危重症医学科,PCCM专科培训学员