Immunomedics公司宣布,美国食品药品监督管理局(FDA)已授予其sacituzumab govitecan的"快速通道"称号,用于治疗局部晚期或转移性尿路上皮癌(mUC)成人患者。这些患者先前已接受过PD-1或PD-L1抑制剂,并且在新辅助/辅助治疗过程中接受过含铂化疗/不符合铂类化疗资格的局部晚期或转移性患者。
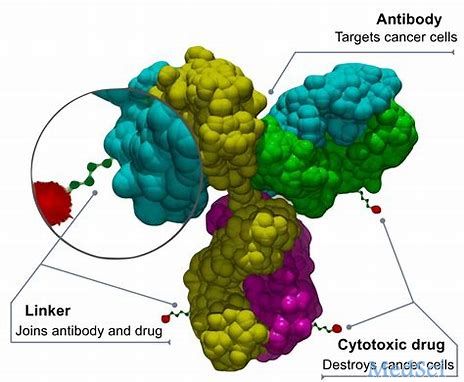
Sacituzumab govitecan是一种新型的抗体药物偶联物(ADC),由靶向TROP-2抗原的人源化IgG1抗体与化疗药物伊立替康(一种拓扑异构酶I抑制剂)的代谢活性产物SN-38偶联而成。
目前正在对mUC患者进行TROPHY U-01的2期临床研究,以评估Sacituzumab govitecan。在2019年欧洲肿瘤医学学会(ESMO)上,中期结果显示在PD-1或PD-L1抑制剂和铂类化疗后疾病进展的mUC患者中,Sacituzumab govitecan的总体响应率为29%。
已有100例先前接受铂类和PD-1或PD-L1抑制剂疗法的患者入组,目前已经完成研究,预计将于2020年下半年获得主要数据。
原始出处:
https://www.firstwordpharma.com/node/1713654?tsid=4
欧盟批准武田抗癌药Adcetris用于霍奇金淋巴瘤患者干细胞移植后的巩固治疗
![]() 0
2016-07-07
点击查看
0
2016-07-07
点击查看

阿斯利康靶向HER2的抗体药物偶联物在II期临床试验中显示出治疗前景
![]() 0
2019-05-11
点击查看
0
2019-05-11
点击查看

抗体药物偶联物治疗肺癌:U3-1402和DS-1062的临床结果更新将在2019年世界肺癌大会上发表
![]() 0
2019-08-22
点击查看
0
2019-08-22
点击查看
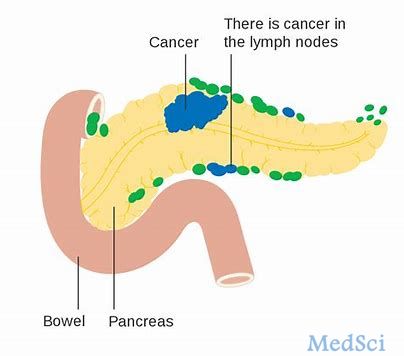
抗体药物偶联物OBI-999治疗胰腺癌获得FDA孤儿药物认定
![]() 0
2019-12-27
点击查看
0
2019-12-27
点击查看
抗体药物偶联物Enhertu达到HER2阳性转移性胃癌注册研究的主要终点
![]() 0
2020-01-27
点击查看
0
2020-01-27
点击查看

抗体药物偶联物ENHERTU获批治疗HER2阳性不可切除的或转移性乳腺癌
![]() 0
2020-03-25
点击查看
0
2020-03-25
点击查看
