肥胖与肾透明细胞癌 (ccRCC)的风险增加有关,但肥胖又矛盾地与该肿瘤的预后改善有关,其潜在机制尚不明确。现作者对肥胖患者和正常体重患者在原发肿瘤和瘤周脂肪组织中的血管生成和免疫转录组差异进行研究分析。
本文介绍了基因表达引起的微环境的差异有助于解释肥胖患者的生存优势(肥胖悖论)。
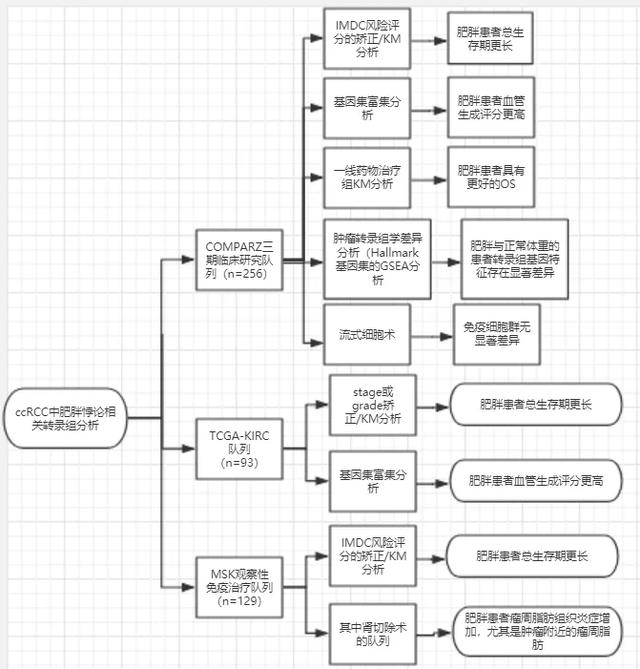
在COMPARZ队列的453名患者中,有375名(83%)患者具有可用的微阵列数据,治疗前BMI测量以及无进展和总体生存数据进行分析(表1)。除119名(26%)超重患者外,来自COMPARZ试验的最终队列包括256名(68%)患者(n=256)。
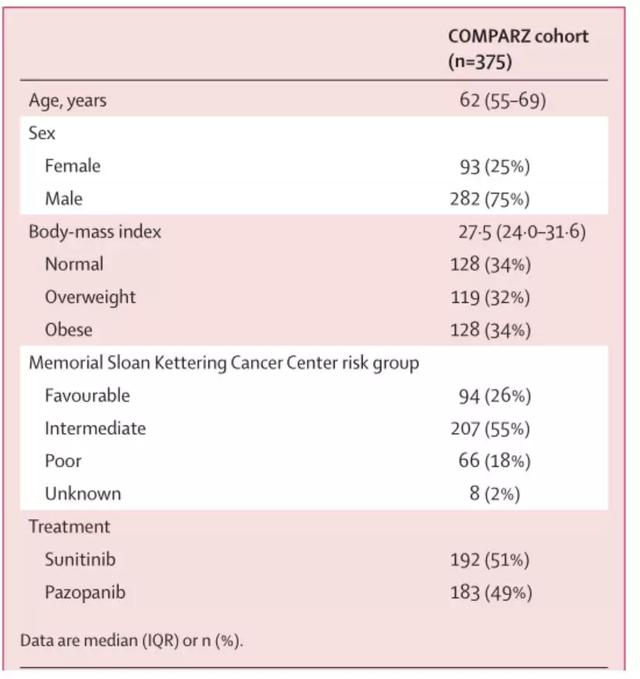
表1.COMPARZ临床试验队列的人口统计学和临床特征
TCGA-KIRC队列中的332例患者中,评估了经肾切除术治疗的152例(46%)晚期(即AJCC III和IV期)ccRCC患者的临床和人口统计学数据(表2)。在排除59名(39%)超重患者后,最后获得的队列包括93名患者(n=93)。
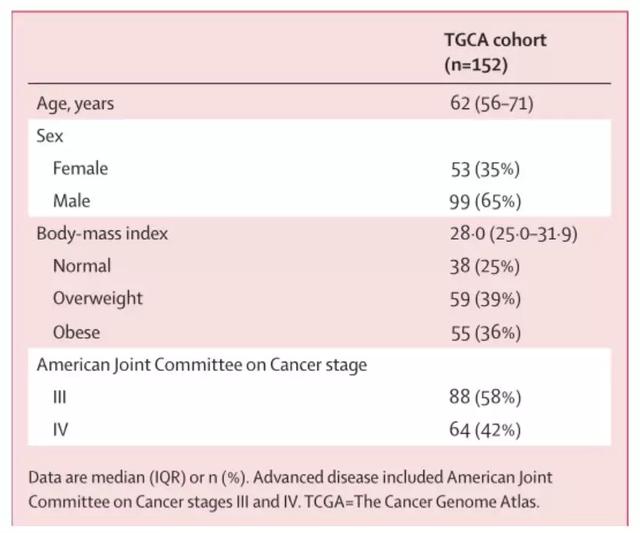
表2.晚期透明细胞肾细胞癌TCGA-KIRC队列的人口学和临床特征
从62例MSK肿瘤周围脂肪组织队列中进行肾脏切除术的非转移性透明细胞RCC患者中获得了原发性肿瘤和肿瘤周围脂肪样品。在这个队列中,从59名患者的PNN(肾周附近)肿瘤周围脂肪,25名患者的PNA(远离肾周)肿瘤周围脂肪以及55名患者的肿瘤组织中取样。在排除超重患者之后,最终队列包括41名(69%)PNN样本患者, PNA样本为17(68%),肿瘤样本为37(67%)。从最初的203名参与者的MSK免疫治疗研究人群中排除74名(36%)超重患者后,总生存分析的最终队列包括129名(64%)参与者(表3)(n=129)。
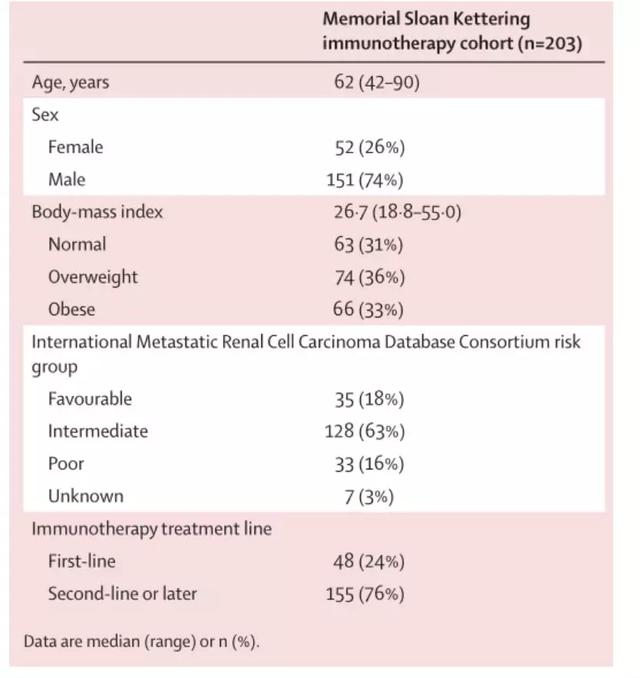
表3. 采用MSK免疫治疗的临床试验队列的人口统计学和临床特征
根据KM生存分析,在三组中都发现肥胖患者的总生存期更长。在TCGA-KIRC队列中,经分期校正后,肥胖患者的总体存活期长于正常体重组;在COMPARZ队列中,经IMDC风险评分校正后,胖患者的总体存活期也长于正常体重组。在MSK免疫疗法队列中,经IMDC风险评分校正后,BMI与死亡率的无显著差异(如图1)。
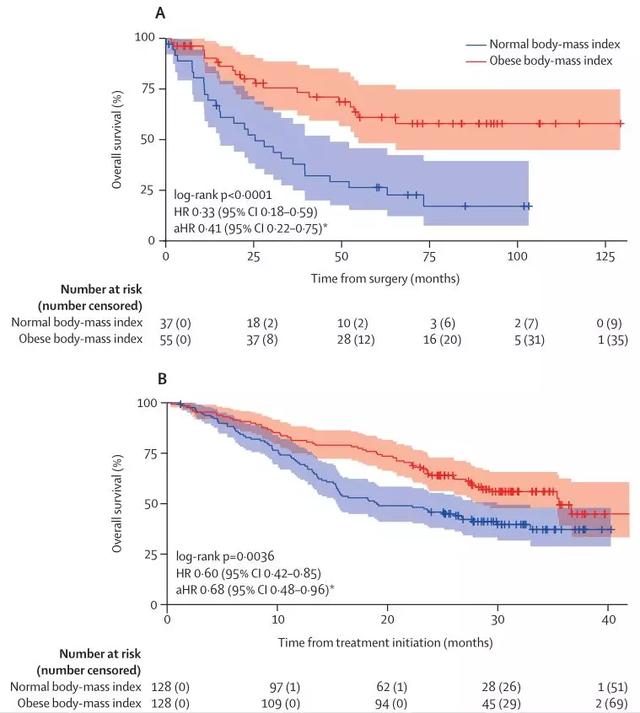
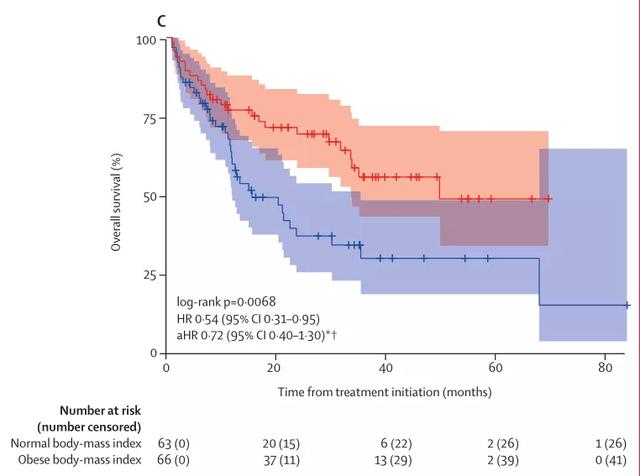
图1.TCGA-KIRC队列 (A)、COMPARZ 队列(B)和MSK免疫治疗队列(C)的总生存期
对CPMPARZ队列KM分析后,KM曲线显示,COMPARZ队列中肥胖患者比正常体重患者具有更好的PFS。
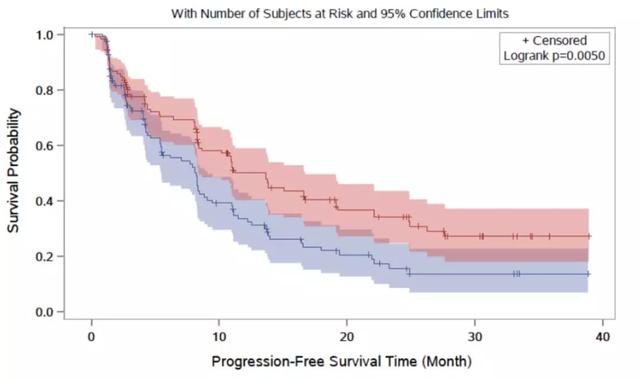
图S1.COMPARZ队列中肥胖患者比正常体重患者具有更好的PFS
KM曲线显示了在使用一线酪氨酸激酶抑制剂(pazopanib或Sunitinib)的两个治疗组中,肥胖患者的OS仍然较正常体重患者好。
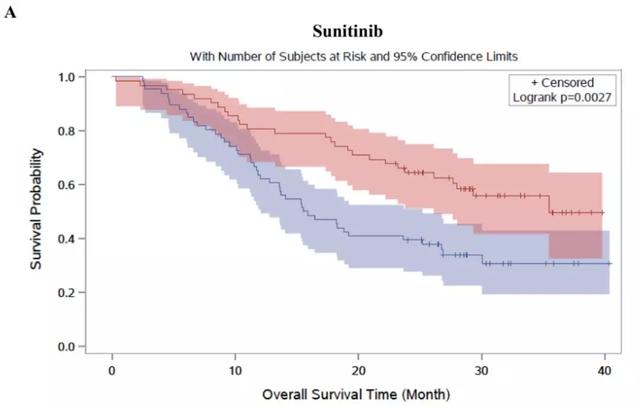

图S2.COMPARZ队列使用一线药物治疗组的总生存期分析
做完上述分析,作者在三个队列中确认肥胖悖论存在之后,接下来在COMPARZ队列中对肥胖和正常体重患者评估了肿瘤转录组学差异。先是做了Hallmark基因集的GSEA分析,比较肥胖患者与正常体重患者之间的差异:肥胖患者中显示缺氧、TGF-β、上皮-间充质转变和血管生成信号通路显著上调,提示伤口愈合途径的激活(图A)。图B是对图A筛选的几个基因表达通路的Enrichment plots。

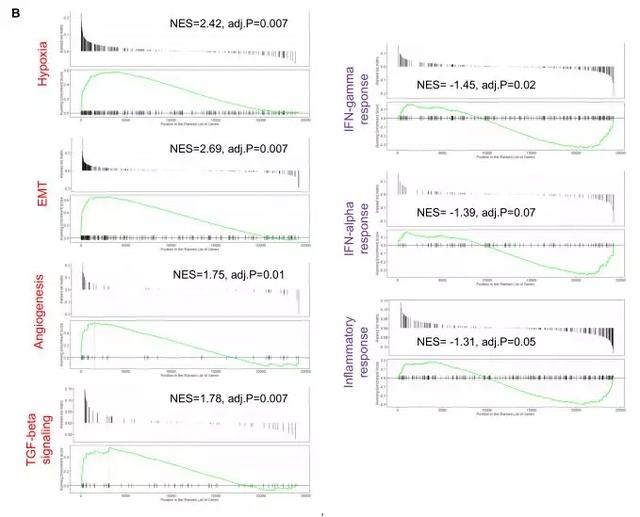
图S4.COMPARZ队列中肥胖患者与正常体重患者的ccRCC肿瘤转录组基因特征存在显著差异
在GESA衍生的特征基因集血管生成评分比较中,肥胖患者高于正常体重患者(如图2)。
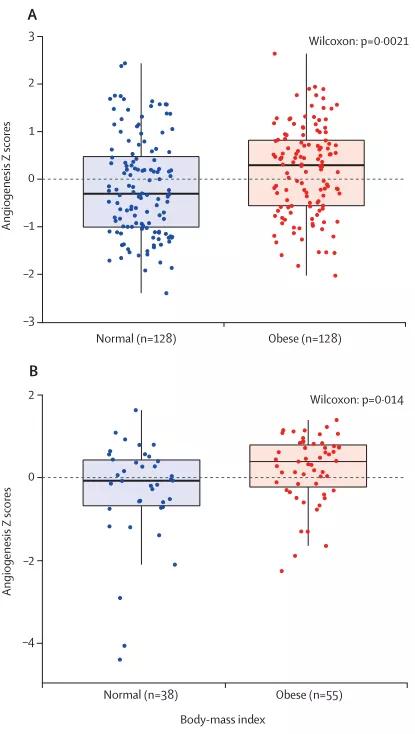
图2.COMPARZ队列(A)与TCGA-KIRC队列 (B)中肥胖原发肿瘤患者与正常体重患者的血管生成的z score
对正常体重(7例)与肥胖(16例)患者的原发肿瘤的主要免疫细胞数量均采用流式细胞术进行评估。图A显示了肥胖患者与正常患者之间的免疫细胞群的总体差异。图B明确显示了肥胖和正常体重患者T细胞群的浸润水平。发现正常体重与肥胖患者肿瘤的免疫细胞群无明显差异,免疫细胞浸润的程度与BMI无关。
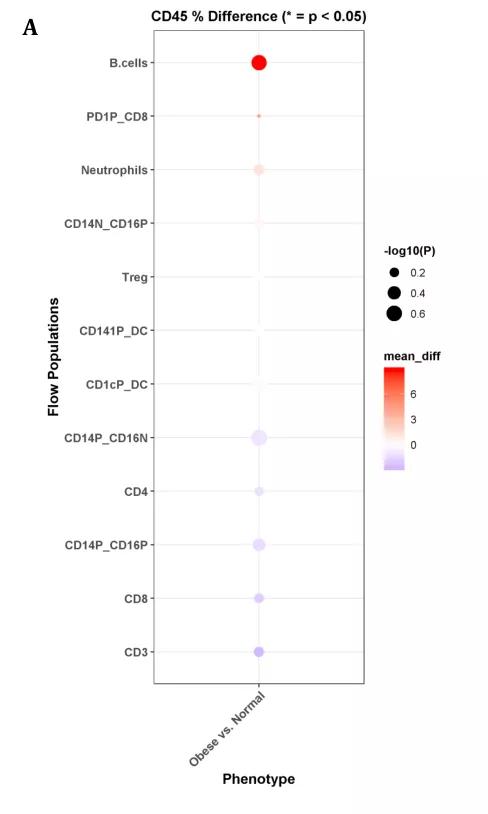
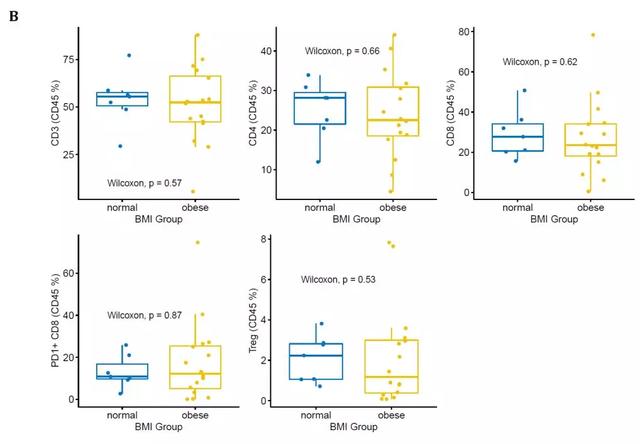
图S9.用流式细胞术分析正常体重与肥胖患者肿瘤的免疫细胞群无明显差异
在MSK的非转移性ccRCC患者的前瞻性队列中,作者合并了20个最显著的丰富的IPA规范通路,这些通路来自于肥胖和正常体重患者的PNN和PNA样本的比较(图A)。肥胖和正常体重患者的PNN和PNA样本之间的免疫浸润(ssGSEA评分)比较(图B)。
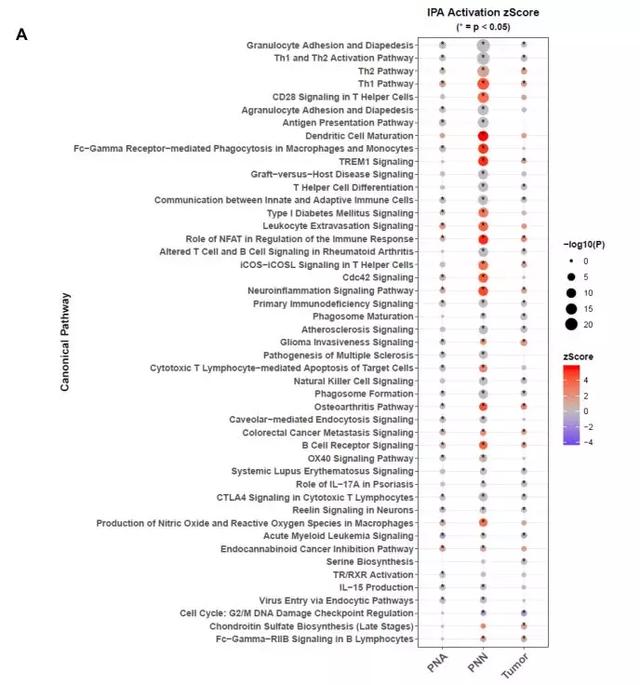
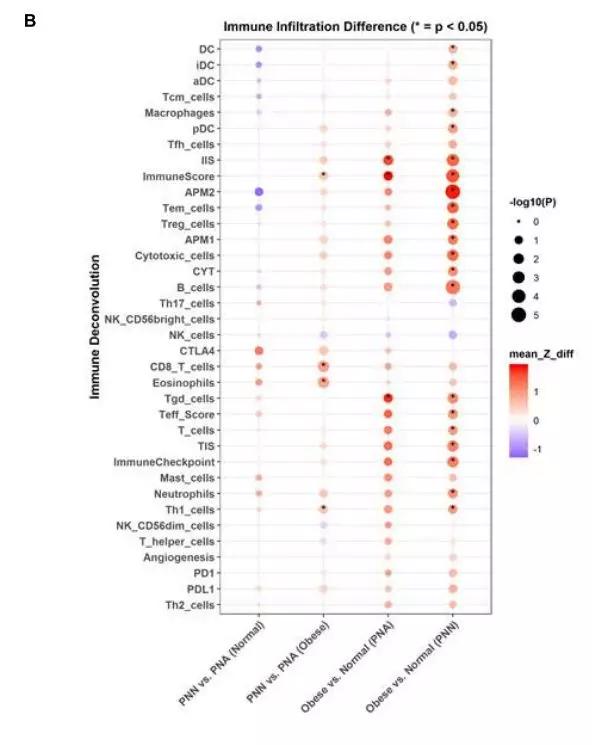
图S5.与正常体重的患者相比,肥胖患者的肾周脂肪显示出炎症和缺氧增加
综上,在COMPARZ试验队列中,经过IMDC风险评分调整后,发现相对于正常体重患者,酪氨酸激酶抑制剂治疗提高了肥胖患者的生存率,特别是接受sunitinib治疗的患者。IMDC风险评分模型包含的组分间接反映宿主因素对癌症系统性炎症作用(例如贫血,中性粒细胞增多,和血小板增多症),这些因素可能也是免疫治疗结果和BMI之间关联机制的原因。发现肥胖患者的肿瘤血管生成分数高于正常体重患者,与之前其他的研究结果表明的,参与血管生成,β-氧化途径等等基因的富集的现象一致。因此,血管生成的差异可以部分解释肥胖患者接受酪氨酸激酶抑制剂治疗后的较好预后。
此研究为肥胖悖论提供了生物学支持。在患有ccRCC的患者观察到肥胖患者相对于正常体重的患者肿瘤微环境的差异:特别是肥胖患者的肿瘤的血管生成增加,但总体炎症无明显差异。值得注意的是肥胖患者的肿瘤周围脂肪显示增加的炎症和缺氧状况。透明细胞癌与瘤周脂肪组织微环境的复杂相互作用可能具有临床意义,值得进一步研究。
原始出处:
Sanchez A, Furberg H, Kuo F, Vuong L, Ged Y, Patil S, Ostrovnaya I, Petruzella S, Reising A, Patel P, Mano R, Coleman J, Russo P, Liu CH, Dannenberg AJ, Chan TA, Motzer R, Voss MH, Hakimi AA. Transcriptomic signatures related to the obesity paradox in patients with clear cell renal cell carcinoma: a cohort study.Lancet Oncol. 2020 Feb;21(2):283-293
PNAS:肥胖、糖尿病竟“重女轻男”!当神经元受损时,女性代谢异常而男性无碍
![]() 0
2020-08-10
点击查看
0
2020-08-10
点击查看

青年时期肥胖,老年痴呆风险增加!
![]() 0
2020-08-12
点击查看
0
2020-08-12
点击查看

J Alzheimers Dis :体重对大脑影响多大?3.5万次大脑扫描结果惊人
![]() 0
2020-08-13
点击查看
0
2020-08-13
点击查看

Nat Neurosci :别指望节食减肥了,高脂饮食后大脑已经“叛变”了
![]() 0
2020-08-15
点击查看
0
2020-08-15
点击查看
CMAJ:肥胖是一种慢性病!加拿大肥胖管理指南
![]() 0
2020-08-15
点击查看
0
2020-08-15
点击查看

Nat Commun:肠道微生物共丰度网络在炎症性肠病和肥胖中的特异性
![]() 0
2020-08-15
点击查看
0
2020-08-15
点击查看