心血管并发症是糖尿病最常见且最严重的并发症之一。目前在临床上,针对糖尿病心肌损伤的治疗手段十分有限。因此深入研究糖尿病心肌损伤的发病机制,发现新的治疗靶点仍迫在眉睫。miRNA存在于多种亚细胞器中,通过截然不同的分子机制调节下游靶基因。然而,将miRNA靶向表达于特定亚细胞器在目前仍有技术困难,亚细胞miRNA治疗的临床转化尚需继续探索。AGO2蛋白是RNA诱导沉默复合体的核心催化酶,不仅介导miRNA在胞浆中的经典作用机制,对miRNA在细胞核和线粒体中的功能也是不可或缺的。
2023年12月21日,华中科技大学同济医学院附属同济医院心血管内科汪道文/李华萍/陈琛教授团队在Circulation杂志在线发表题为“Ago2 protects against diabetic cardiomyopathy via activating mitochondrial gene translation”的研究论文,揭示了AGO2蛋白在糖尿病心肌病中作用及机制,为糖尿病心肌病的发病及治疗提供新思路

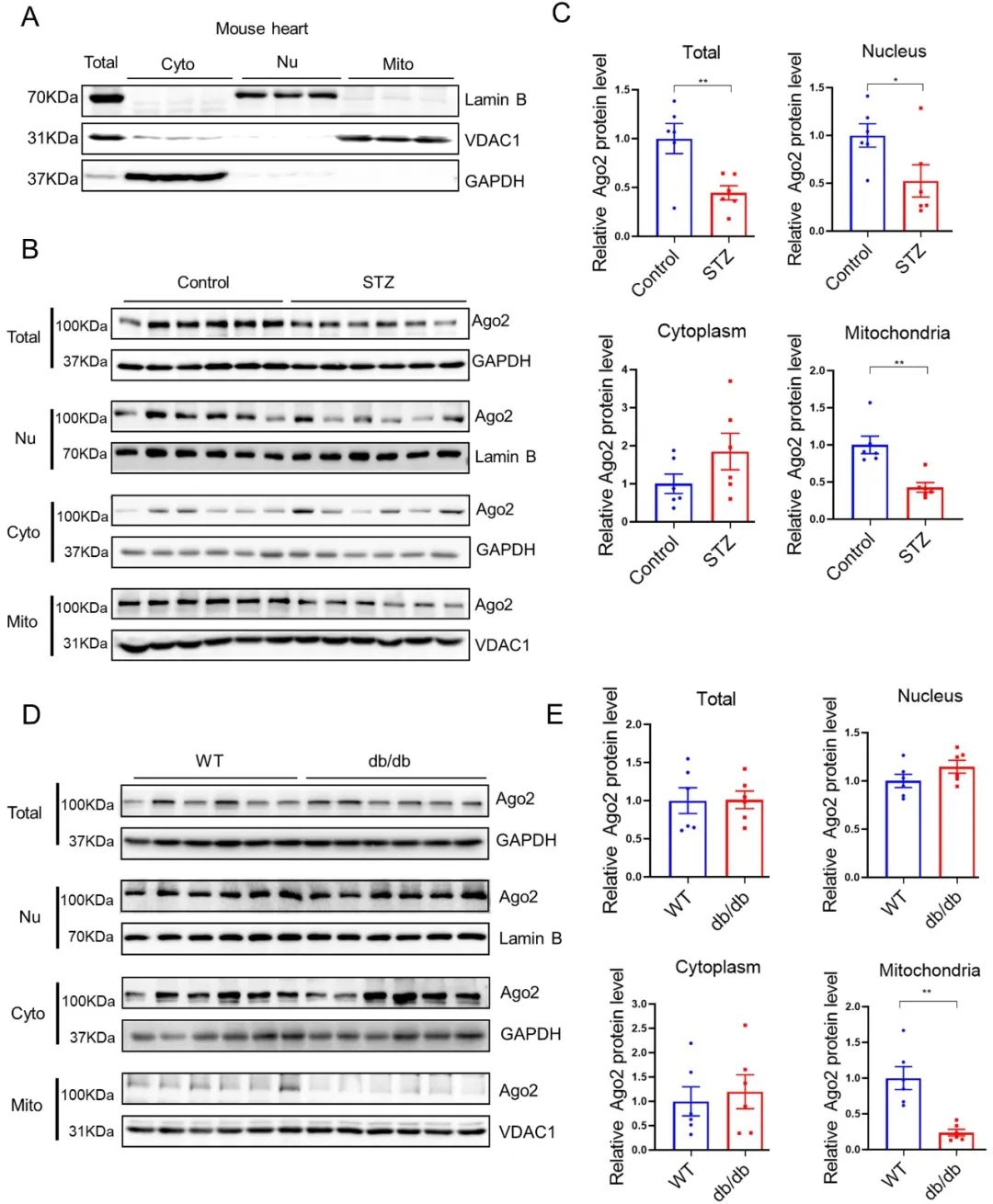
首先,作者通过分离1型和2型糖尿病小鼠心脏的细胞浆、细胞核和线粒体组分,检测AGO2在糖尿病早期的心脏中亚细胞表达水平。结果显示,线粒体AGO2的减少是1型和2型糖尿病心脏中的共有变化,而且这种变化不伴有细胞浆AGO2水平的降低,提示糖尿病时AGO2向线粒体内的转位出现障碍。
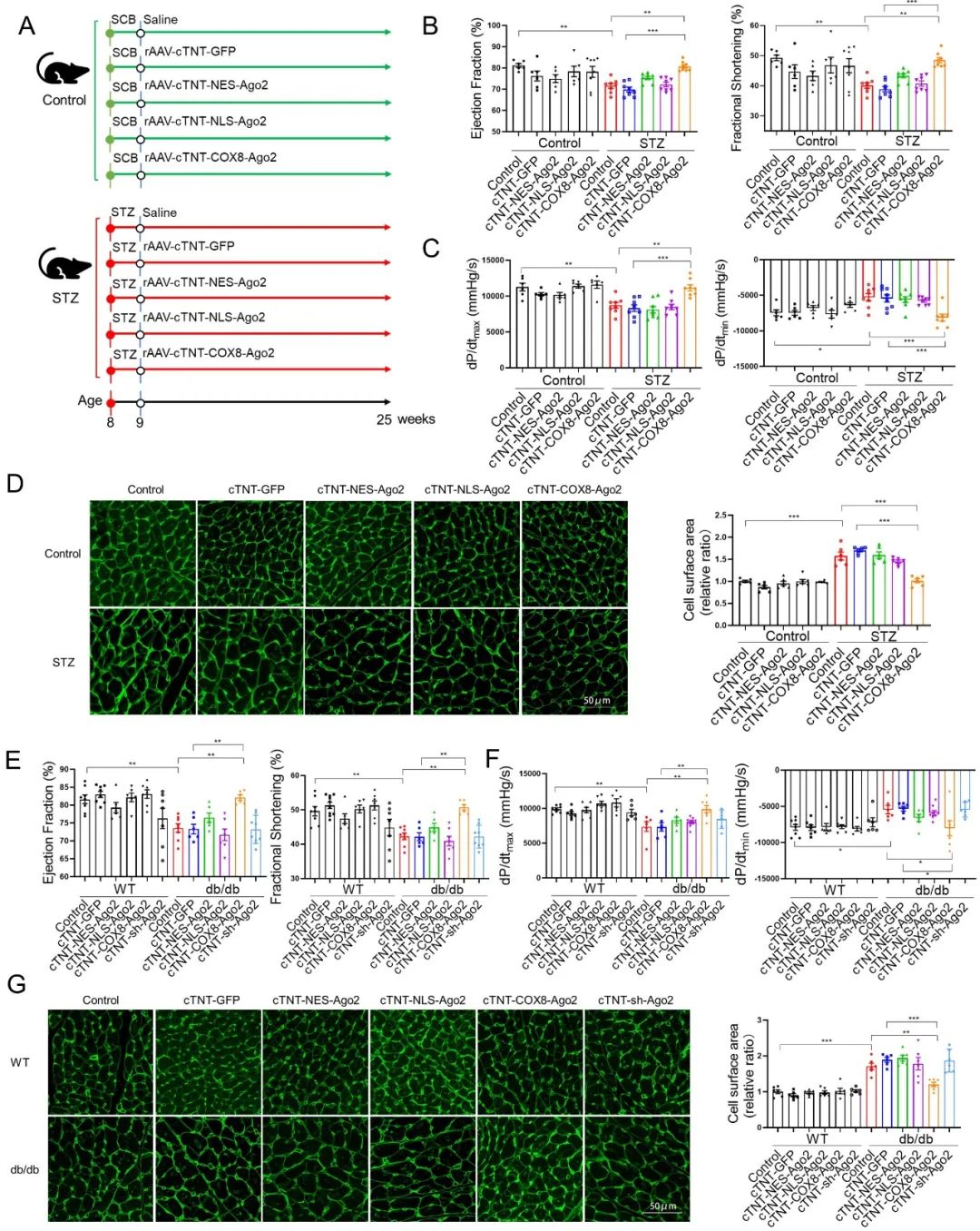
利用9型重组腺相关病毒和心肌特异性启动子(cTNT)在糖尿病小鼠心肌中高表达不同亚细胞定位的AGO2 (NLS:胞核定位信号;NES:出核定位信号;COX8:线粒体定位序列),结果显示,线粒体定位AGO2高表达能够显著改善1型和2型糖尿病小鼠的心功能,细胞浆和细胞核定位的AGO2则对糖尿病小鼠心功能没有显著影响。因此,后续研究主要关注线粒体AGO2的具体作用机制。
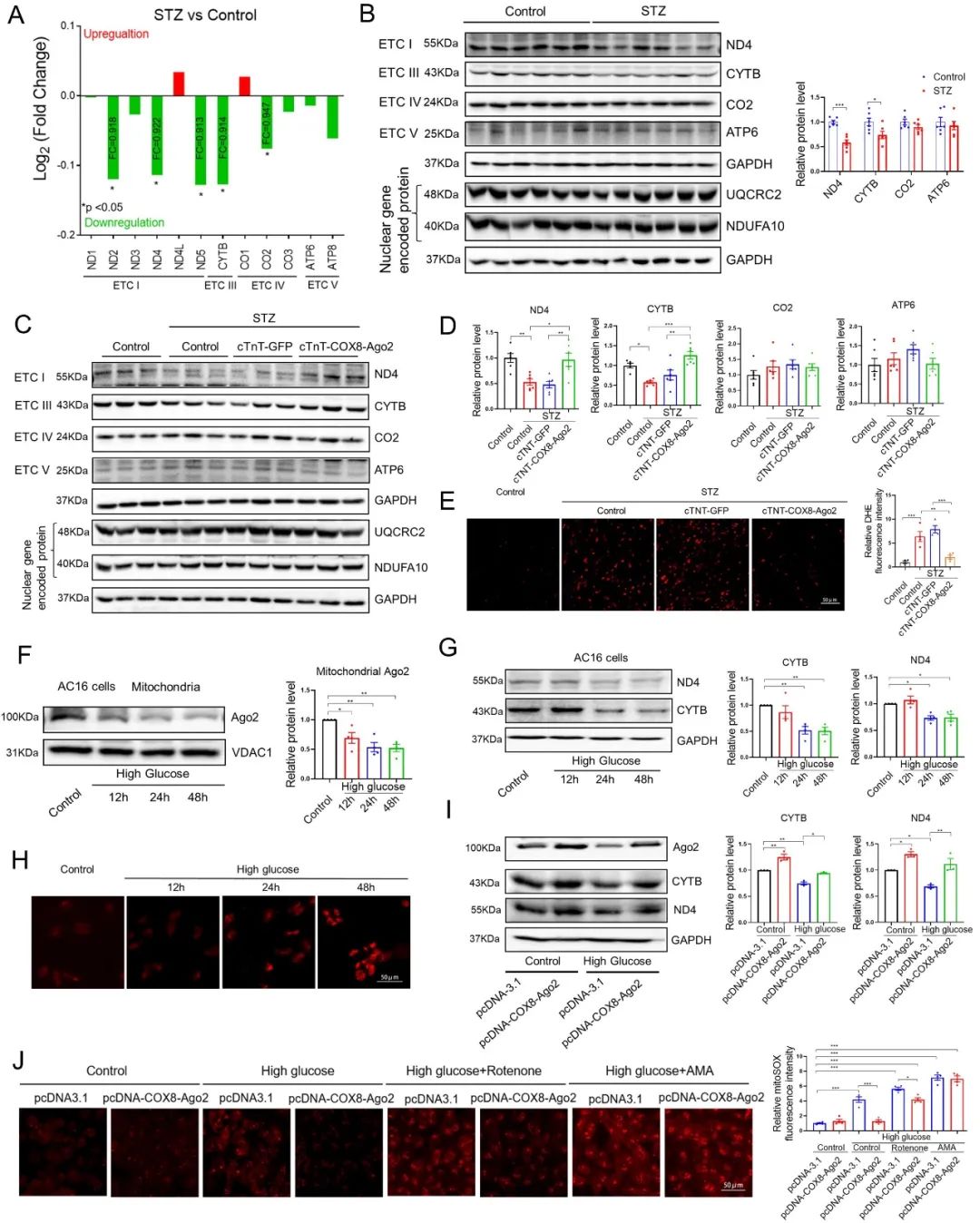
由于在线粒体中,只有线粒体基因的转录或翻译活动能直接受到AGO2/miRNA复合物的调控,因此作者首先通过蛋白质谱检测糖尿病小鼠心脏中线粒体基因的表达水平,并发现电子传递链复合物(ETC)中的线粒体基因存在表达失衡。通过在心肌中高表达线粒体定位AGO2可以恢复下降的线粒体基因CYTB和ND4的表达水平,减少心脏氧化应激水平。在细胞实验中,作者发现高糖刺激会引起线粒体AGO2和CYTB蛋白水平下降;而高表达线粒体AGO2能够阻断高糖刺激对CYTB的下调作用,从而减少线粒体活性氧的产生。
进一步地,作者通过AGO2免疫共沉淀和功能实验,揭示了线粒体AGO2通过募集线粒体翻译延长因子TUFM结合到线粒体CYTB的mRNA上,从而激活CYTB的翻译过程。有趣的是,线粒体AGO2对线粒体基因的调控是不均衡的,其原因在于线粒体AGO2增强线粒体基因翻译依赖miRNA所提供的碱基序列配对信息。因此,miRNAs的序列特异性导致了线粒体AGO2对线粒体基因翻译的选择性调控。

最后,作者揭示了糖尿病时AGO2线粒体转位减少的原因。AGO2蛋白可以发生多种翻译后修饰,其中丙二酰化修饰水平在1型和2型糖尿病心脏中显著增加。细胞浆中定位的短SIRT3调控AGO2蛋白的丙二酰化修饰过程。糖尿病心脏中短SIRT3含量的减少导致AGO2蛋白丙二酰化修饰水平增加。高表达短SIRT3能够减少AGO2蛋白的丙二酰化修饰水平并增加AGO2的线粒体转运能力。

AGO蛋白的丙二酰化修饰阻碍了其与包含TIMM17b的线粒体转运蛋白的结合,从而减少了AGO2向线粒体内的转位。通过AGO2丙二酰化位点突变模拟AGO2的去丙二酰化状态,或通过SIRT3高表达降低AGO2的丙二酰化水平,均能够增加AGO2向线粒体内的转位。
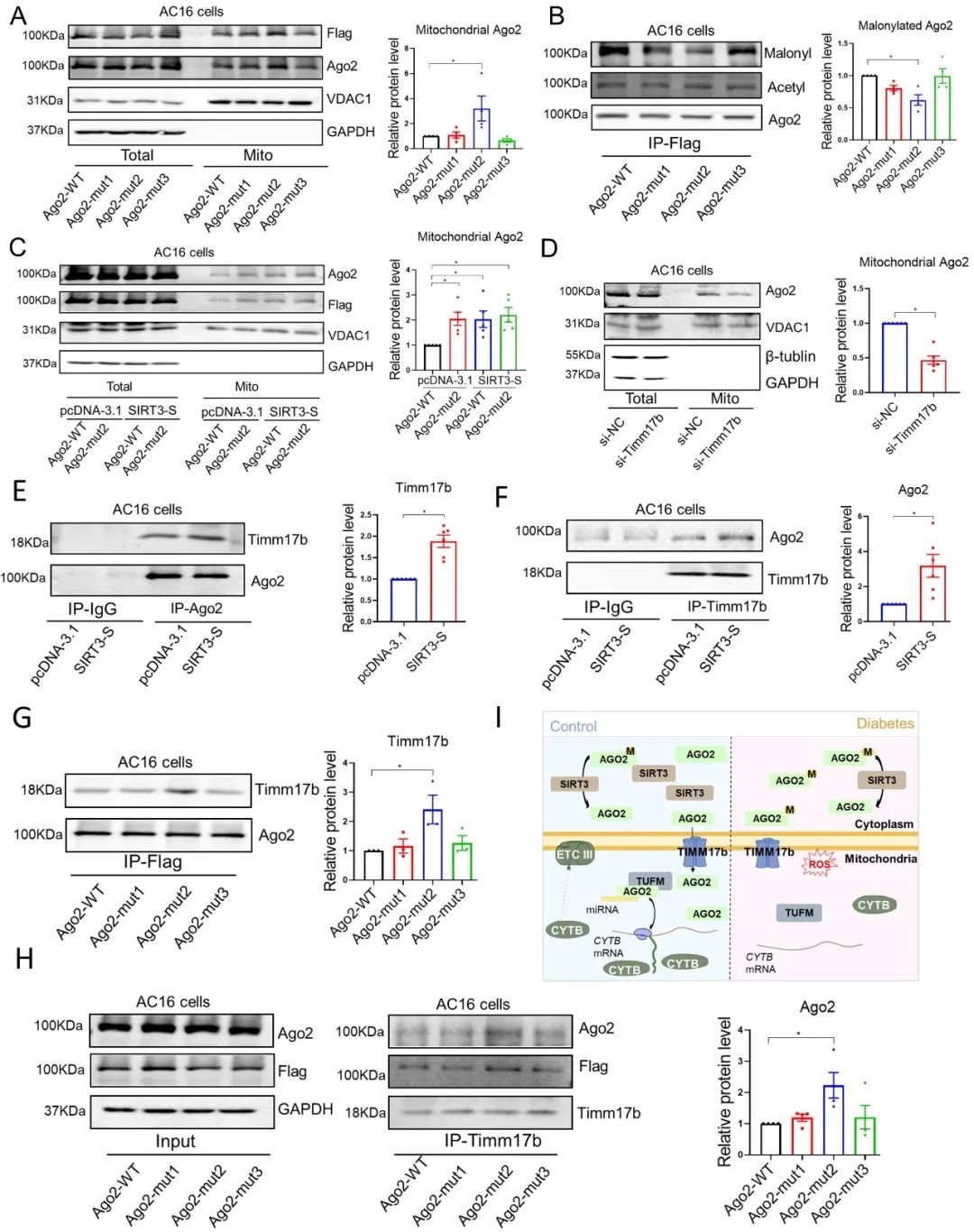
综上所述,在糖尿病心脏损伤中,糖尿病心脏中短SIRT3水平降低,导致AGO2蛋白丙二酰化水平升高,阻碍其与含TIMM17b的线粒体转运蛋白结合,从而导致AGO2蛋白向线粒体内转运减少,线粒体活性氧产生增多,造成心功能损伤。高表达线粒体AGO2通过募集线粒体翻译延长因子TUFM,在miRNA的介导下特异性激活线粒体基因CYTB、ND4等的翻译,使其蛋白水平升高,增强线粒体电子传递链功能,减少线粒体活性氧的产生,从而改善了糖尿病小鼠的心功能。本研究发现SIRT3-AGO2/miRNAs-TUFM-CYTB通路是糖尿病代谢障碍与心肌细胞线粒体呼吸链失平衡之间的桥梁分子。rAAV9介导的线粒体AGO2过表达通过激活线粒体基因翻译从而降低心脏氧化应激水平,为糖尿病心脏损害的防治提供了新的靶点。
近年来,该团队对亚细胞定位miRNA的功能及作用机制展开了深入研究,揭示细胞核和线粒体miRNA通过非经典作用的方式调控心血管疾病的发生发展(Circulation. 2016;134:734, Circ Res. 2019;125:1106)。此项研究是该团队在之前研究的基础上,进一步探索miRNA及其作用蛋白AGO2在线粒体的非经典作用机制,是糖尿病心肌损伤发病机制的又一重大发现,并有望进行临床转化,为糖尿病心肌损伤的治疗提供全新的治疗策略。
华中科技大学同济医学院附属同济医院心内科博士詹佳冰、金坤瑛和谢融为本文共同第一作者,同济医院李华萍副教授、陈琛教授和汪道文教授为共同通讯作者。该研究获得国家自然科学基金(批准号:82170273, U22A20266, 82241034, 82270363)等资助。
原文链接:
https://www.ahajournals.org/doi/10.1161/CIRCULATIONAHA.123.065546
2024年ADA指南发布!心血管疾病和风险管理方面章节的九大更新
![]() 0
2023-12-17
点击查看
0
2023-12-17
点击查看

JAHA:钠-葡萄糖共转运蛋白2抑制剂对糖尿病患者导管消融后房颤复发的影响
![]() 0
2023-12-14
点击查看
0
2023-12-14
点击查看

一文读懂口服葡萄糖耐量试验(OGTT)
![]() 0
2023-12-20
点击查看
0
2023-12-20
点击查看

超10万人数据,早餐、晚餐提早一个小时,糖尿病风险降低59%,脑血管疾病风险降低28%
![]() 0
2023-12-19
点击查看
0
2023-12-19
点击查看

【内分泌医生今日分享】糖尿病这十个公式不可不看
![]() 0
2023-12-20
点击查看
0
2023-12-20
点击查看

Diabetes Obes Metab :钠-葡萄糖共转运蛋白-2抑制剂停药后的预测因素
![]() 0
2023-12-21
点击查看
0
2023-12-21
点击查看