近日,中山大学肿瘤防治中心陈帅教授课题组与黄文林教授等合作,在Nature Communications杂志在线发表题为Cyclophilin J limits inflammation through the blockage of ubiquitin chain sensing的研究论文,揭示了一个脯氨酸异构酶cyclophilin J能够竞争性阻断TAB2/3与K63型泛素链的结合,对于维持天然
免疫应答的平衡具有重要作用。
研究背景
天然
免疫是机体抵御外界微生物入侵的第一道防线。当
感染发生时,宿主细胞的模式识别受体能够识别微生物的病原相关分子模式或损伤相关分子模式,进而启动下游NF-κB、JNK、p38等信号通路,诱导炎症发生。天然免疫应答过强或不足都会对机体产生危害。泛素在天然免疫应答和炎症中发挥着重要的调节作用。
2011年北京生命科学研究所邵峰院士课题组在Nature杂志报道了大肠杆菌NleE蛋白能够通过III型分泌系统进入宿主细胞,并催化TAB2/3的NZF结构域发生半胱氨酸残基的甲基化修饰,从而阻断NZF与K63型泛素链的结合,抑制NF-κB信号通路和炎性细胞因子表达,是大肠杆菌逃逸宿主免疫监视的重要机制。然而是否存在宿主蛋白能够调控该“泛素感受”过程目前尚未知晓。
亲环素(Cyclophilin)是脯氨酸顺反异构酶(PPIase)蛋白家族中的一族,能够催化多肽链中脯氨酰胺键的顺反异构,它们一般都能与免疫抑制剂环孢菌素A(Cyclosporine A,CsA)结合并受其抑制。Cyclophilin J(CYPJ)是陈帅教授在复旦大学就读博士期间参与克隆的一个Cyclophilin家族新成员 。
研究内容概览
本研究中,
科研人员通过在293T细胞中筛选对NF-κB荧光素酶报告质粒有调控作用的蛋白,发现CYPJ及其家族成员CYPA参与了天然免疫应答的负调控,并且这种抑制作用与其PPIase活性无关。
当NF-κB信号通路被TNF、LPS、VSV等激活的时候,虽然CYPJ转录水平不发生改变,但蛋白水平明显上调,呈现一种负反馈的调节方式。通过Co-IP和GST pull-down实验,研究人员发现CYPJ特异性地与TAB2和TAB3发生相互作用,并且CYPJ的C端肽段与TAB2/3的NZF结构域直接结合。CYPJ与TAB2/3的NZF结构域直接相互作用,竞争性拮抗K63型泛素链与TAB2/3蛋白的结合,导致K63型泛素链传递受阻,信号通路传递中断。
Fig1:The C-terminal of CYPJ interacts with TAB2 and TAB3
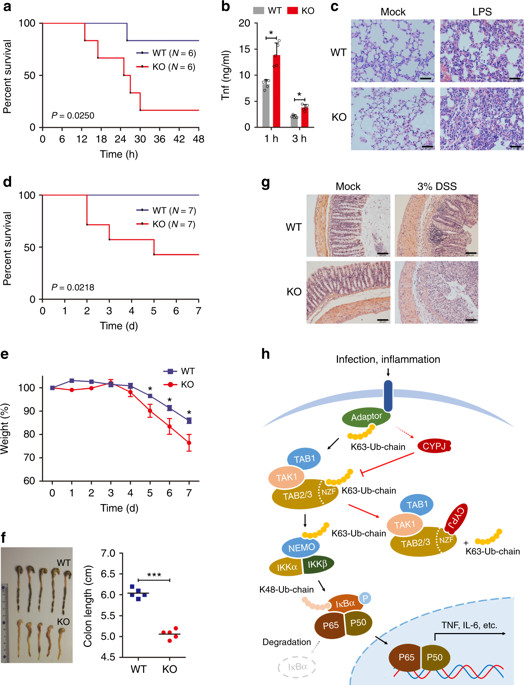
此外,通过CRISPR/Cas9技术构建Cypj敲除(knock out,KO)小鼠,采用两种炎症模型对CYPJ在体内的功能进行验证:LPS诱导系统性炎性和DSS诱导肠炎。KO小鼠均表现出更强烈的炎症反应,死亡时间明显缩短,组织损伤更为严重。体外体内实验一致表明,CYPJ是NF-κB信号通路的新型负反馈调控因子,在炎症消退过程中发挥重要作用。
Fig 2:Cypj protects mice from lethal acute inflammation and DSS-colitis
结语
脯氨酸异构酶 Cyclophilin J(CYPJ)是陈帅教授在复旦大学就读博士期间参与克隆的一个Cyclophilin家族新成员,本研究成功揭示了CYPJ能够竞争性阻断TAB2/3与K63型泛素链的结合,对于维持天然免疫应答的平衡具有重要作用。
中山大学肿瘤防治中心盛春姐博士后为论文的第一作者,陈帅教授为论文的通讯作者;中山大学肿瘤防治中心黄文林教授、徐大志教授、广东药科大学陈宏远教授、美国梅奥诊所黄浩杰教授等也为论文做出了重要贡献。
来源:病毒学界
版权声明:
本网站所有注明“来源:梅斯医学”或“来源:MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有,非经授权,任何媒体、网站或个人不得转载,授权转载时须注明“来源:梅斯医学”。本网所有转载文章系出于传递更多信息之目的,且明确注明来源和作者,不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。同时转载内容不代表本站立场。
在此留言