铁死亡是一种铁依赖性,区别于凋亡的细胞死亡过程,其参与各种退行性疾病,并代表了某些癌症的可靶向的易感性。铁死亡易感性细胞状态可以预先存在于某些谱系的细胞中,并在细胞状态转换过程中获得。然而,确切地说,至今为止,我们对于铁死亡易感性的动态调节仍然是不太了解。

最近,研究人员在Nature杂志发文,其使用全基因组的CRISPR-Cas9抑制剂筛选,发现氧化性细胞器过氧化物酶体是人类肾癌和卵巢癌细胞的铁死亡敏感性的关键贡献者。
在该研究中,为了确定调节铁死亡易感性的因素,研究人员在铁死亡易感性透明细胞肾细胞癌(ccRCC)模型786-O3和高等级血清卵巢癌模型OVCAR-8中进行了两个独立的全基因组CRISPR-Cas9抑制剂筛选。
在这两个模型中,通过使用ML210或1S,3R-RSL3(RSL3)抑制脂质过氧化修复酶谷胱甘肽过氧化物酶4(GPX4),诱导铁死亡。这两个筛选揭示了已知的铁死亡调节器-包括酰基-CoA合成酶长链家族成员4(ACSL4),证实了该筛选识别铁死亡敏感性的介质的可信度。
在以前未被表征的促进铁死亡的基因中,使用STRING(蛋白质网络数据库)和研究人员开发的名为基因列表网络富集分析(GeLiNEA)的路径分析算法,过氧化物酶体成分被发现是最丰富的基因簇。
在这两个筛选中确定的过氧体基因包括过氧化物酶体生物发生基因PEX10和PEX3,以及编码过氧化物酶体中酶类的烷基甘油酯磷酸合成酶(AGPS)和脂肪酰基-CoA还原酶1(FAR1)。其他富集的过氧化物酶体基因包括甘油磷酸O-乙酰转移酶(GNPAT),PEX12和PEX7。
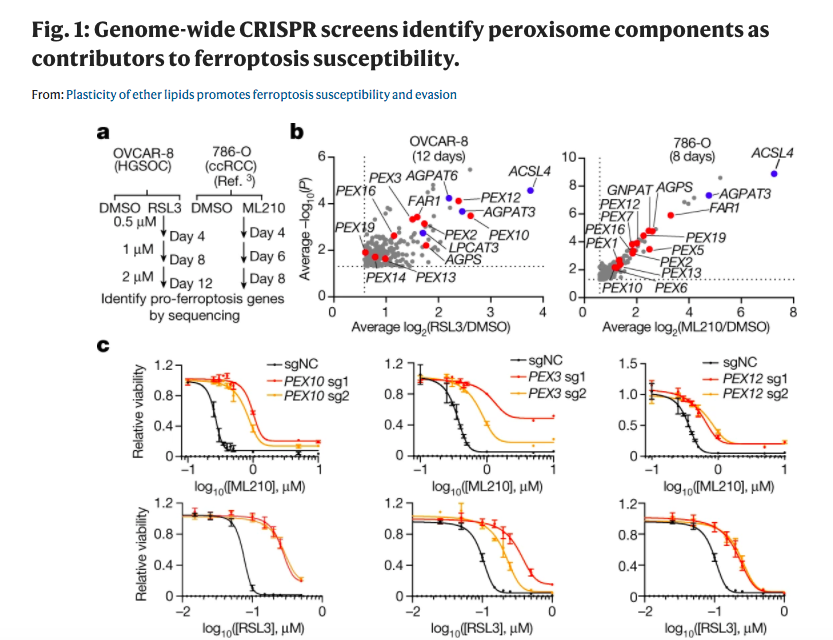
由于过氧化物酶体以前没有牵涉到铁死亡过程中,因此研究人员专注于阐明它们在这个过程中可能的作用。
使用脂质组分析,研究人员表明,过氧化物酶体通过合成多不饱和醚磷脂(PUFA-ePLs),作为脂质过氧化的底物,反过来,导致铁死亡的诱导。
最初对铁死亡敏感的癌细胞在小鼠体内可切换到铁死亡抵抗状态,这与PUFA-ePLs的广泛下调有关。
研究人员进一步发现,PUFA-ePLs的促铁死亡作用可以从肿瘤细胞扩展到其他细胞类型,包括神经元和心肌细胞。
总之,这项工作揭示了过氧化物酶体-醚-磷脂轴在驱动铁死亡易感性和逃避铁死亡方面的作用,突出了PUFA-ePL作为一种独特的功能性脂质类别,在细胞状态转换过程中受到动态调节,并提出了在涉及铁死亡的疾病中进行治疗干预的多个调节节点。
原始出处:
Yilong Zou et al. Plasticity of ether lipids promotes ferroptosis susceptibility and evasion. Nature (2020).
Acta Neuropathologica:伴有RELA改变的幕上膜室间隔瘤中CDKN2A缺失是提后不良的标志物:HIT室间隔瘤试验的回顾性分析
![]() 0
2020-08-22
点击查看
0
2020-08-22
点击查看

BMJ:女性染发剂的使用与肿瘤风险评估
![]() 0
2020-09-05
点击查看
0
2020-09-05
点击查看

Nat Commun:两个大型队列鉴定出相同的癌症遗传风险
![]() 0
2020-09-05
点击查看
0
2020-09-05
点击查看

黑科技燃爆:一把“冰刀”“冻死”肿瘤,第二天可出院……
![]() 0
2020-09-08
点击查看
0
2020-09-08
点击查看

李懿点评:TCR-T细胞疗法,三大障碍有待突破
![]() 0
2020-09-10
点击查看
0
2020-09-10
点击查看

BMJ:意外减重人群的肿瘤风险研究
![]() 0
2020-09-14
点击查看
0
2020-09-14
点击查看
