肿瘤的发生和发展与致癌基因的激活和表观遗传学的失调密切相关,这些因素导致了严重肿瘤免疫逃逸,并降低了免疫疗法的临床治疗效果。表观遗传学免疫疗法(Epigenetic Immunotherapy)作为一种前沿性的癌症治疗策略,在克服癌症免疫抑制方面具有相当大的潜力,但目前在临床上鲜有相关药物组合和递送策略。
近日,四川大学生物医学工程学院/国家生物医学材料工程技术研究中心何斌研究员/蒲雨吉副研究员团队报道了一种名为ROCA的新型三位一体纳米调节剂,展现出强大的肿瘤表观遗传调控和免疫微环境重编程能力,为癌症表观遗传免疫疗法开辟了新的道路。相关工作以“Triune Nanomodulator Enables Exhausted Cytotoxic T Lymphocyte Rejuvenation for Cancer Epigenetic Immunotherapy”为题发表在国际材料领域顶级期刊《ACS Nano》上,四川大学何斌研究员/蒲雨吉副研究员为共同通讯作者,李君花博士为第一作者。

ROCA纳米调节剂的设计理念是通过使用一种新型的DNA甲基化抑制剂奥沙拉嗪(Olsa)和铜离子(Cu2+)作为基本单元构筑纳米级金属有机框架,通过自组装形成具有肿瘤靶向肽(cRGD)修饰的纳米聚集体,同时可实现免疫原性细胞死亡(ICD)诱导剂阿霉素(ADM)的装载(图1)。该三位一体纳米调节剂集表观遗传调控、级联催化反应和免疫原性细胞死亡诱导功能为一身,能够在肿瘤微环境中特异性释放活性因子,通过逆转DNA高甲基化来重编程肿瘤微环境,抑制癌基因MYC的表达,并启动1型辅助T细胞(TH1)趋化因子轴。这一过程与ICD诱导相结合,从根本上增强了肿瘤内耗竭的细胞毒性T淋巴细胞(CTLs,CD8+ T细胞)的再生,展现出强大的癌症表观遗传免疫治疗效果。同时,该纳米调节剂可与抗PD-L1免疫检查点阻断协同作用,进一步显著增强抗肿瘤免疫反应。此外,该策略还建立了长期免疫记忆,有效预防了原位结肠癌的复发。研究人员表示,ROCA纳米调节剂不仅有望成为单一的表观遗传免疫疗法制剂,而且还可以与免疫检查点抑制剂联合治疗,扩大了癌症免疫疗法的组合策略。
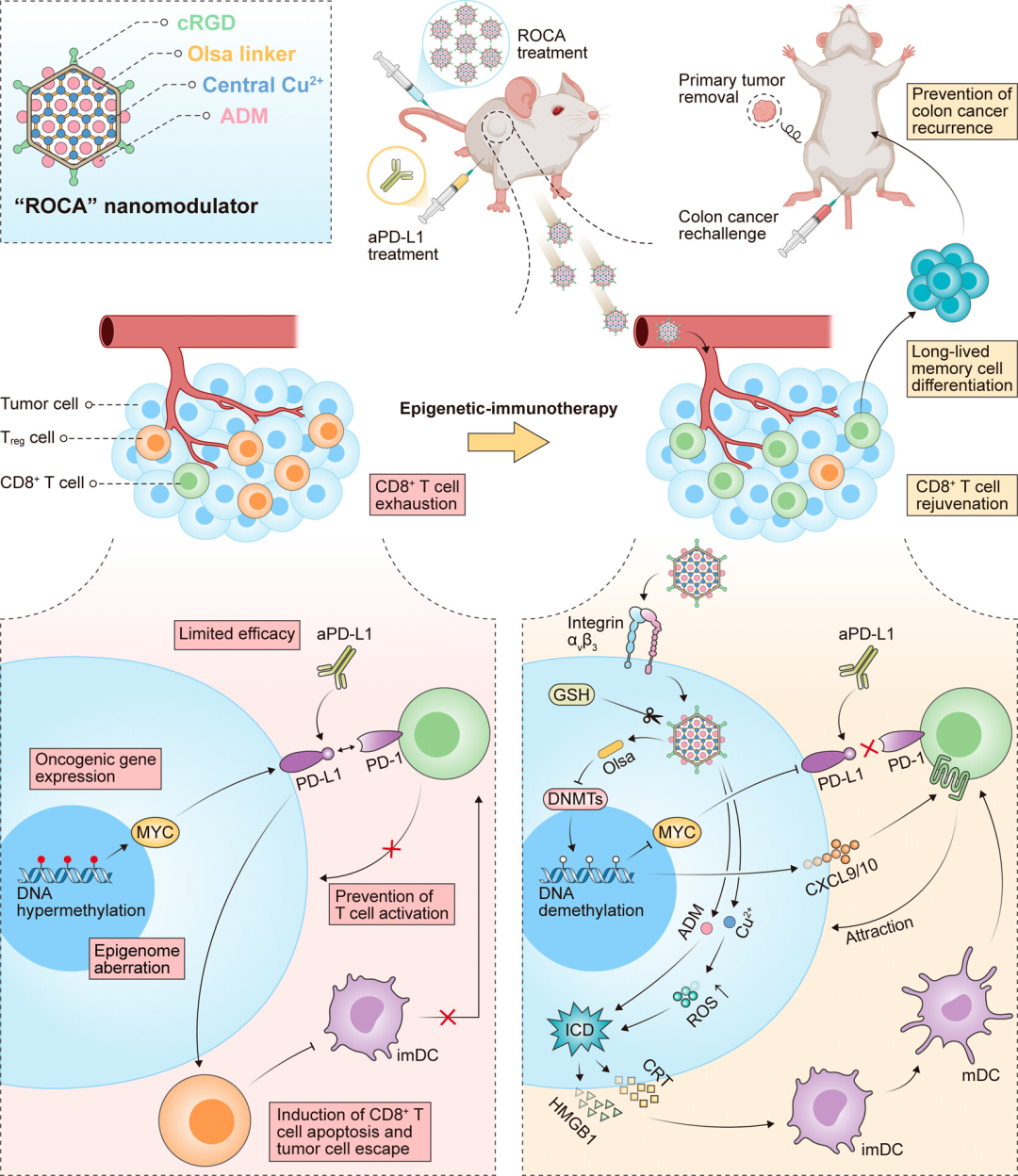
图1. ROCA纳米调节剂及其通过肿瘤微环境重编程进行表观遗传免疫治疗的机制
该研究得到了国家自然科学基金、四川大学“医学+材料”中心医工融合创新项目、四川省科技厅和江苏省卓越博士后计划项目的支持。
参考文献:
Triune Nanomodulator Enables Exhausted Cytotoxic T Lymphocyte Rejuvenation for Cancer Epigenetic Immunotherapy. Junhua Li, Quan Zhao, Nan Zhang, Lihuang Wu, Qiusheng Wang, Jing Li, Qingqing Pan, Yuji Pu, Kui Luo, Zhongwei Gu, and Bin He. ACS Nano Article ASAP
原文链接:
https://doi.org/10.1021/acsnano.4c02337
浦侃裔最新AM: 可抑制外泌体的聚合声敏剂用于肿瘤特异性声动力学免疫疗法
![]() 0
2024-03-10
点击查看
0
2024-03-10
点击查看

浙江大学平渊教授《自然·通讯》: 可热诱导工程化巨噬细胞的促炎极化可在免疫疗法期间重塑肿瘤免疫微环境
![]() 0
2024-04-01
点击查看
0
2024-04-01
点击查看

Allergy:鼻腔过敏原中和抗体与可耐受的鼻内过敏原挑战剂量有何关系?
![]() 0
2024-04-04
点击查看
0
2024-04-04
点击查看
专访美国哈佛医学院的吴博士:癌症个性化疫苗什么时候可以盼到?
![]() 0
2024-04-27
点击查看
0
2024-04-27
点击查看
PD-1 vs PD-L1抑制剂:差异何在?揭秘免疫疗法新篇章!
![]() 0
2024-04-25
点击查看
0
2024-04-25
点击查看

Cancer Med:BCMA CAR-T细胞参与治疗多发性骨髓瘤的有效性和感染并发症——来自瑞典的真实世界证据
![]() 0
2024-04-27
点击查看
0
2024-04-27
点击查看
