1、NA + Peg-IFN α-2b + GMCSF联合方案
Anchor A研究期中分析:应用NA + Peg-IFN α-2b + GMCSF联合治疗方案可以增加NA经治慢乙肝患者的HBsAb产生率
粒细胞-巨噬细胞集落刺激因子(GMCSF)对机体的免疫应答具有多种效应,之前用作乙肝疫苗的佐剂,以增强抗体应答。在本届APASL年会上,我国华中科技大学同济医学院附属同济医院宁琴教授等投稿公布了研究团队联合国内多家中心完成的随机对照试验(NCT02327416)结果:
对于应用核苷(酸)类似物(NA)治疗后获得病毒学抑制的慢性乙型肝炎(CHB)患者,联合应用恩替卡韦(ETV)+聚乙二醇干扰素α-2b(Peg-IFN α-2b)± GMCSF治疗,可以显著提高HBsAg清除/血清学转换率;在丙氨酸氨基转移酶(ALT)水平正常或轻度升高的亚组患者中,加用GMCSF治疗,可以增强Peg-IFN α-2b在提高HBsAb阳性率方面的治疗效果(Abstract #341)。
该项多中心研究中,将249例应用NA治疗>1年、HBsAg水平<3000 IU/mL且HBV DNA水平≤1000 copies/mL的CHB患者,按照1:1:1的比例,进行随机分组,81例患者接受ETV治疗96周(Ⅰ组),83例患者接受ETV治疗48周+ Peg-IFN a-2b(180 μg/周)治疗96周(Ⅱ组),85例患者接受ETV+间断应用GMCSF治疗(75 μg/d,每个月最初5天用药)48周+ Peg-IFNα-2b治疗96周(Ⅲ组),分析三组患者的中期数据,对联合应用NA+ Peg-IFN α-2b+GMCSF治疗,是否可以诱导HBsAg清除/血清学转换进行评估。
结果,三组患者的基线特征具有可比性。96周时,接受三联治疗(NA+ Peg-IFN+ GMCSF)的Ⅲ组患者和接受二联治疗(NA+ Peg-IFN)的Ⅱ组患者与继续应用NA单药治疗的Ⅰ组患者相比,获得的HBsAg清除率显著较高(分别为19.40%、31.34%和0%,Ⅲ组、Ⅱ组和Ⅰ组相比,P值均< 0.001),Ⅲ组和Ⅱ组的HBsAg清除率差异无统计学意义(P=0.527)。Ⅲ组和Ⅱ组的HBsAb产生(≥ 10 IU/mL)率显著高于Ⅰ组(分别为32.76%、34.43%和0%,Ⅲ组、Ⅱ组和Ⅰ组相比,P值均< 0.001),只有Ⅲ组和Ⅱ组观察到HBsAg血清学转换(分别为20.69%和27.87%,P=0.3619)。
开始Peg-IFN治疗后12周时,Ⅲ组中的58例患者和Ⅱ组中的47例患者ALT正常或轻度升高[<2倍正常值上限(2×ULN)],在这些亚组患者中,三联治疗所诱导的HBsAb阳性率显著高于二联治疗者(96周时,分别为48.28%和29.79%),两组间的差异为18.49%(95% CI:0.15%~36.83%),具有统计学意义。此外,第96周时,Ⅲ组的HBsAb>100 IU/L率在数字上高于Ⅱ组(分别为17.24%和8.51%,P=0.19)。二联和三联治疗方案的总体耐受性均良好。
2、TLR8激动剂 Selgantolimod(GS-9688)
多中心、随机、双盲、安慰剂对照Ⅱ期研究:病毒学抑制成人慢乙肝患者口服TLR8激动剂Selgantolimod(GS-9688)治疗24周的安全性和效果
Selgantolimod是一种口服小分子Toll样受体8激动剂,研发用于治疗慢性乙型肝炎(CHB)。在本届APASL年会上,新西兰奥克兰大学Gane教授等报告了CHB患者应用Selgantolimod治疗的多中心、随机、双盲2期研究结果:
经口服抗病毒治疗病毒学得到抑制的CHB患者口服Selgantolimod治疗,安全耐受性良好,可引起剂量依赖性的药效动力学变化,至24周时,5%的患者达到HBsAg水平下降≥1 log IU/mL或HBsAg清除。正在对至48周时的免疫学、抗病毒和药效动力学进行评估(Abstract #431)。
该项研究中,48例经口服抗病毒治疗,病毒学得到抑制的患者纳入HBeAg阳性和阴性2个队列,按照2:2:1的比例,将患者随机分组,应用Selgantolimod 3.0 mg/次、1.5 mg/次或安慰剂,每周一次,治疗24周。安全性评估包括监测不良事件和实验室异常,主要疗效终点为从基线至24周时,HBsAg水平下降≥1 log IU/mL的患者比例,次要终点包括HBsAg清除和HBeAg清除的患者比例以及药效动力学、IL-1RA和IL-12p40的变化,对经口服抗病毒治疗病毒学抑制CHB患者应用Selgantolimod治疗的安全性和效果进行评估。
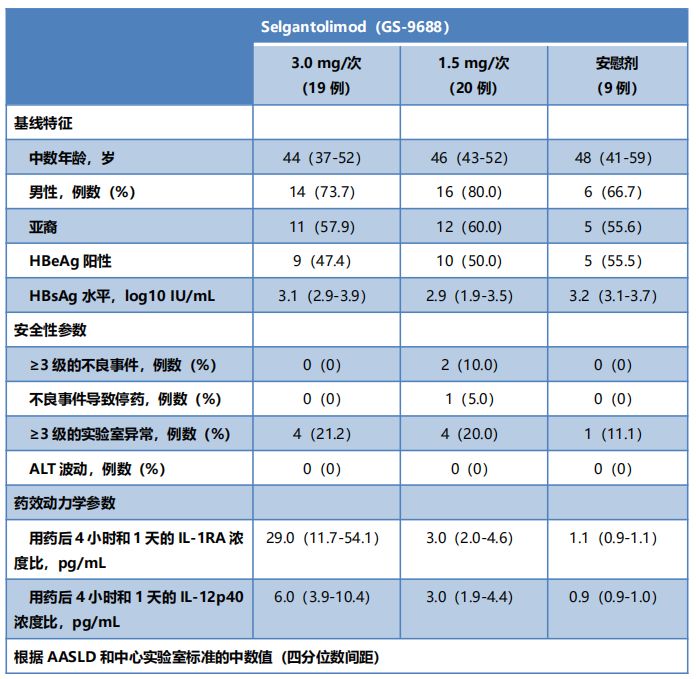
结果,各组患者的基线特征相似(表1),应用Selgantolimod 3.0 mg/次、1.5 mg/次或安慰剂治疗的患者分别有0%、10%和0%观察到≥3级的不良事件,没有观察到快速抗药反应。至24周时,1例应用Selgantolimod 1.5 mg/次治疗的HBeAg阴性患者达到HBsAg水平下降≥1 log IU/mL的主要终点,1例应用Selgantolimod 3.0 mg/次治疗的HBeAg阴性患者达到HBsAg清除,1例应用Selgantolimod 1.5 mg/次治疗的HBeAg阳性患者达到HBeAg清除。Selgantolimod治疗组观察到剂量依赖性的IL-1RA和IL-12p40升高。
表1. 患者的基线特征、安全性参数和药效动力学参数
3、反义寡核苷酸 GSK836
2a期随机、双盲、安慰剂对照研究:GSK836治疗可以使慢乙肝初治患者的HBsAg水平下降
GSK3228836或GSK836之前称为ISIS 505358,是一种针对所有HBV RNA的2´-MOE修饰反义寡核苷酸。在本届APASL年会上,我国香港大学玛丽医院袁孟峰教授等投稿公布了慢性乙型肝炎(CHB)初治患者应用GSK836治疗4周的研究结果:
对HBsAg和HBV DNA具有显著的抑制作用,安全耐受性良好,适合更长疗程的继续治疗(Abstract #510)。
该项2a期随机、双盲、安慰剂对照研究纳入HBV DNA≥2×103 IU/mL、HBsAg≥50 IU/mL的HBeAg阳性或阴性CHB初治患者,排除有肝硬化、同时合并HCV、HIV或HDV感染或者丙氨酸氨基转移酶(ALT)或天门冬氨酸氨基转移酶(AST)>5倍正常值上限(×ULN)的患者,第1、4、8、11、15和22天,皮下注射GSK836,300 mg/次,第29天时评估抗病毒的效果,对GSK836的抗病毒作用和安全性进行评估。
结果,GSK836治疗组(12例)和安慰剂组(6例)相比,自基线的HBsAg水平变化分别为-1.556±1.379(P=0.001)和0.000±0.112 log IU/mL,自基线的HBV DNA水平变化分别为-1.655±1.479(P<0.001)和-0.001±0.471 log IU/mL。3例患者的HBsAg水平下降>3.0 log IU/mL,其中2例患者的HBsAg水平降至低于定量检测的下限(LLoQ,0.05 IU/mL),4例患者的HBV DNA水平下降>3.0 log IU/mL,其中1例患者的HBV DNA水平降至
GSK836治疗组有1例患者发生严重不良事件,1例HBsAg和HBV DNA水平降至
4、基于RNA干扰的三联方案
基于RNA干扰的三联方案治疗慢乙肝的第一项临床研究:JNJ-3989 + JNJ-6379 +核苷(酸)类似物安全有效
在AROHBV1001研究中,慢性乙型肝炎(CHB)患者联合应用JNJ-3989 RNA干扰(RNAi)和核苷(酸)类似物(NA)治疗,具有叠加/协同抗病毒作用,并且耐受性良好。应用限定疗程的JNJ-3989 + JNJ-6379[N类衣壳组装调节剂(CAM-N)] + NA三联治疗方案,有望提高患者的功能性治愈率。
在本届APASL年会上,我国香港大学玛丽医院袁孟峰教授等投稿公布了AROHBV1001研究附加队列中,CHB患者应用JNJ-3989 + JNJ-6379 + NA三联治疗方案的研究结果:患者对三联治疗的耐受性良好,HBsAg定量水平和其他病毒学参数均有大幅下降(Abstract #763)。
12例CHB患者接受3剂JNJ-3989治疗(第1天、第29天和第57天,皮下注射200 mg)+口服JNJ-6379(250 mg QD)治疗12周,继续NA治疗,定期对HBsAg、HBeAg、HBV DNA、HBV RNA和HBV核心相关抗原(HBcrAg)水平进行定量检测。计划随访1年,对三联治疗方案的效果和安全性进行评估。
结果,所有12例患者均为亚裔,包括4例HBeAg阳性和8例HBeAg阴性患者,其中7例为NA经治患者,中数年龄为46岁,8例男性接受根据计划的JNJ-3989和JNJ-6379所有用药,随访17~64天。没有发生死亡、中止治疗、重度/严重不良事件或临床显著的生命体征/实验室异常,报告2例不良事件(轻度呼吸道感染,与治疗无关)。

图1 治疗期间的病毒学指标变化
治疗期间的病毒学指标变化如图1所示。第85天和第113天,HBsAg水平分别下降1.4 ± 0.12 log IU/mL(12例)和1.8± 0.11 log IU/mL(7例);第1天HBV DNA水平>1000 IU/mL的所有6例患者(3.7~7.7 log IU/mL)均达到HBV DNA快速下降,9例患者有HBV RNA定量检测结果(第1天,1.75~7.5 log1IU/mL);第29天时,6例患者的HBV RNA降至低于检出限。第1天时HBeAg阳性(4例)和HBcrAg阳性(8例)患者的HBeAg和HBcrAg水平均有下降。
5、JNJ-3989 RNAi+ NA联合方案
联合应用核苷(酸)类似物 + JNJ-3989 RNAi治疗慢乙肝患者的剂量效应
JNJ-3989可以沉默来自游离cccDNA和整合HBV DNA的HBV RNA转录,AROHBV1001 2a期研究表明,应用JNJ-3989和核苷(酸)类似物(NA)治疗,可以使HBsAg水平下降≥1 log IU/mL,使可检测的病毒产物下降,耐受性良好。在本届APASL年会上,新西兰Gane教授等研究人员报告了扩大100~400 mg JNJ-3989队列,并且增加2个较低剂量(25和50 mg)队列的研究结果:
CHB患者应用3剂JNJ-3989(剂量范围为25~400 mg,每个月一次),联合NA治疗的耐受性良好,应用100~400 mg的JNJ-3989治疗,97%(31/32)的患者达到HBsAg水平下降≥1.0 log IU/mL,25 mg和50 mg剂量的JNJ-3989也有效果,但是,不如较高剂量有效(Abstract #777)。
研究纳入NA经治或初治的HBeAg阳性或阴性CHB患者,接受3剂JNJ-3989皮下注射(第1、27和57天时,25、50、100、200、300和400 mg),患者开始应用或继续应用NA治疗(第1天),并且整个研究期间继续应用NA,对JNJ-3989 + NA联合治疗的安全性以及HBsAg、HBeAg、HBV DNA、HBV RNA和HBV核心相关抗原(HBcrAg)等病毒学参数进行评估。
结果,没有患者中断治疗或发生药物相关的严重不良事件。第113天时(应用3剂JNJ-3989后的典型平均最低点,最后一次用药后第56天),自第1天(8例)的HBsAg水平下降分别为1.00 ± 0.18 log10 IU/mL(25 mg)、1.18 ± 0.08 log10 IU/mL(50 mg)、1.54 ± 0.18 log10 IU/mL(100 mg)、1.77 ± 0.18 log10 IU/mL(200 mg,7例)、1.48 ± 0.11 log10 IU/mL(300 mg)和1.75 ± 0.16 log10 IU/mL(400 mg)(图2)。
4/8(25 mg)、5/8(50 mg)、7/8(100 mg)、8/8(200 mg)、8/8(300 mg)和8/8(400 mg)例患者的HBsAg水平达到从第1天至最低点下降≥1.0 log10 IU/mL。对于HBsAg水平>100 IU/mL(第1天)的患者,第113天时,2/7(25 mg)、3/8(50 mg)、5/7(100 mg)、6/6(200 mg)、6/8(300 mg)和5/7(400 mg)例患者达到HBsAg水平<100 IU/mL。治疗患者的HBV DNA、HBV RNA、HBeAg和HBcrAg水平均有下降。
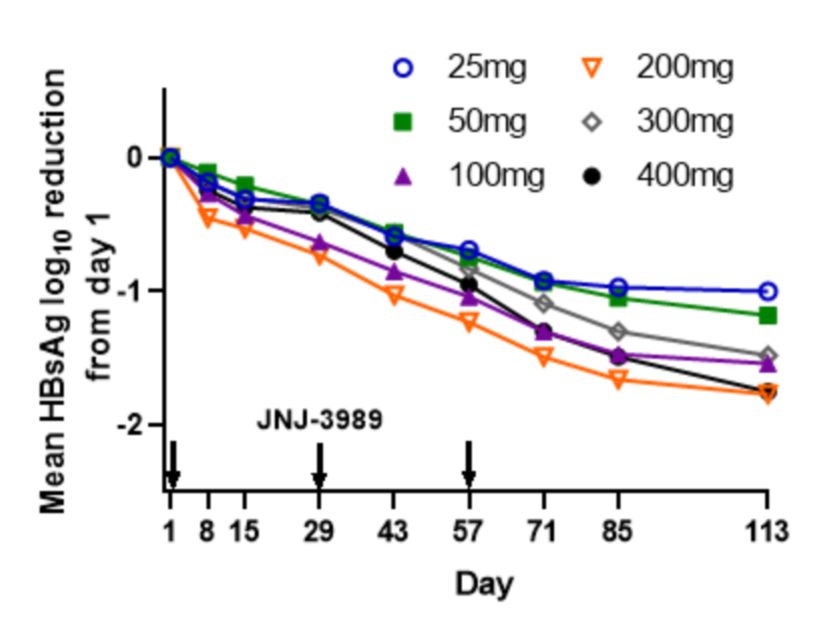
图2 HBsAg水平水平变化