衰老是一个复杂的生物过程,伴随着生理功能的下降,导致疾病和死亡的易感性增加。确定生理衰老转变为病理疾病状态的时机为在临床症状发作之前改变疾病结果提供了一个合适的药理学窗口。生物标志物越来越普遍地用于了解随着年龄和疾病发作而发生的生理过程。生物标志物是存在于血液、体液和组织中的分子,可以通过定量测量直接评估疾病的发作或进展。
本文的重点是讨论谷氨酸能调节与衰老和阿尔滋海默病(AD)相关的变化。谷氨酸是中枢神经系统中最丰富的神经递质,谷氨酸受体存在于大部分神经元和突触上。谷氨酸稳态对于健康老龄化和降低各种神经系统疾病的风险至关重要,包括癫痫、成瘾、肌萎缩性侧索硬化症、帕金森病、阿尔滋海默病(AD)等。生理上,谷氨酸在突触稳定性和可塑性中起着关键作用,包含谷氨酸神经传递的功能元件是突触前和突触后神经元以及神经胶质细胞,被共同定义为“三联突触”。

南伊利诺伊大学医学院神经科学研究所的研究者回顾了衰老和AD小鼠模型的研究结果,并为这种表型转变提供了生物学背景。最后,重点介绍了当前监测脑谷氨酸的技术。这些技术可能有助于阐明特定时间点的治疗窗口以改变疾病结果。
研究结果
1、生理老化
衰老是生理过程的自然衰退,会在所有生物体的整个生命周期中改变各种生化途径。运动、新陈代谢、炎症和执行功能的生理衰退很普遍,并且因个体和性别而异。衰老也会影响大脑的结构和功能完整性,从而导致这些生理衰退。
2、阿尔滋海默病患者谷氨酸失调
Aβ或过度磷酸化的tau有助于神经元兴奋性,从而促进过度兴奋,进而导致谷氨酸能兴奋性毒性。NMDA(谷氨酸受体)的持续过度激活会扰乱对生理信号的识别,从而影响记忆巩固和回忆。突触前,可溶性 Aβ 在早期阶段优先结合 VGLUT1,从而增强释放特性。虽然在死后脑组织的后期阶段发现 VGLUT1 水平降低。mGluR2在海马锥体神经元中的表达增加,并与死后AD组织中的过度磷酸化tau沉积相关。
在阿尔滋海默病动物模型中也存在谷氨酸失调。APP/PS1 小鼠中的海马基础和刺激诱发的谷氨酸信号在认知下降开始之前以亚区域特异性方式变得过度活跃,第一个变化出现在 CA1 中,其中刺激诱发的谷氨酸释放在 3 个月大时显着升高。在6个月时,当海马斑块开始积累时,整个海马体的基础谷氨酸含量升高,并随着年龄的增长而继续增加。在这个年龄,DG 中的谷氨酸释放也会增加,并在整个疾病进展过程中保持升高。CA3 诱发的谷氨酸释放直到12个月大时才会升高,此时斑块积聚更加突出。到12个月时,APP/PS1小鼠海马的所有区域都会出现高谷氨酸能信号。
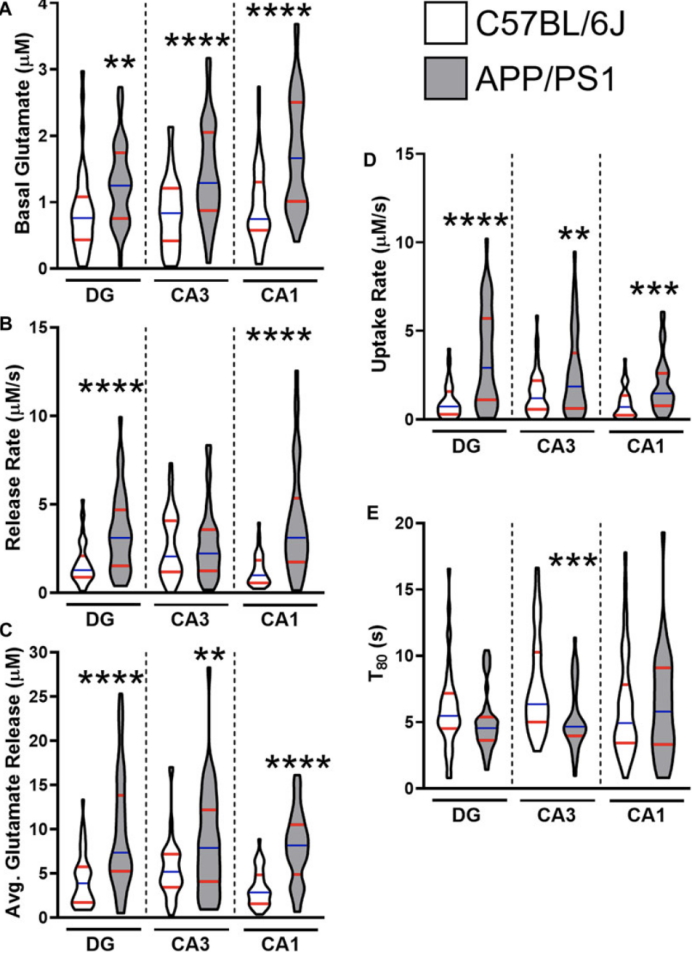
图1 APP/PS1 和 C57BL/6J 小鼠 12 个月时的谷氨酸动力学
3、体外谷氨酸检测的诊断方法
越来越多的证据支持调节谷氨酸能信号作为 AD 治疗的重要性。因此,需要监测谷氨酸从生理信号转变为病理信号的方法。通过脑脊液 (CSF)测量淀粉样蛋白和 tau 的沉积,同时通过神经丝轻链确定神经元损失。通过分析AD患者的脑脊液中的谷氨酸,表明与健康衰老的人相比,谷氨酸存在增加或减少的现象,这些不一致的结果可能反应了AD个体连续性的病理进展。
取脑脊液对患者创伤较大,需要腰椎穿刺,通常会留下脊髓性头痛等后遗症。目前正在探索先进的神经影像学技术检测健康老龄化、轻度认知障碍和AD患者中谷氨酸和谷氨酸受体的变化。成像提供了检测大脑内代谢功能变化和监测整个衰老过程中结构转变的潜力。正电子发射断层扫描 (PET) 成像可与多个放射性示踪剂一起使用,以定量评估突触密度。磁共振 (MR) 使用磁场来创建大脑的 3D 图像,而无需电离辐射或放射性示踪剂,与 PET 成像不同,MR 无法直接测量神经活动。
通过数十年的谷氨酸生物学研究积累,该系统有望在神经系统疾病领域取得重大进展。作者的实验室已经展示了使用谷氨酸作为生物标志物来确定生理和病理衰老之间的潜力。使用微创和无创技术的进步允许纵向监测谷氨酸水平的区域变化。这些方法有可能提供依赖于疾病状态的治疗干预,以改善患者的预后。
原文链接:https://www.frontiersin.org/articles/10.3389/fragi.2022.929474/full?utm_source=BN-AT03&utm_medium=wechat&utm_campaign=chinaad
参考文献
Cox MF, Hascup ER, Bartke A and Hascup KN (2022) Friend or Foe? Defining the Role of Glutamate in Aging and Alzheimer’s Disease. Front. Aging 3:929474. doi: 10.3389/fragi.2022.929474
校审: Simon (Brainnews编辑部)