三阴性乳腺癌(triple-negative breast cancer,TNBC)是乳腺癌的一种分型,患者的癌组织的免疫组织化学检查结果表现为雌激素受体(ER)、孕激素受体(PR)和原癌基因人表皮生长因子受体(HER2)的表达均为阴性,其约占所有乳腺癌类型的15%-20%。TNBC临床表现为较具侵袭性的病理特征,包括较高的复发率、对化疗药物的耐药性、确诊时较频繁的远端转移和较差的预后等特点。

(图片来源:百度图片)
目前对于早期TNBC最有效的化疗组合包括蒽环类、紫杉烷类和/或铂类药物的治疗,而新辅助化疗模式(NAC)也为临床上的病理完全缓解(pCR)提供重要的预后信息,且在许多临床试验(尤其是TNBC)中被视为替代终点。与pCR的患者相比,在新辅助化疗后仍残留浸润性疾病的患者具有较高的早期复发风险和更差的预后。
本文主要汇总了2020年美国临床肿瘤学会(ASCO)年会中发布的包括卡培他滨(capecitabine)和奥拉帕尼(Olaparib)等部分靶向药对于治疗三阴性乳腺癌(TNBC)的最新研究进展。
(图片来源:百度图片)
之前的研究显示,卡培他滨(capecitabine)能够用于残余癌的辅助治疗,在CREATE-X临床试验中,卡培他滨的辅助治疗可以提高TNBC患者的5年无病生存率。
近期中山大学肿瘤防治中心王曦团队的研究发现使用卡培他滨进行持续一年的维持治疗可以显著改善可手术三阴性乳腺癌患者的无病生存率。
研究人员将总共434例可手术TNBC患者随机分成两组,分别是卡培他滨组(n=221)和观察组(n=213)。实验组给予维持剂量的卡培他滨(650mg/m2,每日两次,连续给药一年)进行维持治疗。第56.5个月的随访中位时间显示,卡培他滨组的5年无病生存率(DFS)显著高于观察组(83%vs. 73%,p = 0.027)。5年无远处疾病生存率(DDFS)也显著高于观察组(85%vs. 76%,p = 0.016)。然而两组的5年总生存率(OS)无显著的统计学差异(85%vs. 81%,p = 0.203)。202名患者(91.4%)按计划完成了卡培他滨的一年治疗。该研究也表明了卡培他滨的维持治疗是一种安全且耐受性良好的治疗策略,其可以显著改善可手术三阴性乳腺癌患者的无病生存率。
韩国高丽大学医学院同样发布了一项相关的II期临床试验,该试验目的在于评估新辅助治疗后的具有残留浸润性癌的三阴性乳腺癌(TNBC)患者在采取阿特朱单抗(一种抗PD-L1抗体)与卡培他滨的联合辅助治疗以及卡培他滨单药治疗后的疗效和安全性。该试验将招募韩国15个地区的284名患者,主要目标在于获得患者的5年无侵袭性疾病生存率(IDFS)。次要目标包括PD-L1阳性人群的5年IDFS,无远处复发生存率(DRFS),总生存率(OS)以及用药的安全性等数据。研究人员对于招募对象设立了相关的采纳和排除标准,目前该研究已募集13名患者。
之前的临床研究表明,TNBC细胞系和小鼠模型对PARP1抑制剂更为敏感,该研究结果为开发针对TNBC的新型疗法提供了有力的依据。奥拉帕尼(Olaparib)作为一种PARP抑制剂,目前已被批准用于BRCA1/2突变和HER2阴性的转移性乳腺癌临床治疗。
法国巴黎居里研究所开展了奥拉帕尼结合放射性治疗(RT)的I期临床研究,研究对象为具有炎症反应、局部晚期或转移性三阴性乳腺癌(TNBC)患者或手术后具有残留癌的TNBC患者。
该研究的目的旨在研究局部放射性治疗结合奥拉帕尼给药的最大耐受剂量(MTD)以及评估剂量限制毒性(DLT)。
研究结果显示,奥拉帕尼的最大耐受剂量能够提高至200 mgx2的目标剂量且未出现剂量限制性毒性,而患者的晚期毒性研究则需要进一步的随访。

表一 患者相关临床信息
美国波士顿哈佛医学院下的贝斯以色列女执事医疗中心和丹娜法伯癌症研究院的II期临床研究探讨了奥拉帕尼单药治疗转移性乳腺癌患者的治疗效果,招募患者在DNA损伤反应(DDR)通路基因上存在遗传上或体细胞突变。
招募的患者分为两个队列,一是除BRCA1/2外的DDR途径基因的遗传性突变患者队列,二是包含BRCA1/2在内的DDR途径基因体细胞突变的患者队列,在2018年3月至2020年1月期间研究人员共招募了符合要求的患者53例,患者的年龄中位数为59岁(覆盖范围为30-87岁)。招募的患者接受每日两次的300 mg的奥拉帕尼治疗直至疾病出现恶化或出现药物剂量毒性。
迄今为止,经过长达16.4个月的临床观察,在两个队列中奥拉帕尼单药治疗的测试均成功到达主要终点。
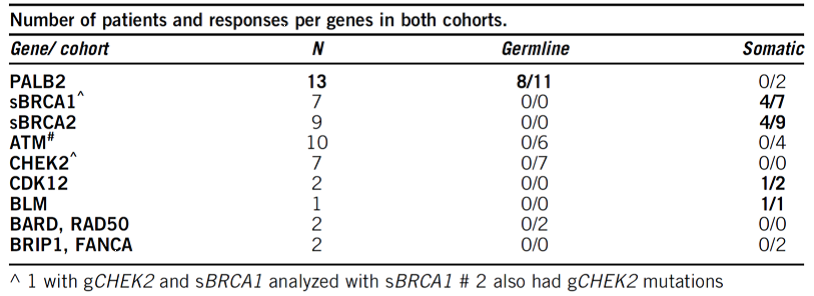
表二 两个队列中患者信息汇总
美国耶鲁大学医学院发布了关于三阴性乳腺癌队列II期研究的初步治疗数据,该研究旨在探讨在晚期实体瘤中西地尼布联合奥拉帕尼的治疗效果。
西地尼布是一种VEGF(血管内皮生长因子)受体抑制剂,其能够抑制BRCA1,BRCA2和RAD51的表达水平,且提高肿瘤组织对PARP抑制剂的敏感性。而作为PARP抑制剂的奥拉帕尼已被证实在BRCA1/2突变以及HER2阴性的转移性乳腺癌患者具有一定的临床疗效。该研究旨在测试在转移性三阴性乳腺癌(TNBC)患者中西地尼布联合奥拉帕尼治疗策略的抗肿瘤活性。
该II期临床研究的招募对象为至少接受过一次系统性治疗的晚期转移性TNBC患者。对招募的患者进行每日一次的口服30mg西地尼布以及每日两次的口服200mg奥拉帕尼,给药持续至疾病恶化或出现剂量毒性。
研究结果显示总体客观缓解率为14%,中位缓解时间为2个月,疾病控制率为81%,而其中3/4级不良事件(G3/4 AEs)发生率为66%。5%的患者出现高血压(24%)、呼吸困难(11%)、腹泻(8%)以及呕吐(8%)等症状。该研究显示西地尼布和奥拉帕尼的联合治疗对于14%的招募转移性TNBC患者具有潜在缓解作用,研究人员也提出了在治疗开始时及时使用降压药能够较为有效的控制不良事件的产生。

表三 患者相关信息
目前对于局部复发、无法进行手术的TNBC或转移性TNBC(mTNBC)的较有前景的一线治疗策略为免疫疗法与化疗相结合的治疗方式。
然而针对诱导治疗后的维持性治疗以及长期化疗可能产生的潜在化学毒性或耐药性,有效且可耐受的mTNBC维持方案的制定还有待探索。
加州大学旧金山分校医学中心的海伦迪勒家庭综合癌症中心为探讨该联合治疗策略的效果制定了一项相关的(KEYLYNK-009)II/III期开放性临床研究。
该研究旨在招募局部复发的无法手术或转移性三阴性乳腺癌患者,所有患者将接受长达6个周期的诱导疗法,每3周服用200 mg派姆单抗以及其他化学药物(卡铂AUC 2 和1000 mg/m2的吉西他滨)。经过诱导治疗后的患者将被分为两组,分别实验组接受每3周服用200 mg派姆单抗以及每日两次300mg的奥拉帕尼治疗,对照组延用之前的诱导治疗方案。治疗将持续至疾病恶化或出现药物剂量毒性。
综上研究进展显示,随着对三阴性乳腺癌相关分子机制的越来越多的研究,无论是卡培他滨的辅助治疗还是奥拉帕尼单药治疗以及结合其他药物的联合疗法均为三阴性乳腺癌的治疗提供有意义的研究结果和参考。除了如奥拉帕尼的PARP抑制剂外,HDAC抑制剂、铂类药物、派姆单抗以及新辅助治疗等各类靶向药物的联用或与化学药物联用的个体化治疗方案正越来越多的运用于临床上三阴性乳腺癌患者的治疗中,因此,三阴性乳腺癌的治疗和预后将会逐步的得到改善。
参考文献
1. Phase III trial of metronomic capecitabine maintenance after standard treatment in operable triple-negative breast cancer (SYSUCC-001). First Author: XI Wang, Departments of Breast Oncology, Sun Yat-Sen University Cancer Center, State Key Laboratory of Oncology in South China, Collaborative Innovation Center for Cancer Medicine, Guangzhou, China
2. Randomized, phase II trial to evaluate the efficacy and safety of atezolizumab plus capecitabine adjuvant therapy compared to capecitabine monotherapy for triple receptor-negative breast cancer (TNBC) with residual invasive cancer after neoadjuvant chemotherapy (MIRINAE trial, KCSGBR18- 21). First Author: In Hae Park, Division of Hemato-Oncology, Department of Internal Medicine, Korea University College of Medicine, Guro Hospital, Seoul, South Korea
3. Radioparp: A phase I of olaparib with radiation therapy (RT) in patients with inflammatory, locoregionally advanced or metastatic triple-negative breast cancer (TNBC) or patient with operated TNBC with residual disease— Preliminary results. First Author: Youlia M. Kirova, Institut Curie, Paris, France
4. TBCRC 048: A phase II study of olaparib monotherapy in metastatic breast cancer patients with germline or somatic mutations in DNA damage response (DDR) pathway genes (Olaparib Expanded). First Author: Nadine M. Tung, Beth Israel Deaconess Medical Center and Dana-Farber Cancer Institute, Boston, MA
5. Preliminary efficacy data of triple-negative breast cancer cohort of NCI 9881 study: A phase II study of cediranib in combination with olaparib in advanced solid tumors. First Author: Navid Hafez, Yale University School of Medicine, New Haven, CT
6. KEYLYNK-009: A phase II/III, open-label, randomized study of pembrolizumab (pembro) plus olaparib vs pembro plus chemotherapy after induction with first-line pembro plus chemotherapy in patients with locally recurrent inoperable or metastatic triple-negative breast cancer (TNBC). First Author: Hope S. Rugo, University of California San Francisco , San Francisco, CA