新型冠状病毒肺炎(COVID-19)是由冠状病毒SARS-CoV-2引起的大流行性疾病,随着病毒的传播,迄今为止COVID-19病死率约在1%~5%之间。先前有研究表明,在中国的COVID-19患者合并高血压发生不良预后的风险可能会增加,高血压患者的死亡率危险比(HR)为1.70(95%CI 0.92–3.14)~3.05(95%CI 1.57–5.92)。然而这些前期工作并未排除混杂因素,例如年龄,而年龄恰是COVID-19相关的死亡预测因子。
SARS-CoV-2通过血管紧张素转换酶2(ACE2)受体进入人体细胞,ACE2在人体中广泛表达。血管紧张素转换酶抑制剂(ACEIs)和血管紧张素受体阻断剂(ARB)是两种肾素-血管紧张素-醛固酮系统(RAAS)抑制剂可用于治疗高血压和心脏、肾功能衰竭。动物模型及人体中的报告表明,ACEI或ARB治疗后ACE2的表达可能会增加,因此或可增加机体对病毒进入宿主细胞后繁殖的敏感性[1]。尽管ACEI或ARB对人类ACE2的影响尚无定论,但这项研究已引起越来越多的关注,即ACEI或ARB可能会增加(或降低)COVID-19患者的死亡率。
2020年6月4日,中国西京医院的研究人员在《European Heart Journal》杂志上发表了一项回顾性观察研究,他们通过对火神山医院收治的所有COVID-19患者进行回顾性观察研究,根据感染前的病史或所用药物对高血压和治疗进行分层,发现高血压及降压治疗与COVID-19死亡率有关联,并对高血压与降压治疗对COVID-19患者的预后之间的联系进行了详细阐述[2]。
图1: doi:10.1093/eurheartj/ehaa433
研究方法及研究对象
这项回顾性观察性研究,比较了因COVID-19住院的患者中高血压状态和降压治疗类别与死亡率之间的关系。研究纳入了从2020年2月5日至2020年3月15日在中国武汉市火神山医院住院的所有患者,在2877例住院患者中,共有29.5%(850/2877)的患者有高血压病史。
本项研究的主要终点是住院期间的全因死亡率,其他重点包括症状发作与出院之间的时间、有创机械通气的使用率以及COVID-19症状的严重程度。图2显示本项研究的主要流程及操作步骤。
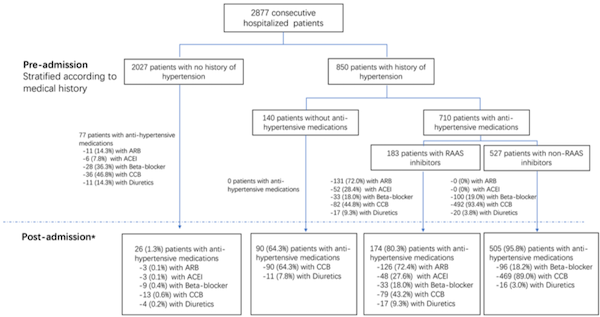
图2: 研究主要流程图
研究结果
1、高血压患者倾向于发展为重症COVID-19疾病
此项研究共纳入2877例确诊COVID-19的连续住院患者。从症状发作到出院(最后一次随访)的中位时间为39(30-50)天。与无高血压的患者相比,患有高血压的患者年龄更大,且过往有糖尿病、心绞痛、中风、肾衰竭或血运重建(PCI或CABG)史,并且接受了更多的糖尿病和高血压药物治疗。
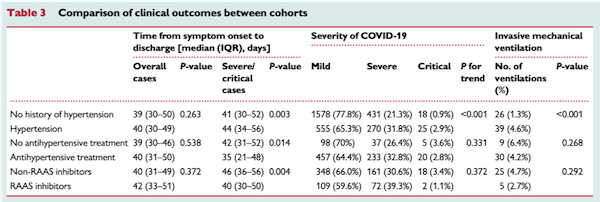
观察结果显示,共有34/850(4.0%)的患者在高血压队列中死亡,22/2027(1.1%)的患者在无高血压队列中死亡(HR 3.75,95%CI 2.19–6.41,P <0.001)。调整混杂因素后,与无高血压相比,高血压仍使死亡风险增加两倍(校正后的HR 2.12,95%CI 1.17-3.82,P = 0.013)。两组患者从症状发作到出院的时间相当。但是,高血压患者倾向于发展为重症COVID-19疾病(P<0.001),并且更有可能接受有创机械通气(P<0.001)(表1)。
表1: 两个队列之间临床结果的比较
2、不同队列患者死亡率比较
然而研究发现,未接受抗高血压治疗的患者(11/140)的死亡率显着高于接受降压治疗(23/710)的患者的死亡率(7.9%:3.2%,HR 2.52,95%CI 1.23–5.17,P=0.012);混杂因素调整后,未进行降压治疗的患者的死亡风险仍然更高(HR 2.17,95%CI 1.03–4.57,P = 0.041)。
接受降压治疗对患者中,有183例(25.7%)的患者接受过RAAS抑制剂治疗,有527例(74.2%)的患者接受了β-受体阻滞剂、CCB或利尿剂(非RAAS抑制剂)治疗。调整前后,RAAS抑制剂组和非RAAS抑制剂组之间死亡率的数值差异无统计学意义(2.2%vs. 3.6%,校正后HR 0.85,95%CI 0.28–2.58,P = 0.774)。两组患者从症状发作到出院的时间,COVID-19的严重程度和通气百分比均相似(图3)。
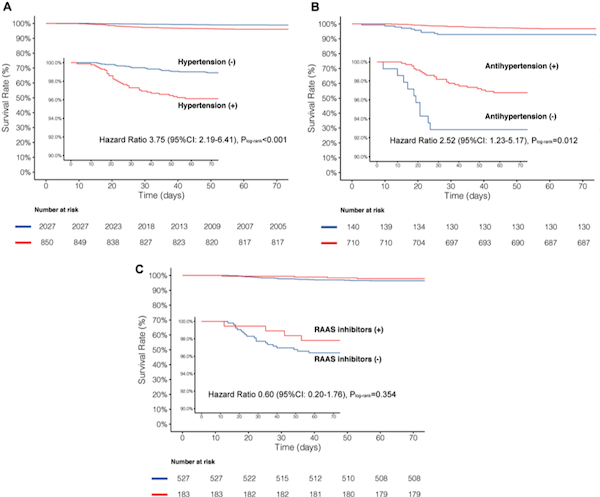
图3: Kaplan–Meier生存曲线从出现症状开始的死亡率。(A)有或无高血压的患者,(B)接受或未接受降压治疗的患者,(C)使用ACEI / ARBs(RAAS抑制剂)或使用β受体阻滞剂、CCB或利尿剂(非RAAS抑制剂)的患者,之间的死亡率比较。
结果讨论
研究人员表示,本项研究主要结论可以概括如下:
(1)在对混杂因素进行调整后,与非高血压患者相比,高血压患者的COVID-19死亡风险相对增加了两倍;
(2)有高血压病史但未接受降压治疗的患者与接受抗高血压治疗的患者相比,死亡风险显着更高;
(3)使用RAAS抑制剂和非RAAS抑制剂治疗的患者之间的相对死亡率、COVID-19的严重程度和通气百分比无统计学差异。然而,在荟萃分析中,RAAS抑制剂往往与较低的死亡风险相关(图4)。

图4: 荟萃分析显示接受RAAS抑制剂和非RAAS抑制剂者的死亡率
迄今为止,仅有少数几项临床证据表明降压治疗可能会影响COVID-19的预后。然而,欧洲心脏病学会高血压委员会(ESC)建议医师和患者应继续采用常规的降压治疗。本项研究表明,与未经高血压治疗的患者相比,入院前接受抗高血压治疗的患者死亡率较低。这些数据支持ESC的建议,指出除非得到医生的指导,否则患者不应中止或改变其降压治疗。
研究局限性
来自西京医院的学者表示,本项研究仍然存在一定的局限性:
1. 为了估计抗高血压药物的真实治疗效果,进行了多变量调整的Cox比例风险模型。但是,观察研究通常存在缺陷,例如无法包括所有相关的混杂因素,尤其是那些无法衡量的混杂因素,从而导致无法调整的偏见。
2. 尽管当前的研究招募了2877名患者,是迄今为止是最大的队列研究之一,然而本项研究仅比较了183例具有RAAS抑制剂的患者和527例具有非RAAS抑制剂的患者。从统计学上讲,研究结果应谨慎使用。
3. 作为一项回顾性研究,由于隔离病房的局限性和遏制COVID-19流行的紧迫性,该研究未详细记录一些数据,如心电图和超声心动图。
4. 这项研究中的数据可以短期评估抗高血压治疗效果的临床结果。仍需要对这些疗法的效果进行长期前瞻性研究。
尽管该项研究存在一定的局限性,但仍可以确定的是COVID-19合并高血压患者不应停止降压治疗。同时荟萃分析也显示,RAAS抑制剂的使用可能与更低的死亡风险相关,然而这仅仅是一项回顾观察性研究,无法证明RAAS抑制剂与COVID-19死亡风险之间存在因果关联,仅发现其相关性,因此未来还需要更多的证据支持本项研究的结论。
参考文献:
1. Wrapp, D.; Wang, N.; Corbett, K.S.; Goldsmith, J.A.; Hsieh, C.L.; Abiona, O.; Graham, B.S.; McLellan, J.S. Cryo-EM structure of the 2019-nCoV spike in the prefusion conformation. Science 2020, 367, 1260-1263, doi:10.1126/science.abb2507.
2. Gao, C.; Cai, Y.; Zhang, K.; Zhou, L.; Zhang, Y.; Zhang, X.; Li, Q.; Li, W.; Yang, S.; Zhao, X., et al. Association of hypertension and antihypertensive treatment with COVID-19 mortality: a retrospective observational study. European Heart Journal 2020, 41, 2058-2066, doi:10.1093/eurheartj/ehaa433.