患者女,61岁。体检B超发现盆腔肿块1周,患者平素自觉偶有腹胀,无明显腹痛,无不规则阴道出血,既往月经规律,量多,绝经11年,无明显痛经史,无子宫肌瘤病史。
专科检查:外阴已产型,阴道畅通、白带淡黄色,宫颈光滑、萎缩,无接触性出血,宫体中位,正常大小,质地中等,盆腔扪及大小约20 cm囊性为主肿物,活动受限,边界清,无明显压痛。
实验室检查:血钙2.05mol/L(2.13~2.54)轻度减低,血常规、尿常规、肝肾功、甲状腺功能全套(三碘甲状腺原氨酸、甲状腺素、游离三碘甲状腺原氨酸、游离甲状腺素、超敏促甲状腺素)、肿瘤六项(甲胎蛋白、癌胚抗原CTA、糖类抗原199、糖类抗原125、糖类抗原153、铁蛋白)均正常。
CT平扫显示盆腔巨大囊实性肿块,边界清晰,部分区域包膜增厚,大小约18.5 cm×14.9 cm×10.5 cm,肿块内囊性密度均匀,无明显分隔,CT值约26HU,其偏右侧后方见实性软组织肿块,大小约7.1 cm×5.5 cm,实性肿块密度不均匀,内伴有斑片状稍低密度,CT值约32~43HU,其旁见环状骨化,有缺口与囊性部分相贯通(图1),增强扫描动脉期肿块内囊性部分无强化,未见明确分隔样强化,实性部分轻度强化,CT值约37~49HU(图2),实质期肿块实质部分进一步轻度强化,CT值约39~59HU,其右侧部分包膜强化(图3),矢状位可观察病灶的全貌,病灶实性部分位于肿块上壁和后壁,环形骨化形态不完整,盆腔内无积液(图4),B超显示盆腔内见19.5 cm×15 cm液性为主团块,边界清晰,团块内见7.0mm×5.8mm稍低回声团块,形态不规则,内未见明显彩色血流(图5)。
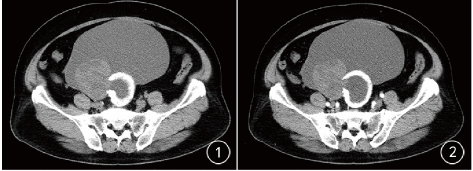
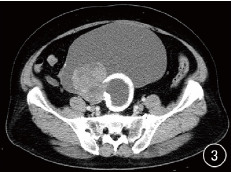
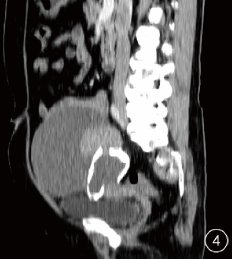
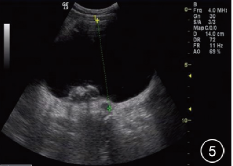
图1 CT平扫示盆腔巨大囊实性肿块,边界清晰,囊性部分密度均匀,偏右侧后方见软组织肿块和环状钙化;图2 动脉期肿块实性部分轻度强化,其内见斑片状坏死区,囊性部分无强化,未见明显分隔;图3 实质期肿块实性部分进一步轻度强化,其右侧部分包膜强化;图4 实质期矢状位重组显示肿瘤实性部分位于肿块上壁和后壁,环形骨化形态不完整;图5 盆腔内液性为主团块,边界清晰,其后方见稍低回声团块,未见明显彩色血流
手术所见:盆腹腔未见明显积液,盆腔内见大小约20.0 cm×16.0 cm×12 cm囊性为主肿块,内可扪及直径约7 cm实质性肉样组织,其偏后下方道格拉斯窝处触及8 cm×9 cm骨骼样坚硬肿块,整个肿瘤包膜完整,表面未见穿破包膜,部分肿瘤包膜与后腹膜、右侧盆壁及部分肠管、阑尾紧密粘连,吸净肿瘤内黄色浑浊色液体,锐性分离肿块,完整取出整个肿瘤,行全子宫切除、双侧附件切除、大网膜切除、阑尾切除及盆腔淋巴结清扫术,参照国际妇产科联盟(FIGO)分期法,临床分期Ic。
巨检:切面实性部分呈灰黄色,部分伴骨样组织。镜检:卵巢上皮成分呈腺样及巢状,细胞异型性明显,胞浆透明,伴斑片状坏死。免疫组织化学:上皮成分,CD15(+),AE1/AE3(+),EMA(+),CA125(+),AFP(-),CD30(-),CD10(-),ER(-),WT-1(-)。诊断:右侧卵巢透明细胞腺癌伴坏死。
讨论
卵巢透明细胞癌(ovarian clear cell carcinoma,OCCC)属于卵巢上皮来源的少见恶性肿瘤,其发生率占卵巢上皮类肿瘤的5%,恶性程度高,对传统以铂类为主的化疗药物不敏感,容易复发,是卵巢上皮性肿瘤预后最差的一个亚型。本病起源于苗勒管的卵巢上皮细胞,与子宫内膜异位症密切相关,多发生于围绝经期妇女,好发年龄48~58岁。病理上呈囊实性肿块,切面多呈鱼肉状或淡黄色,常常伴有坏死,镜下肿瘤细胞胞浆透明,主要由透明细胞、嗜酸细胞、鞋钉细胞构成,细胞间质有基底膜样物质沉积和透明红染小体细胞为特征,10%~30%的肿瘤可伴有微小钙化。免疫组织化学上CA125多为阳性,而Wilm瘤1基因(WT-1)和雌激素受体(ER)表达多呈阴性。
本病临床症状不典型,多以腹胀腹痛、腹部肿块、阴道不规则流血等为首发症状,部分患者为无症状的体检发现,实验室检查无明显特异性,CA125可增高,约10%的患者可发生高钙血症,血钙升高可能与肿瘤细胞分泌甲状旁腺激素相关肽PTH-rP有关,本例患者血钙轻度降低,与文献报道不符,可能与个体因素有关。首诊时多为Ⅰ期及Ⅱ期患者,虽然短期预后相对较好,但复发率明显增高,潜在恶性程度更高,建议术前对患者进行全面风险评估,包括系统性淋巴结清扫在内的全面分期手术结合放化疗综合治疗手段。
本病主要影像学表现为:(1)肿瘤形态规则,呈圆形或类圆形,常常较大,多>10 cm;(2)肿瘤边界清晰,多位于单侧,少见双侧;(3)囊实性肿块,以囊性为主,囊性肿块密度多均匀,CT值约20~30HU,若合并有出血时可密度增高、不均匀,分隔少见;(4)实性部分多位于肿瘤的偏侧壁,CT值约28~53HU,形态不规则,并突向腔内的较大结节,密度不均匀,坏死常见,钙化少见,且钙化多呈点状,部分囊实性交界处可分界不清,邻近的囊壁可增厚;(5)增强扫描囊性部分无强化,实性部分呈持续强化趋势,若肿瘤血供丰富且密实,可在动脉期明显强化;(6)若实性成分较多,可在肿块内及周围伴有增多扭曲的供血血管,伴有同侧增粗的卵巢血管;(7)包膜可作为相对特征性的表现,主要表现为包膜完整,在增强扫描实质期包膜呈延迟强化,结合多平面重组技术可清晰显示包膜的完整性,可作为判断其预后的一个重要指标;(8)晚期可浸润周围脏器,伴有盆腔淋巴结肿大,继发腹腔、盆腔积液;(9)MRI表现显示囊性成分多表现为长T1、长T2信号,若伴有出血呈稍短T、稍短T2信号,而实性成分呈等T1、稍长T2为主,DWI显示实性部分弥散受限,可伴有子宫肌瘤、子宫内膜异位症;(10)B超:以无回声液性团块为主,边界清晰,团块内伴有稍低回声软组织团块,形态不规则,可伴有彩色血流。
本例患者为老年绝经期女性,临床症状不典型,体检发现,影像上表现为边界清晰的囊实性肿块,包膜完整,但实性部分轻度强化,且伴有明显的环状骨化,影像征象不典型,术前误诊为卵巢囊腺癌,最终经病理及免疫组织化学确诊。
卵巢来源的囊实性表现为主的肿瘤主要需与卵巢囊腺癌、卵巢甲状腺肿相鉴别。(1)卵巢囊腺癌:40~50岁多发,可双侧,形态不规则分叶状,可表现为多房囊性肿块和囊实性肿块,囊壁及分隔厚薄不均,伴有壁结节或“菜花”状实性突起,增强扫描强化明显,伴有CA125明显增高,常常伴有腹膜种植转移,腹腔积液和淋巴结转移。(2)卵巢甲状腺肿:多为单侧、边界清晰的分叶状或椭圆形囊实性或多囊性肿块,由于囊腔内富含黏稠的甲状腺胶质蛋白平扫表现为囊腔高密度较具特征,囊壁光滑、多均匀,囊壁和间隔相对较厚,常常伴有斑点状或斑片状钙化,实性组织因富含甲状腺组织和纤维基质具有丰富的血管网而明显强化,囊性部分无强化。
原始出处:
朱玉春,周伟,唐琪,张阳,邢伟.伴骨化的卵巢透明细胞腺癌一例[J].临床放射学杂志,2019(01):197-198.