乳腺癌骨转移可因骨质疏松症加重,与长期生存差相关,治疗选择有限。硬化蛋白(Sclerostin,SOST)是一种内源性骨形成抑制剂,是治疗骨质疏松症的一个有吸引力的靶点。然而,目前尚不清楚SOST是否可以作为乳腺癌骨转移的治疗靶点,以及乳腺癌细胞中靶向SOST的小分子化合物是否能抑制乳腺癌骨转移。
2022年12月29日,中国医科大学刘彩刚团队与中国科学院大连化学物理研究所吴思晋团队合作在Molecular Cancer 杂志在线发表题为“Targeting SOST using a small-molecule compound retards breast cancer bone metastasis”的研究论文,该研究发现SOST表达上调与乳腺癌患者预后不良相关。机制上,SOST通过激活下游信号通路促进乳腺癌细胞增殖和骨转移。通过计算筛选,该研究确定了一种候选治疗化合物S6,可以破坏SOST与STAT3的相互作用,以抑制STAT3磷酸化并减少乳腺癌骨转移。总之,这项研究发现强调了一种新的治疗乳腺癌骨转移的潜在疗法。
全世界每年有超过150万的癌症骨转移患者。癌症骨转移患者通常会发生严重的骨骼相关事件(skeletal-related events,SREs),包括骨折、剧烈疼痛和残疾,严重降低生活质量。骨质疏松症是癌症骨转移的危险因素,抗骨质疏松药物已被用作癌症骨转移患者的常规治疗。
骨靶向药物(bone targeted agents,BTAs),如双磷酸盐,可以减少骨溶解和改善骨微环境,抑制癌症骨转移的进展。然而,在SUCCESS III期临床试验中,双磷酸盐未能预防早期乳腺癌骨转移。虽然有报道双膦酸盐可抑制乳腺癌细胞增殖,但尚无证据表明双膦酸盐可直接消除局灶性骨病变中的癌细胞。此外,一些骨分泌蛋白对骨质疏松症的发展很重要,针对这些蛋白的治疗性人源化抗体已经被开发出来,目的是抑制骨吸收和转移。地诺单抗(Denosumab)是一种抗核因子κ b配体(receptor activator of nuclear factor kappa-B ligand, RANKL)受体激活剂的抗体。地诺单抗治疗可延缓骨转移患者SRE的发生和随后的(多重)进展。然而,仍然没有证据表明地诺单抗直接消除局灶性骨病变中的癌细胞。
硬化蛋白(Sclerostin, SOST)是骨基质中成熟骨细胞分泌的一种糖蛋白。在功能上,SOST作为骨形成的抑制剂,使其成为治疗骨质疏松症的治疗靶点。此外,SOST作为致癌因子可诱导乳腺癌骨转移和骨溶解,抑制SOST可缓解乳腺癌引起的骨转移和肌无力。罗莫单抗(Romosozumab)是一种针对SOST的人源化抗体,已被美国FDA批准用于治疗骨质疏松症。在功能上,罗莫单抗可结合间质中的SOST促进成骨。虽然它在治疗绝经后骨质疏松症方面有很好的疗效,但在临床试验中与高心血管风险相关。因此,迫切需要发现新的SOST抑制剂,特别是小分子的SOST抑制剂,以安全地治疗癌症骨转移和骨质疏松症。
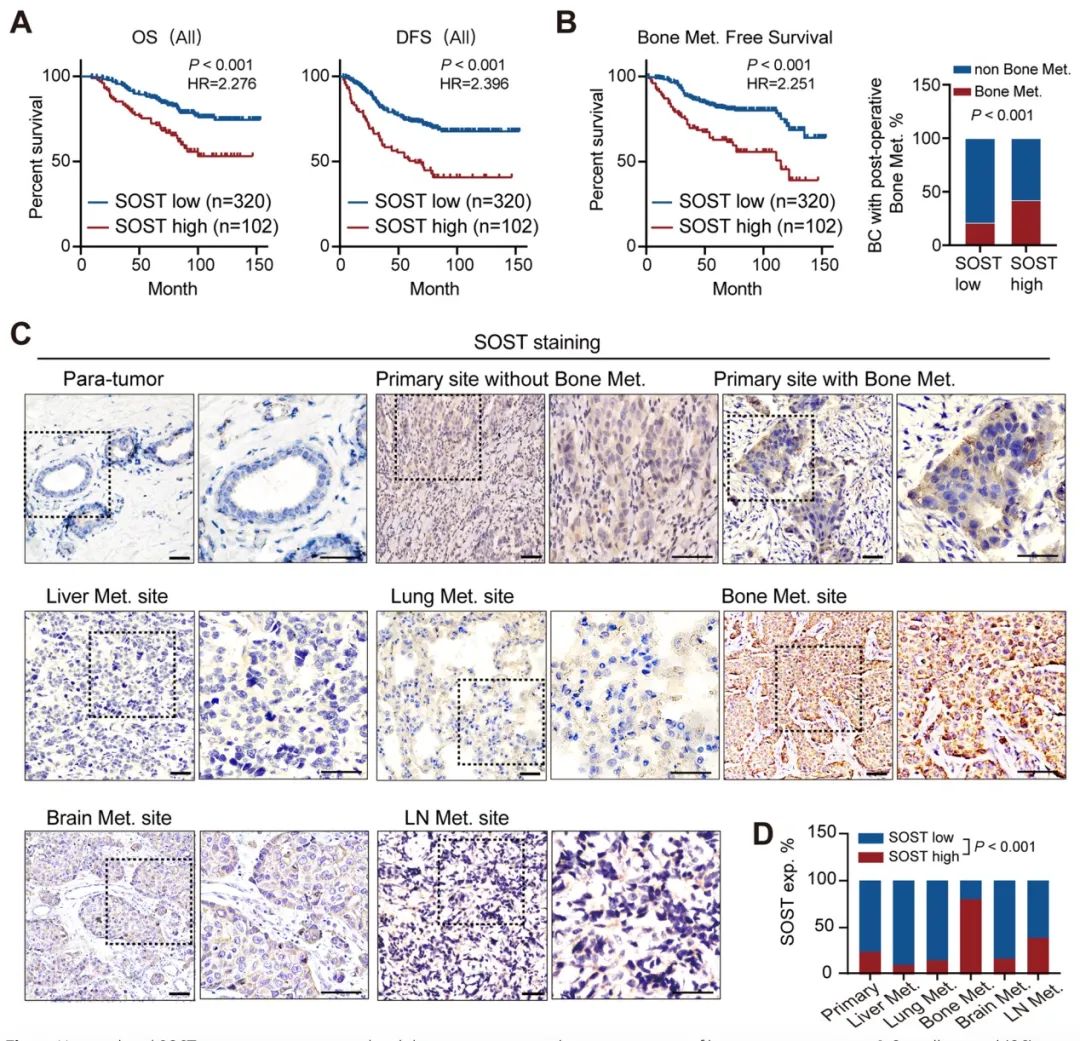
在这项研究中,研究人员在422名乳腺癌患者中发现乳腺癌组织中SOST表达上调与乳腺癌骨转移的发生显著相关。这一新发现支持了SOST作为促癌因子促进乳腺癌骨转移的观点,提示SOST可能是抑制乳腺癌骨转移的治疗靶点。
图1. SOST表达上调与乳腺癌骨转移及预后不良有关(图源自Molecular Cancer )
通过诱导骨转移性乳腺癌SCP2细胞沉默或过表达SOST,并在体外和体内检测其骨转移行为,研究发现SOST表达上调与乳腺癌骨转移和乳腺癌患者生存率降低有关。SOST沉默显著降低了SCP2细胞的骨转移能力。进一步研究表明,SOST与STAT3相互作用增强TGF-β/KRAS信号通路,促进肿瘤生长和骨转移。
为了确定潜在的治疗方法,研究人员从一个小的化学分子库中筛选了SOST与STAT3相互作用的抑制剂,并在体外和体内测试了一种抑制剂对乳腺癌生长和骨转移的抑制作用。结果表明通过用一种先导候选S6治疗可以显著抑制小鼠乳腺癌类器官的生长和骨转移。在功能上,化合物S6具有抑制肿瘤的作用。值得注意的是,目前用于治疗骨质疏松症的SOST单克隆抗体主要靶向SOST的环2,该环参与心血管保护。
研究人员筛选了可能针对SOST非环2口袋的小分子化合物。结果表明S6在体内耐受良好,毒性最小,特别是避免心脏毒性。S6-SOST复合物的结构建模和免疫沉淀证实了S6与SOST的结合及其与STAT3的竞争以破坏SOST-STAT3复合物的形成。在分子水平上,S6似乎占据了SOST的一个重要口袋,以阻止其在乳腺癌细胞中与STAT3的相互作用。
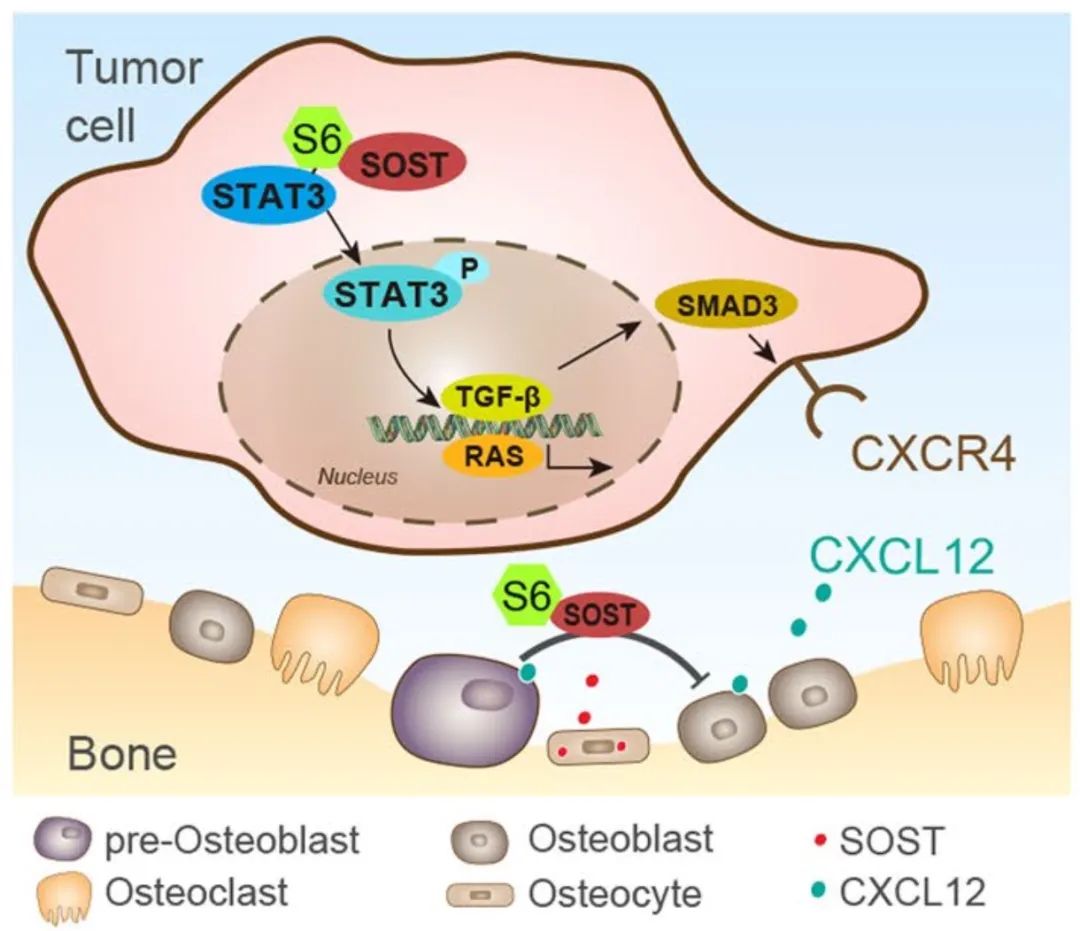
图2. 研究机制(图源自Molecular Cancer )
SOST结合STAT3激活RAS和TGF-β/ SMAD/CXCR4信号通路,促进癌细胞增殖和骨肥大,而S6抑制SOST-STAT3结合抑制后续过程
综上所述,该研究结果强调了靶向SOST-STAT3复合物治疗乳腺癌骨转移的可行性和治疗潜力,并确定了S6作为一种有前途的候选药物作为一种新的癌症治疗药物进一步发展。
原文链接:
https://molecular-cancer.biomedcentral.com/articles/10.1186/s12943-022-01697-4
来源:iNature
版权声明:
本网站所有注明“来源:梅斯医学”或“来源:MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有,非经授权,任何媒体、网站或个人不得转载,授权转载时须注明“来源:梅斯医学”。本网所有转载文章系出于传递更多信息之目的,且明确注明来源和作者,不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。同时转载内容不代表本站立场。
在此留言