脓毒症发病率持续升高,产生了巨大的医疗成本。细菌的耐药带来全球危机,尤其是新冠流行期间,大量激素和免疫药物的使用,挑战不断升级。
在ICU中,抗菌药物治疗非常普遍,大约71%的患者接受抗生素治疗。许多抗菌药物可对危重患者造成伤害,本文旨在对危重患者抗菌药物治疗时考虑因素和面临的障碍进行讨论。
1.危重症患者的细菌定植
细菌定植是指微生物在人体内部(胃肠道、呼吸道或泌尿生殖系统)或外部(皮肤)表面的存在和存活,而不会在宿主体内产生疾病。医护人员和ICU内的无生命物体表面可能被各种耐药病原体定植,将会导致医院感染。耐药病原体携带者发生耐药微生物感染的风险将增加。共生菌可保护宿主免受这些病原体的侵害。当这种平衡在住院治疗或应用抗生素治疗定殖细菌后被破坏时,可能会导致感染、耐药性和患者伤害的发展。
在SARS-CoV2大流行期间,当大量患者接受高剂量类固醇和免疫药物治疗时,定植问题尤其突出。正常的定植细菌可在慢性免疫抑制患者(如移植受体或癌症患者)中发展成病毒感染。原发性念珠菌肺炎在健康人群中是罕见的,但在接受免疫调节药物治疗的人群中,继发性念珠菌肺炎非常严重。侵袭性念珠菌病在全部住院患者中占1-8%,在ICU中上升至约10%,占所有医院感染的15%。但抗真菌药物的应用并不能改善预后。
肠道和肺部储存大量共生保护菌群。在ICU中使用侵入性装置,如中心静脉导管、气管插管和尿管,也可能成为感染的储存库。共生菌的肠-肺易位可引起严重感染。肠道内无害的微生物可导致严重的肺部感染。导尿管也可能含有有害病原体,但是尿培养阳性并不提示感染必须抗菌治疗。共生菌,如金黄色葡萄球菌,可以栖息在病人的皮肤或鼻咽部,当侵入性操作时,就会获得毒力。肺炎链球菌(Streptococcus pneumoniae)是一种常见的肺部共生菌,可在住院或患病后出现免疫下调的老年或年轻患者中引起致命感染。
2. ICU的抗菌药管理
抗菌素在ICU中的使用率非常高,61%的内科和外科ICU患者接受抗生素治疗。随着多重耐药菌的流行持续升级,抗微生物药物管理战略(AMS)的实施非常关键。AMS通过一套全面的干预措施以减少抗菌药物不合理应用、降低成本、减少细菌耐药。虽然限制抗生素的使用是其基本原则之一,但AMS的总体目标超越了单纯的限制,强调了合理正确使用抗生素的重要性。从本质上讲,AMS旨在确保抗生素的处方是有针对性的,避免给那些不需要的病人使用抗生素,同时确保及时有效地治疗那些感的病人。
虽然AMS原理似乎很简单,但在日常临床中,其应用很复杂。医生需要根据患者复杂的临床表现、诊断不明确、耐药菌进行权衡,制定患者个体化治疗方案。
3. 重症医师应该了解哪些耐药机制?
根据WHO最近文件,抗菌素耐药性(AMR)处于全球公共卫生事件首位。仅细菌AMR(不包括真菌AMR)直接导致全球127万人死亡,并在2019年造成495万人死亡。选择合理抗生素,了解耐药机制至关重要。确定可能耐药菌定植的高危患者,以便进行合理的治疗。耐药机制也可以指导未来潜在的药物靶点。
抗生素耐药机制大致分为四种主要类型,
一,微生物可能会限制药物的吸收,限制其进入细胞。
二,它们可修饰药物作用靶点,改变药物在微生物内的特定结合部位。
三,药物的失活,钝化药效。
四,微生物通过外排泵作用,在药物发挥抗菌作用之前将其排出细胞。
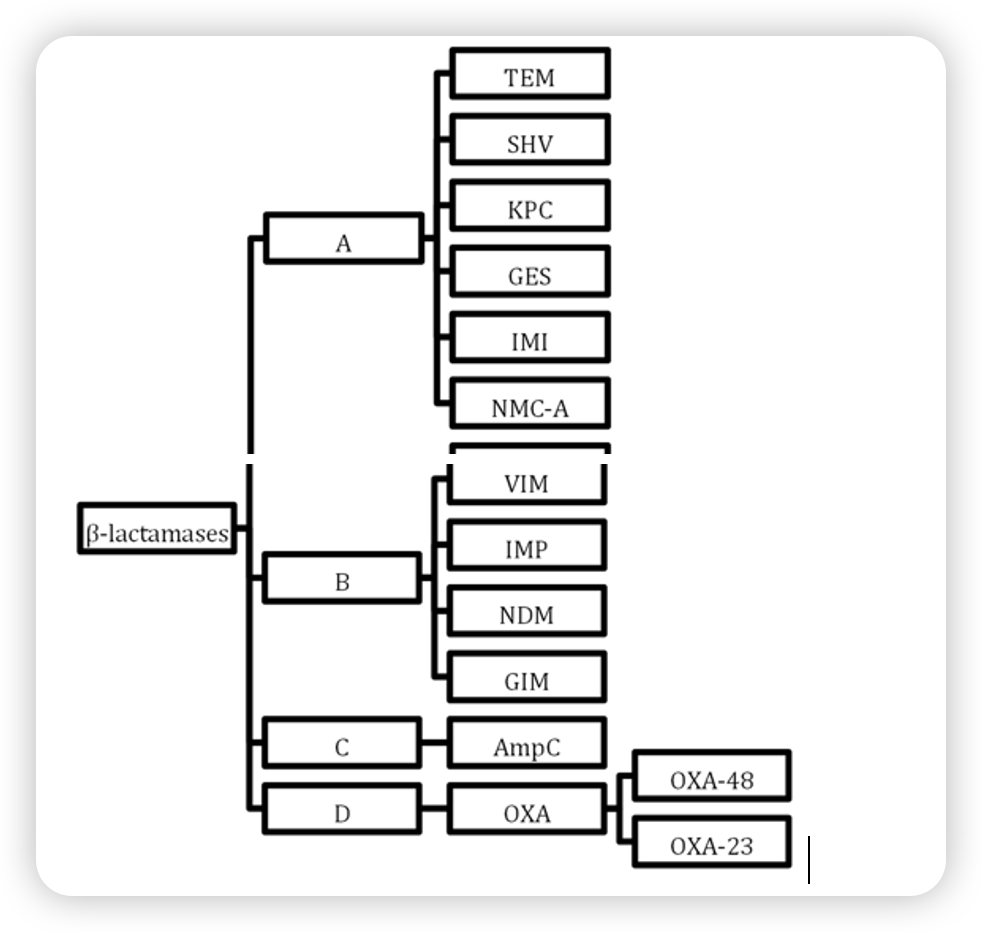
图2。β-内酰胺酶的Ambler分类。根据Ambler分类系统,β-内酰胺酶被分为四个不同的类别:A类,B类,C类和D类。这种分类是由构成蛋白质分子的初级序列固有的特定基序决定的。值得注意的是,A类、C类和D类β-内酰胺酶在其酶活性位点内使用丝氨酸残基来催化反应,而B类β-内酰胺酶则依赖锌离子来促进其催化活性。
由于染色体编码的孔蛋白通道和外排泵发生突变,喹诺酮类药物也产生耐药性。但是,在氨基糖苷易感细菌中,对氨基糖苷的耐药可能性少。
铜绿假单胞菌常耐药机制多种多样,包括AmpC β-内酰胺酶、ESBLs、MBLs、下调孔蛋白和上调外排泵。铜绿假单胞菌耐药性是ICU环境中死亡率和医疗费用增加的原因。
鲍曼不动杆菌耐药性在全球范围内是一个日益严重的问题,特别是在ICU中,该细菌已迅速产生耐药性并引起暴发。OXA碳青霉烯酶越来越多地出现在鲍曼不动杆菌中。
4. 抗生素剂量
抗菌药物的剂量和PK/PD原则至关重要,掌握这些原则以更好的在感染部位杀死细菌,减少抗菌素耐药性,最大限度地减少药物不良反应和毒性,并保持现有抗菌素的使用寿命。
4.1. 危重症患者的生理改变
ICU脓毒症患者病理生理变化,可改变抗菌药物体内浓度。脓毒症的炎症反应导致液体转移至第三间隙、高心排和低白蛋白血症,均导致分布容积增加(Vd),血浆中有效的抗菌素减少。伴有肾脏或肝脏损伤的患者,可能需要减少剂量,以确保治疗剂量,而不增加毒副作用。15%脓毒症患者因肾损伤需要CRRT治疗,此时抗菌药物剂量应个体化。
4.2. 潜在的药物突变浓度
传统上,抗菌药物的选择和耐药性依赖实验室最小抑制浓度(MIC)值。根据突变预防浓度(MPC)给药可以防止第一步耐药突变体的生长,因为ICU脓毒症患者初始细菌负担高,第一步耐药突变体的可能性增加,需要增加抗菌药物剂量。早期使用较高的抗菌药物剂量(根据PK和感染特征选择),然后在血流动力学改善时减少剂量,以优化抗菌药物剂量。
4.3. 肌酐清除率增高
增强肾清除率(Augmented renal clearance, ARC),定义为肌酐清除率 >130 mL/min,在20-65%的ICU患者中,由于其高动力状态下心输出量增加、肾血流量增强而发生ARC。它可以显著增加氨基糖苷、β-内酰胺和糖肽的清除率,导致低于治疗性抗菌药物浓度。
4.4. 雾化
通过适当的通气模式、剂量和雾化装置,雾化抗菌剂作为VAP的辅助治疗可促进抗菌剂浓度远高于MIC,增强肺实质渗透,减少耐药菌的发生率,并降低全身毒性。IDSA/ATS指南目前推荐在GNB、泛耐药和广泛耐药(PDR、XDR) VAP中使用雾化抗菌剂,尤其是那些在肺部渗透性差或静脉治具有全身毒性的抗生素,如:氨基糖苷类和多黏菌素类。
4.5. 长时间输注vs.间歇给药
最新的《拯救脓毒症指南》(2021)建议延长(延长或连续)β-内酰胺输注时间。然而,这方面的证据质量一般。假设的益处来自于达到MIC (fTMIC)以上的较高累积时间百分比,这可能导致更快的杀菌和更快的临床改善。
5. 治疗药物监测
脓毒症早期有效抗菌治疗可改善死亡率。传统的抗生素剂量可能不适用于ICU患者或病原体的特定MIC。治疗药物监测(TDM)是指在抗菌药物给药后的规定时间内获得血清样本,检测药物浓度。与经验性给药相比,TDM已被证明可以增加达到PK-PD目标的患者比例。目前推荐β-内酰胺类、氨基糖苷类和糖肽类检测TDM。
5.1. 剂量软件
最近,ICU中的给药软件已采用专门的算法,以帮助确定和管理危重症患者的适当药物剂量。这些软件解决方案旨在提高在复杂和动态的重症监护环境中进行药物管理的准确性、效率和安全性。在ICU中实施给药软件可以改善患者的治疗效果,减少用药错误,并提高医疗保健服务效率。
5.2. 未来方向
ICU抗菌治疗的潜在发展确实令人鼓舞。AI的整合作为这一领域的变革力量脱颖而出。AI有能力通过利用计算机程序仔细跟踪医院和更广泛地区的耐药性模式和传播趋势,彻底改变抗菌素管理。这种数据驱动的方法可以实现实时监测,提高干预措施的准确性并优化治疗策略。
Critical Care Medicine:成人脓毒症存活者重大心血管事件发 生的危险因素:一项基于人群的队列 研究
![]() 0
2024-01-05
点击查看
0
2024-01-05
点击查看
Critical Care Medicine:单核细胞分布宽度、降钙素原和C-反应蛋白对脓毒症 诊断准确性的比较:一项系统评价和荟萃分析
![]() 0
2024-01-05
点击查看
0
2024-01-05
点击查看
CGP医学前沿|入院前使用二甲双胍可以降低糖尿病合并脓毒症患者的死亡率
![]() 0
2024-01-24
点击查看
0
2024-01-24
点击查看

直接从血液检测病原体的技术和挑战
![]() 0
2024-01-24
点击查看
0
2024-01-24
点击查看

临床热点讨论 | 感染性休克中关于激素的使用
![]() 0
2024-02-20
点击查看
0
2024-02-20
点击查看

IVD前沿丨4小时快速鉴定和定量病原菌的新方法
![]() 0
2024-02-18
点击查看
0
2024-02-18
点击查看
