当地时间2022年2月28日,传奇生物(NASDAQ: LEGN)在美国新泽西州萨默塞特正式宣布,其自主研发的细胞治疗产品西达基奥仑赛(英文商品名:CARVYKTI®,英文通用名ciltacabtagene autoleucel,简称Cilta-cel)获得美国FDA批准上市, 用于治疗复发或难治性多发性骨髓瘤(R/R MM)患者,这些患者既往接受过四种或四种以上的治疗,包括蛋白酶体抑制剂、免疫调节剂和抗CD38单克隆抗体。传奇生物与杨森公司于2017年12月签订了全球独家许可和合作协议,以开发和商业化CARVYKTI®。
传奇生物的西达基奥仑赛CARVYKTI®获FDA批准上市,用于治疗成人复发/难治性多发性骨髓瘤(MM),成为中国首个获FDA批准的细胞治疗产品,及全球第二款获批靶向BCMA的CAR-T细胞免疫疗法。
CARVYKTI®是一款具有两种靶向B细胞成熟抗原(BCMA)单域抗体的嵌合抗原受体 (CAR)T细胞免疫疗法,以一次性输液的方式给药,推荐剂量为每公斤体重0.5~1.0×106个CAR-T细胞。
CARTITUDE-1是一项正在进行的1b/2期、开放标签、单臂、多中心的研究,用于评估CARVYKTI®治疗复发或难治性多发性骨髓瘤成人患者的安全性和有效性,这些患者至少接受过3线前期治疗,包括蛋白酶体抑制剂(PI)、免疫调节剂(IMiD)和抗CD38单克隆抗体。在参与研究的97名患者中,99%的患者对最后一线治疗不耐受,88%的患者对三种类型的治疗难治,这意味着他们对IMiD、PI和抗CD38单克隆抗体没有反应,或不再有反应。正在进行的CARTUTDE-1研究用于评估CARVYKTI®的长期疗效和安全性。
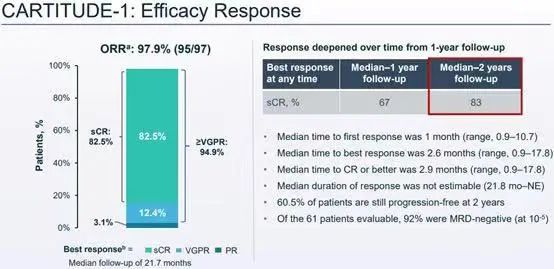
根据 2021 ASCO 公布的摘要数据显示,截至 2020 年 9 月 1 日,共有 97 名患者接受了 cilta cel 治疗,患者既往接受治疗中位线数为 6 线。独立评审委员会 IRC 评估的总缓解率为 97%(95%CI,91-99),其中 67% 达到严格意义上的完全缓解(sCR)。首次缓解的中位时间为 1 个月(范围 1-9),缓解或好转的中位时间为 2 个月(范围 1-15)。在 57 例微小残留病(MRD)可评估的患者中,93.0%(n=53)在10-5水平为MRD阴性。12个月无进展生存率(PFS)和总生存率(95%CI)分别为 77%(66-84)和 89%(80-94);中位 PFS 尚未达到。
安全性方面,3/4 级血液学不良反应事件≥20%,CRS 发生率为 95%(3/4 级为 4%),中位发病时间为 7 天(范围 1-12),中位病程 4 天(范围 1-14,不包括 1 例 97 天)。除 1 例 5 级 CRS(噬血细胞性淋巴组织细胞增多症)外,其余患者 CRS 均消失。21% 的患者出现 CAR-T 细胞神经毒性(≥3 级, 10%)。研究期间,cilta cel 输注后有 14 例死亡:前 30 天内无死亡,100 天内 2 例死亡;12 例输液后超过 100天,其中 5 例因病情进展,4 例因治疗相关不良事件。
最新公布的数据,97名R/RMM患者出现了深度持久的缓解,总缓解率(ORR)高达98%(95%CI:92.7-99.7),78%的患者获得了严格的完全反应(sCR,95%CI:68.8-86.1)。在18个月的中位随访时间中,中位缓解持续时间(DOR)为21.8个月(95% CI,21.8-无法预估)。此前报道:金斯瑞子公司传奇再次公布CAR-T临床数据,总缓解率达97%,研究者期待用于更前线治疗
CARVYKTI®只能通过风险评估和缓解策略(REMS)的受限给药计划(CARVYKTI®REMS)获取。CARVYKTI® 的安全信息包括细胞因子释放综合征(CRS)、免疫效应细胞相关神经毒性综合征(ICANS)、帕金森病和吉兰-巴雷综合征、嗜血细胞性淋巴组织增生症/巨噬细胞活化综合征(HLM/MAS)以及长期或复发性细胞减少症的黑框警告。警告和预防措施包括长期复发性细胞减少、感染、低丙种球蛋白血症、超敏反应、继发性恶性肿瘤、对驾驶和使用机器的能力的影响。最常见的不良反应(≥20%)为发热、CRS、低丙种球蛋白血症、低血压、肌肉骨骼疼痛、疲劳、不明病原体感染、咳嗽、寒战、腹泻、恶心、脑病、食欲下降、上呼吸道感染、头痛、心动过速、头晕、呼吸困难、水肿、病毒感染、凝血功能障碍、便秘和呕吐。
传奇生物CEO&CFO黄颖博士表示:“ 多发性骨髓瘤至今无法治愈,既往接受过多重治疗的患者仍然面临着预后不良和治疗选择有限。CARVYKTI®的获批对于传奇生物来说意义重大,这是我们自成立以来第一款获批上市的产品。但更可喜的是,对于那些需要长期无治疗间隔的患者而言,该药物有潜力成为新的有效治疗选择。这是我们计划带给患者众多细胞疗法的第一款产品,未来我们将继续推进各类疾病的研发管线布局。”
多发性骨髓瘤是骨髓中的浆细胞恶性增殖引起的一种恶性肿瘤。大多数患者在接受初始治疗后复发,并在接受免疫调节剂、蛋白酶体抑制剂和抗CD38抗体等主要药物治疗后预后不佳。
“ 对于大多数多发性骨髓瘤患者来说,治疗过程是一个不断缓解和复发的循环,只有较少的患者经末线治疗后获得了深度缓解”,西奈山医学院血液肿瘤学教授、CARTITUTE-1 主要研究者Sundar Jagannath博士说。“这就是为什么我对CARTITUDE-1研究的结果感到非常兴奋,该研究表明CARVYKTI®在即使经过多线治疗后的多发性骨髓瘤患者群体中,同样能提供深度持久的缓解和长期无治疗间隔。CARVYKTI®的获批有望满足这些巨大且尚未被满足的患者需求。”
作为一种个性化疗法,CARVYKTI®的使用需要通过广泛的培训、准备和认证方能确保为患者提供良好的体验。传奇和杨森从2022年起将分阶段地启动认证治疗中心网络,扩大生产能力并增加CARVYKTI®在全美的可及性,确保CARVYKTI®以可靠、及时的方式提供给肿瘤医生及他们的患者。
值得一提的是,该结果甚至优于已经获批上市的BCMA CAR-T疗法Abecma,其中经Abecma治疗后,患者总缓解率(ORR)为72%,有28%的患者完全缓解(CR),治疗后起效的中位时间是30天,中位持续缓解时间为11个月。
关于CARVYKTI®(Cilta-cel,西达基奥仑赛)
Cilta-cel是一种靶向B细胞成熟抗原(BCMA)的嵌合抗原受体T细胞(CAR-T)疗法,使用嵌合抗原受体(CAR)的转基因对患者自身的T细胞进行修饰,以识别和消除表达BCMA的细胞。BCMA主要表达于恶性多发性骨髓瘤B细胞、晚期B细胞和浆细胞的表面。CARVYKTI®的CAR蛋白具有两种BCMA靶向单域抗体,对表达BCMA的细胞具有高亲和力,在与BCMA表达细胞结合后,CAR可促进T细胞活化、扩增,继而清除靶细胞。
2017年12月,杨森与传奇生物签订了全球独家许可和合作协议,以开发和商业化CARVYKTI®。2021年4月,传奇生物宣布向欧洲药品管理局提交上市许可申请,以寻求Cilta-cel的获批, 用于治疗复发或难治性多发性骨髓瘤患者。除2019年12月在美国授予的突破性疗法(BTA)外,Cilta-cel于2020年8月在中国被纳入“突破性治疗药物”。美国FDA和欧洲EMA分别于2019年2月和2020年2月授予Cilta-cel孤儿药的名称。