罗氏宣布,国家药品监督管理局(NMPA)已批准PD-L1单抗Tecentriq(atezolizumab)联合抗血管内皮生长因子(VEGF)单抗Avastin(贝伐单抗),用于未接受过全身性治疗、不可切除的肝细胞癌(HCC)患者。
图片来源:https://www.biospace.com/article/genentech-s-avastin-tecentriq-combination-gets-greenlight-for-liver-cancer/
罗氏首席医学博士Levi Garraway说:“全世界上近一半的肝细胞癌患者在中国,这项批准标志着中国肝细胞癌治疗的重大进展。”
中国临床肿瘤学会(CSCO)肝癌专家委员会主席秦叔逵教授说:“在中国,原发性肝癌是第四常见的恶性肿瘤,大多数中晚期患者诊断时已经不能选择手术或其他局部疗法,因此迫切需要新的治疗药物。IMbrave150研究表明,Tecentriq和Avastin联合使用可以显着改善患者的预后。该组合现在中国获批,为中国肝癌患者提供了新的选择。”
肝癌是中国最常见的癌症之一,每年诊断近40万例,约368,000例死亡,相当于每天超过1000例死亡。中国肝癌患者的平均5年生存率仅约15%。
该批准是基于III期IMbrave150研究的结果,在194名中国患者中的研究结果显示与索拉非尼相比,Tecentriq联合Avastin将死亡风险(总体生存率,OS)降低了56%,将疾病恶化或死亡的风险(无进展生存期,PFS)降低了40%。并且Tecentriq和Avastin具有良好的耐受性,毒性易于控制。
IMbrave150全球研究结果表明,与索拉非尼相比,Tecentriq与Avastin组合可使死亡风险(OS)降低42%,并将疾病恶化或死亡风险(PFS)降低41%。这些结果已于2020年5月14日发表在《新英格兰医学杂志》上。
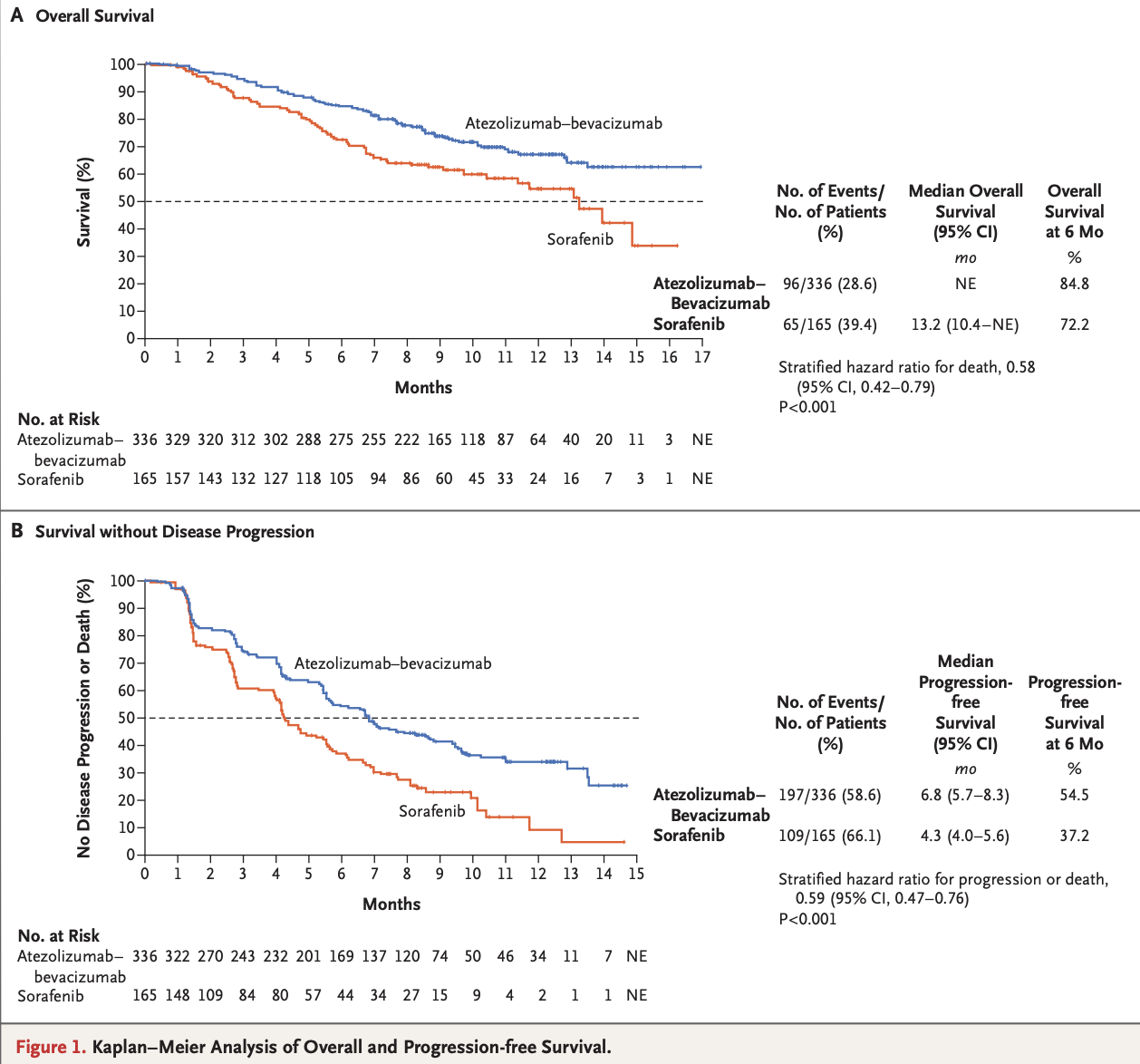
图片来源:Atezolizumab plus Bevacizumab in Unresectable Hepatocellular Carcinoma. N Engl J Med. 2020
原始出处:
https://www.firstwordpharma.com/node/1769169?tsid=4
百济神州PD-1单抗Tislelizumab治疗肝细胞癌的新药申请被NMPA接受,以及Tislelizumab抗肿瘤临床研究汇总
![]() 0
2020-07-03
点击查看
0
2020-07-03
点击查看

AP&T:免疫耐受期慢性乙型肝炎患者发生肝细胞癌的风险极低
![]() 0
2020-07-07
点击查看
0
2020-07-07
点击查看
JGH Open:肝细胞癌的危险因素总结
![]() 0
2020-07-13
点击查看
0
2020-07-13
点击查看
Cell Death Dis:BRD9激活TUFT1/AKT通路促进肝细胞癌的生长和转移
![]() 0
2020-09-10
点击查看
0
2020-09-10
点击查看

Brit J Cancer:年龄对索拉非尼治疗肝细胞癌患者结局的影响
![]() 0
2020-10-21
点击查看
0
2020-10-21
点击查看
Br J Cancer:国际性队列研究:年龄对索拉非尼治疗肝细胞癌预后的影响
![]() 0
2020-10-24
点击查看
0
2020-10-24
点击查看
