病 史:
6月患儿,家属发现右腹部包块入院;
泌尿系CT提示:
右肾实质内见多发大小不等囊状类圆形,较大约100x74x100mm,内见分割,增强扫描未见明显强化(图1);
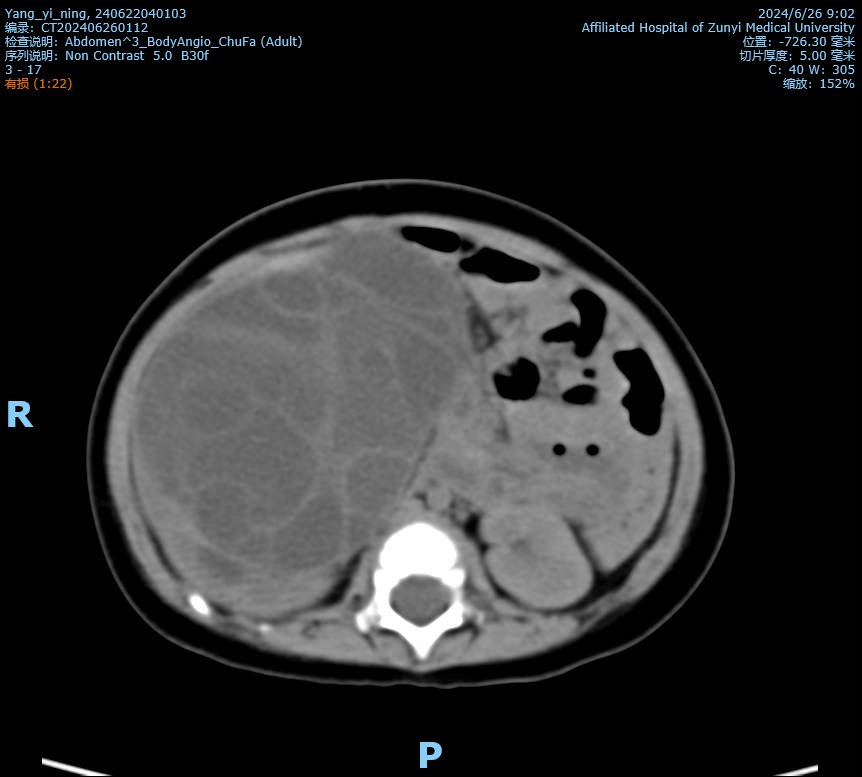
图1
大体检查:
右肾表面呈多房囊性改变,内见纤维分割,囊肿壁水肿增厚(图2),囊内液稍浑浊。
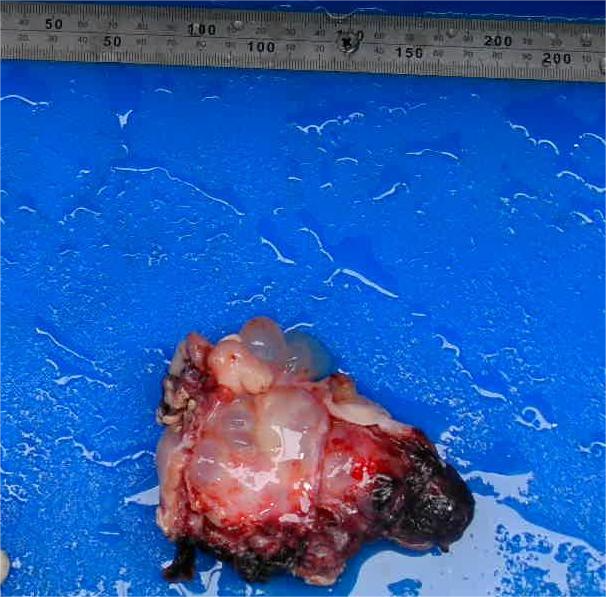
图2
镜下所见:
(右侧)肾组织呈多房囊性改变,囊壁被覆单层立方或柱状上皮,囊壁内见小蓝圆细胞增生,细胞原始幼稚、染色深,内见小灶小管状结构,局灶可疑横纹肌样分化成分。
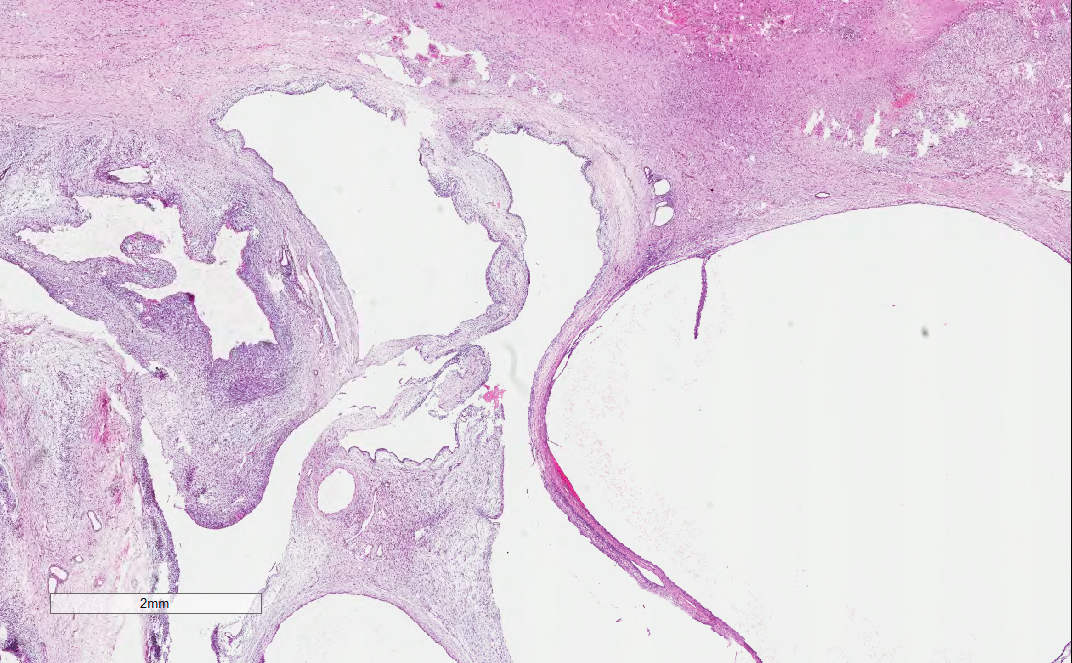
低倍镜下显示,组织呈囊性改变

中倍镜下,可见囊壁上皮呈靴钉样改变
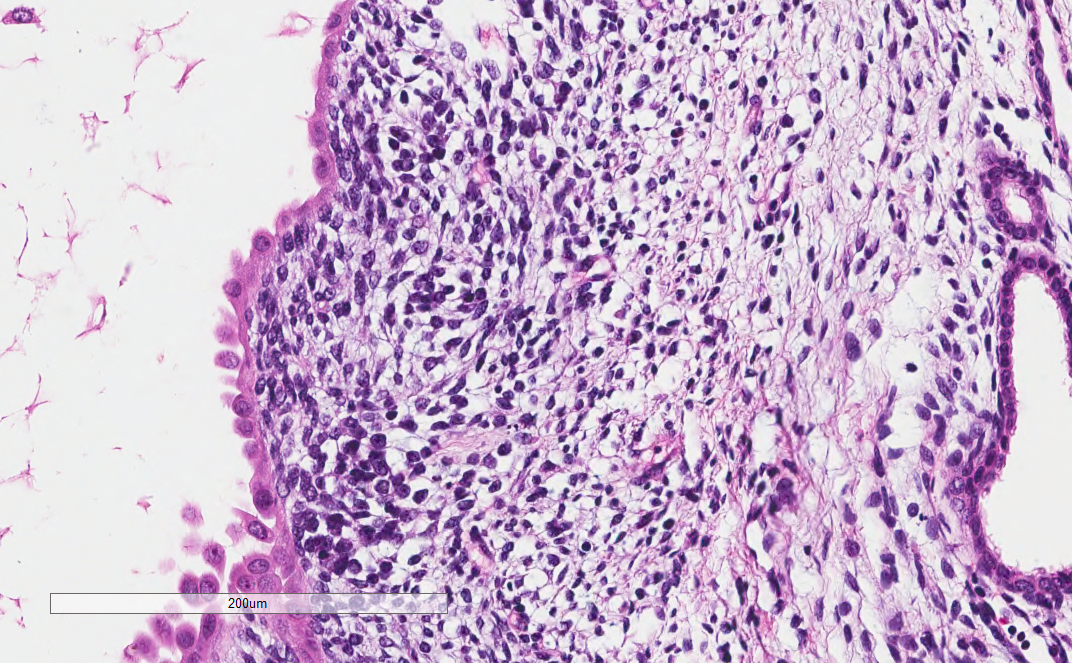
高倍镜下,可见囊壁上皮呈靴钉样改变,间质内可见幼稚的梭形细胞
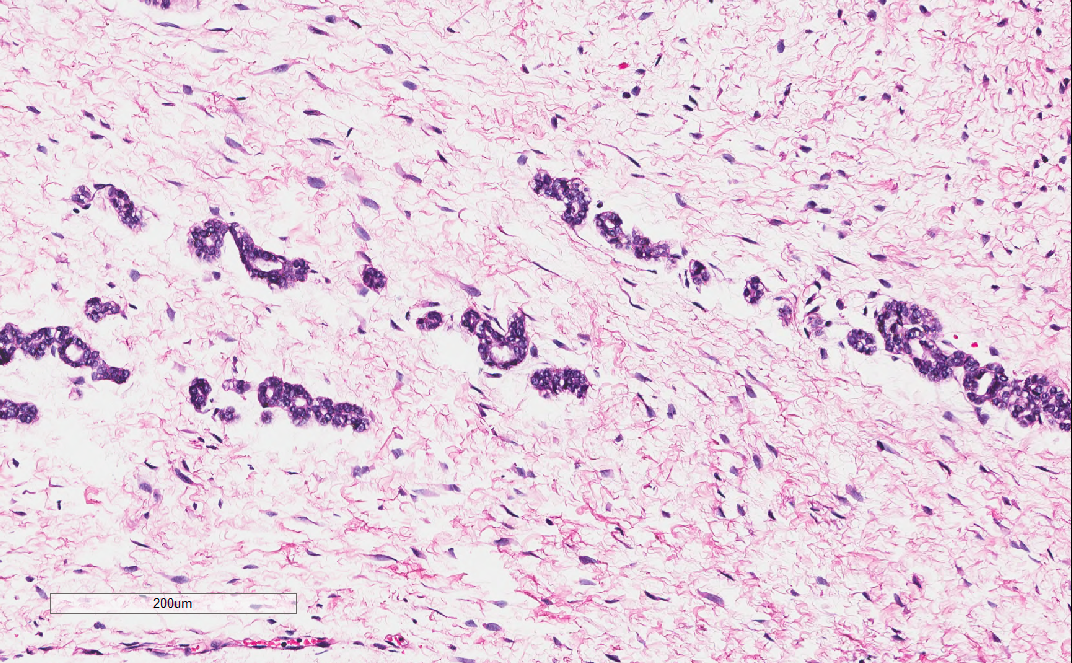
部分间质内可见上皮样管状结构
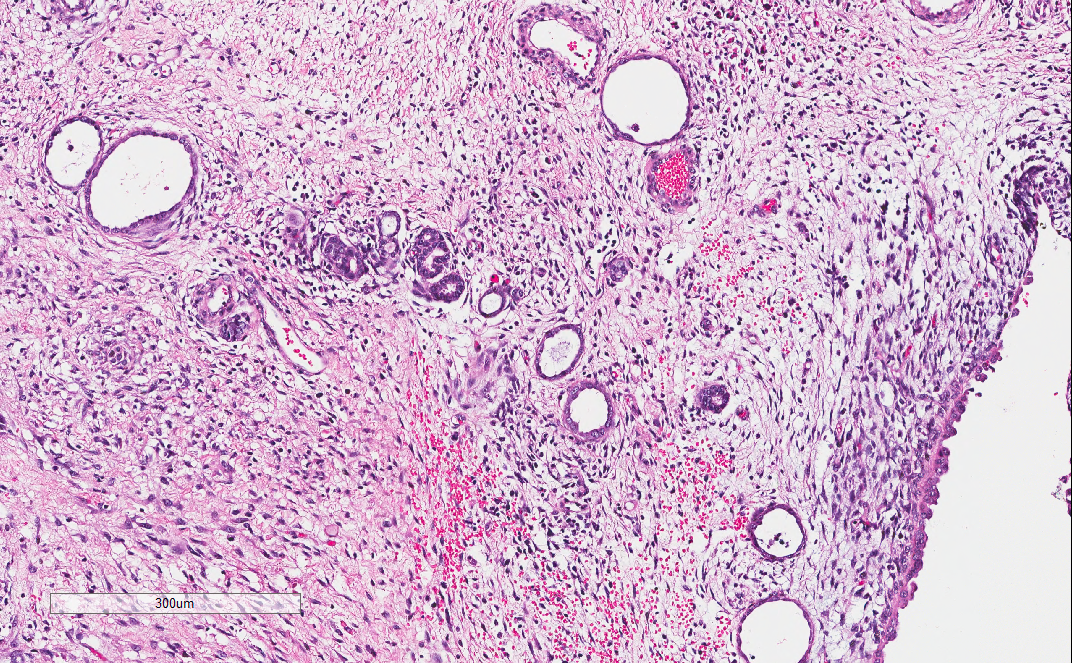
部分间质内可见上皮样管状结构
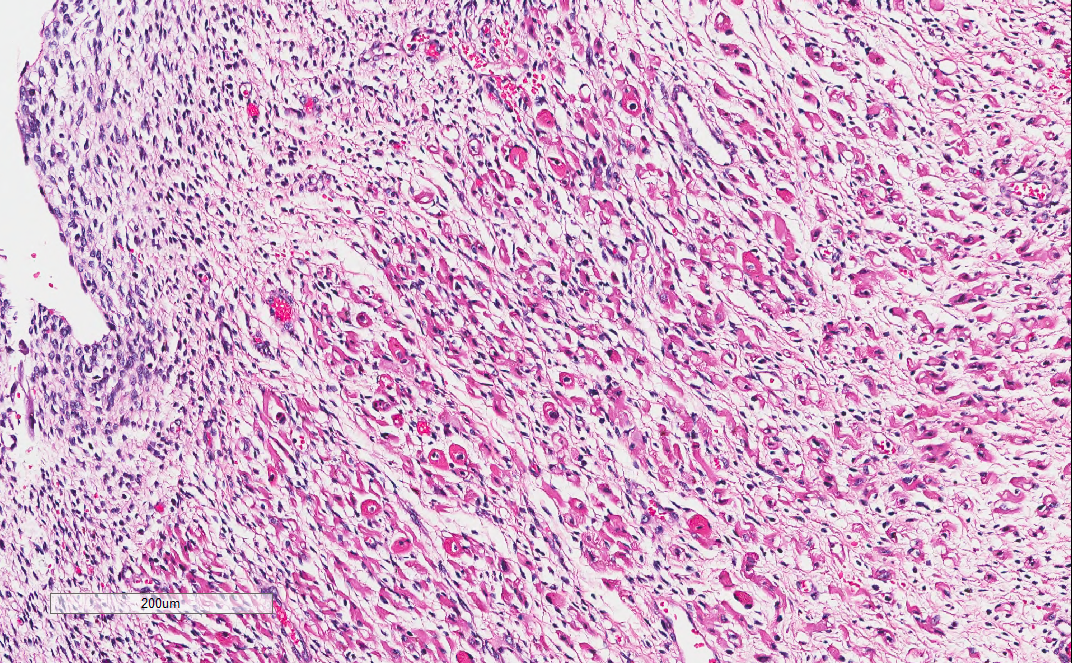
部分间质内还可见横纹肌样分化
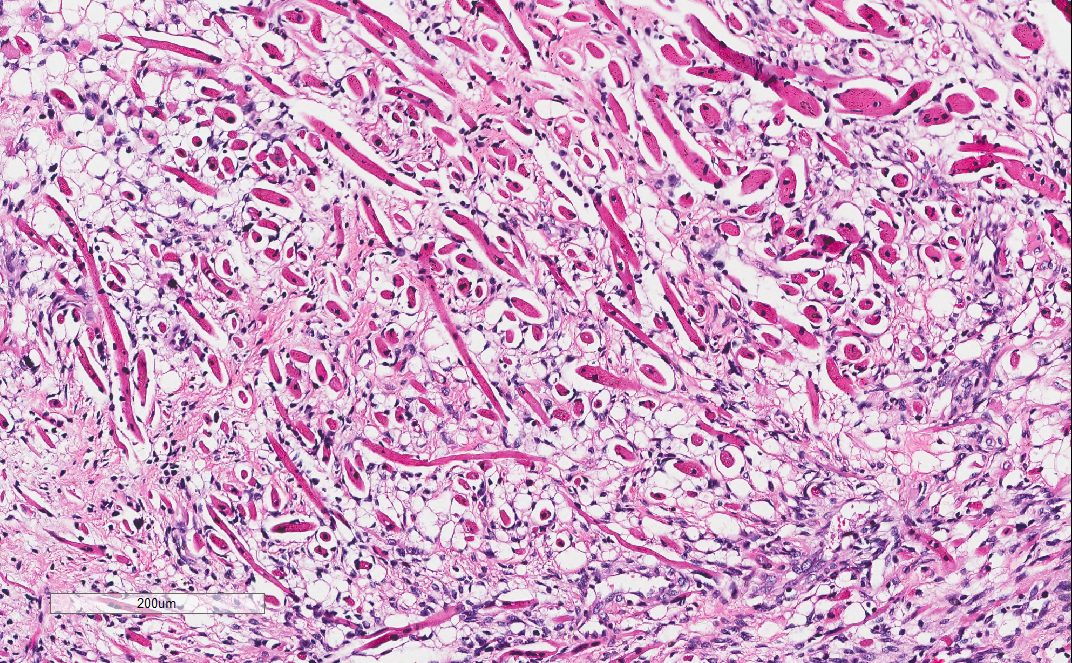
部分间质内还可见横纹肌样分化
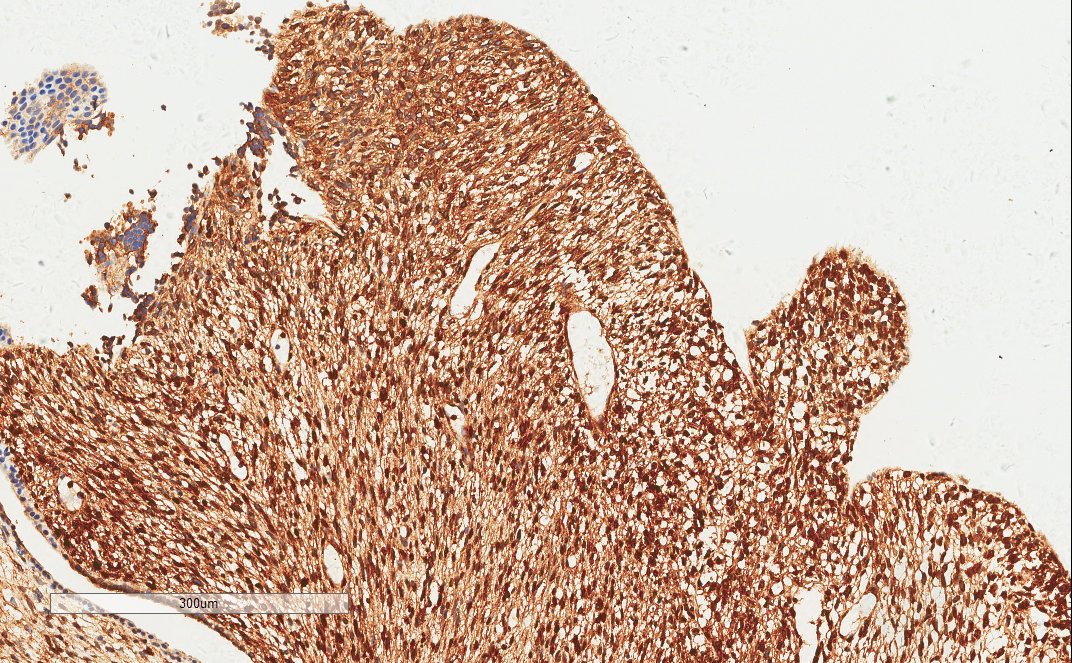
CD10阳性
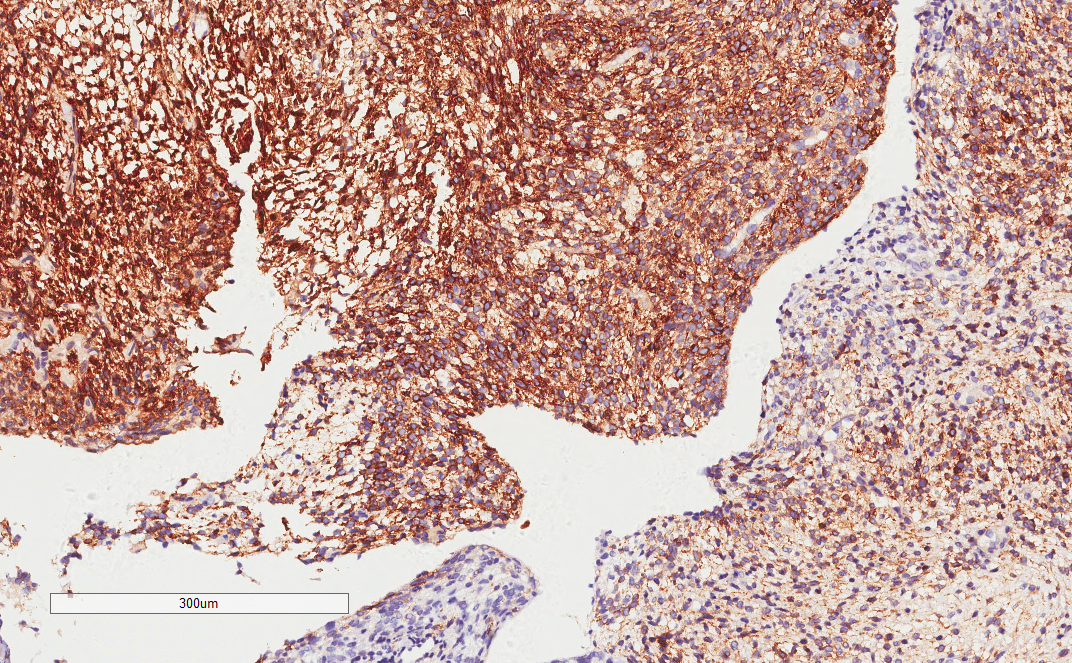
CD56阳性
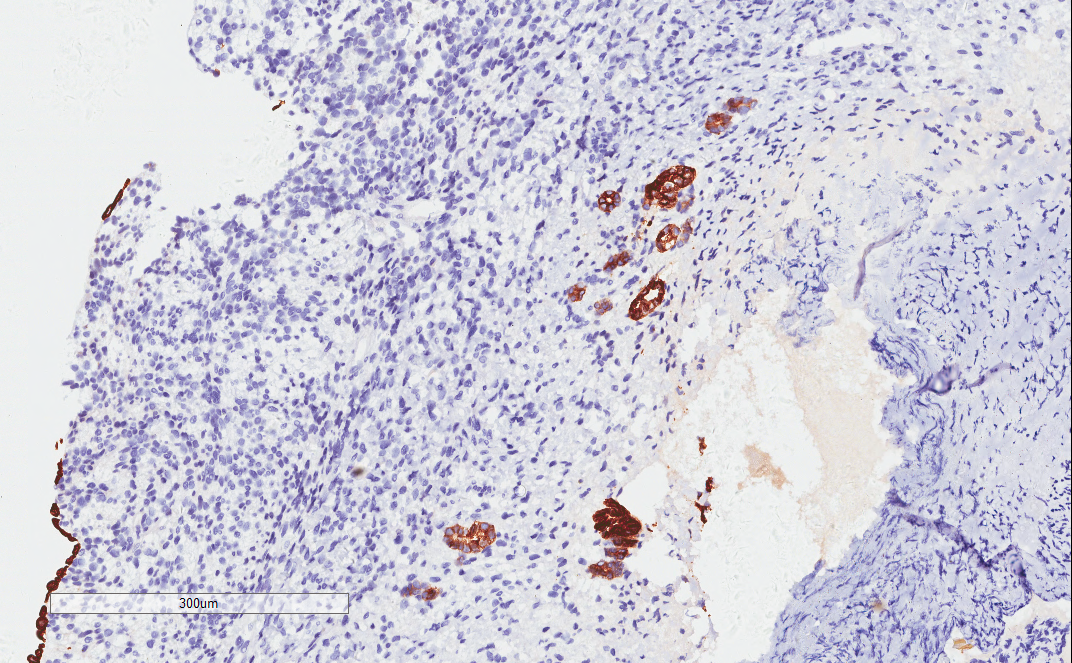
CK7部分小管+
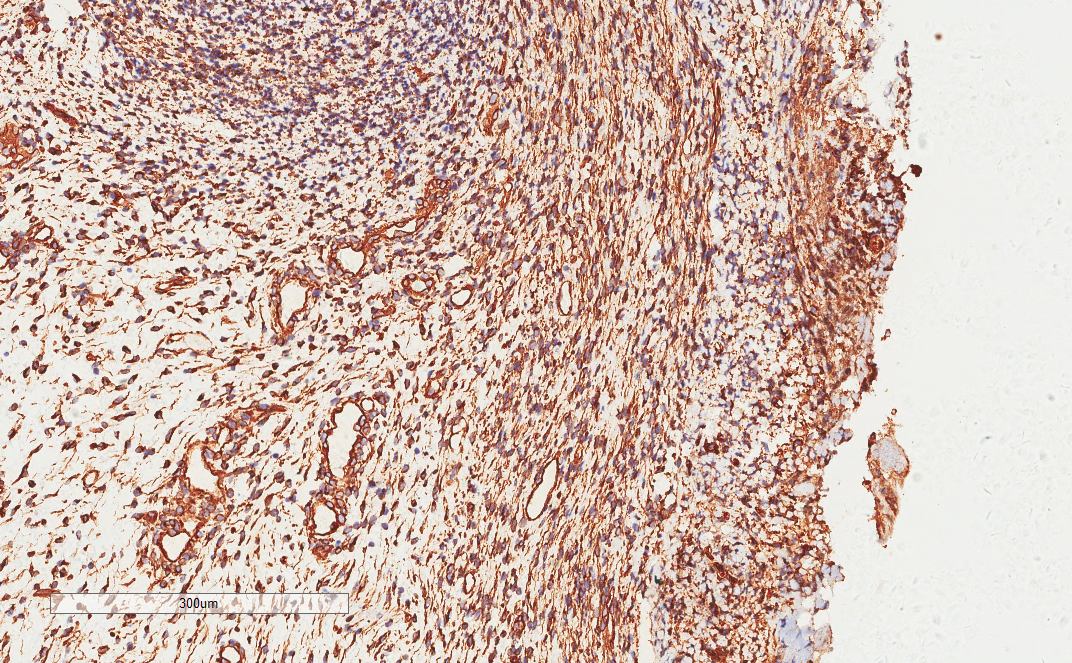
Vimentin 阳性
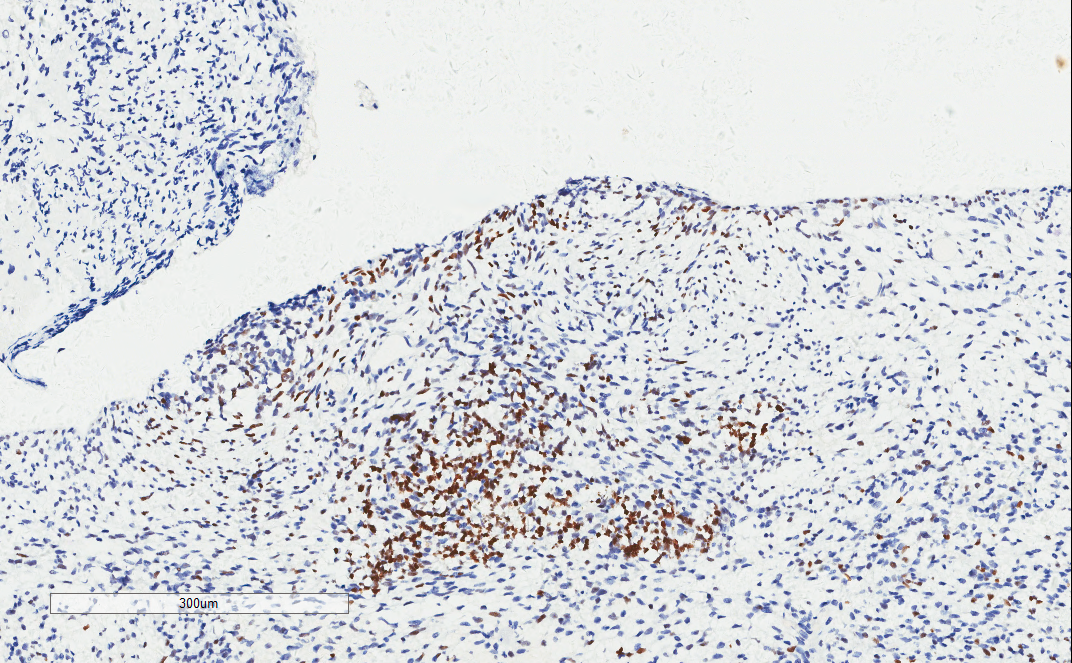
WT-1局灶+
免疫组化:
囊性部分分化性肾母细胞瘤是肾母细胞瘤(Wilms瘤)的一种特殊亚型,以囊性结构为主,含少量分化性胚基、间质或上皮成分。其免疫组化特征与经典肾母细胞瘤相似,但需结合形态学综合判断:
1. 典型阳性标记:
WT1:核阳性(胚基和上皮成分阳性,间质成分通常阴性)。
CD56:胚基成分阳性。
CK(AE1/AE3):上皮成分局灶阳性。
PAX8:肾源性分化的标志,常阳性。
β-catenin:核阳性(提示Wnt通路激活)。
2. 阴性或弱表达:
CK7/CK20:通常阴性(可与肾细胞癌鉴别)。
CD34:阴性(排除血管源性肿瘤)。
SMA/Desmin:间质成分可能局灶阳性,但无弥漫表达。
3. 增殖指数:
Ki-67:通常较低(与高分化的生物学行为一致)。
01 鉴别诊断
CPDN需与其他肾脏囊性病变及儿童肾脏肿瘤鉴别:
1. 多房性囊性肾瘤(Multilocular Cystic Nephroma, MCN)
- 形态学:囊壁被覆扁平或立方上皮,无胚基成分,间质为致密纤维组织。
- 免疫组化:WT1阴性(与CPDN不同),PAX8可能阳性。
- 临床:多见于儿童和成年女性,与CPDN同属肾母细胞瘤谱系,但生物学行为良性。
2. 囊性肾母细胞瘤(Cystic Wilms瘤)
- 形态学:囊性变显著,但可见明显胚基或未分化成分,大体为囊性+实性肿块。
- 免疫组化:WT1、CD56阳性,Ki-67指数可能更高。
3. 中胚层肾瘤(Congenital Mesoblastic Nephroma, CMN)
- 形态学:梭形细胞为主,呈束状排列,无胚基成分。
- 免疫组化:SMA、Desmin阳性,WT1阴性。
4. 囊性肾细胞癌(Cystic Renal Cell Carcinoma)
- 形态学:囊壁内衬透明细胞或嗜酸细胞,可见异型性。
- 免疫组化:PAX8、CAIX阳性,WT1阴性,CK7可能阳性。
5. 后肾腺瘤(Metanephric Adenoma)
- 形态学:小管状结构为主,无囊性结构或胚基成分。
- 免疫组化:WT1阳性,但CD56阴性。
02 诊断要点
1. 形态学优先:
囊性结构+少量胚基/上皮/间质成分是诊断CPDN的核心。
2. 免疫组化辅助:
WT1、CD56、PAX8支持肾母细胞瘤分化,需结合临床(年龄、影像学)。
3. 分子检测:
必要时检测WT1基因突变或11p15区域异常(与Wilms瘤相关)。
[ 总结表 ]

03 讨 论
囊性部分分化性肾母细胞瘤(cystic partially differentiated nephroblastoma, CPDN)是较罕见的儿童肾源性肿瘤。其临床表现与儿童囊性肾瘤相似,术前影像学检查及研究均不能将其分开。本病多发生在幼儿,年龄多小于24个月,文献中偶见超过24个月甚至发生于成人的报道。呈良性经过,手术切除后可治愈。其诊断主要依赖于病理形态学,但因其囊性结构及分化性成分的多样性,常与其他肾脏囊性病变混淆。
1.以下是诊断中的主要难点:
(1)胚基成分的识别:CPDN的诊断关键在于识别囊壁内是否存在胚基成分,但这些成分可能非常稀少,容易漏诊。特别是在穿刺活检标本中,由于取材有限,诊断更具挑战性。
(2)与多房性囊性肾瘤(MCN)的鉴别:MCN与CPDN在形态学和影像学上极为相似,但MCN完全缺乏胚基成分。两者的鉴别对治疗和预后有重要意义,因为MCN为良性肿瘤,而CPDN具有潜在恶性倾向。
(3)免疫组化的局限性:虽然WT1、CD56等标志物有助于支持肾母细胞瘤的诊断,但这些标志物并非完全特异,需结合形态学综合判断。
2. 生物学行为与预后:
CPDN属于肾母细胞瘤谱系中的一种特殊亚型,其生物学行为通常较为惰性,预后良好。然而,以下几点值得关注:
(1)潜在恶性倾向:尽管CPDN的囊性结构和分化性成分提示其低度恶性,但若存在较多胚基成分或未分化区域,可能提示更高的复发或转移风险。
(2)治疗策略:目前对CPDN的治疗以手术切除为主,术后通常无需辅助化疗或放疗。但对于存在高危因素(如胚基成分较多或肿瘤破裂)的病例,可能需要个体化治疗。
(3)长期随访:由于CPDN的罕见性,其长期预后数据有限,建议对患者进行长期随访,监测复发或转移。
3. 分子病理学进展:
近年来,分子病理学在肾母细胞瘤及其亚型的诊断和分类中发挥了重要作用。CPDN的分子特征与经典肾母细胞瘤相似,可能涉及以下改变:
(1)WT1基因突变:WT1是肾母细胞瘤的关键驱动基因,其突变或表达异常在CPDN中也可能存在。
(2)Wnt/β-catenin通路激活:β-catenin的核阳性提示Wnt通路激活,可能与肿瘤的发生发展相关。
(3)11p15区域异常:肾母细胞瘤中常见的11p15区域甲基化异常在CPDN中也可能存在。
*本文(包括图片)均为作者投稿, 仅供行业交流学习用,不作为医疗诊断依据。
参考文献
[1]Wang Z P , Li K , Dong K R ,et al.Congenital mesoblastic nephroma: Clinical analysis of eight cases and a review of the literature[J].Oncology letters, 2014(8-5).
[2]Moch,Holger,Cubilla,et al.The 2016 WHO Classification of Tumours of the Urinary System and Male Genital Organs-Part A: Renal, Penile, and Testicular Tumours[J].[2025-02-07].
[3] 陈杰,步宏主编:临床病理学(第2版),人民卫生出版社,2021.
[4] 刘彤华主编:刘彤华诊断病理学(第四版),人民卫生出版社,2018.
[5] 杨文萍,武海燕,张文,等. 儿童肾母细胞瘤病理诊断共识[J]. 中华病理学杂志,2017,46(3):149-154.
[6]《儿童肾母细胞瘤诊疗规范(2019年版)》
[7] 泌尿生殖系统病理学图谱1(美)麦克莱农( Maclennan,G.T.), (美)程亮编著;黄文斌,肖立译. 2013.1