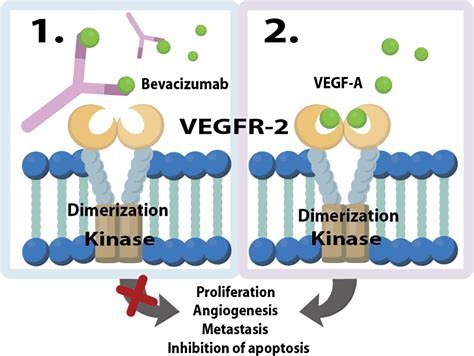
韩国三星Bioepis公司近日宣布,欧洲药品管理局(EMA)的人用药品委员会(CHMP)对AYBINTIO持肯定态度,该药品是贝伐单抗的生物类似物。CHMP推荐将AYBINTIO用于贝伐单抗的适应症,包括转移性结直肠癌(mCRC)、转移性乳腺癌(mBC)、非小细胞肺癌(NSCLC)、转移性肾细胞癌(mRCC)、上皮性卵巢癌、原发性腹膜癌和宫颈癌。欧盟委员会(EC)将对CHMP的积极意见进行审查,以决定是否授予AYBINTIO营销许可。
三星Bioepis临床科学高级副总裁Hee Kyung Kim表示:“高质量生物类似物是减轻患者经济负担的重要手段。一旦获得批准,AYBINTIO将成为针对不同类型癌症的有效治疗选择,可能会帮助欧洲的许多患者”。
AYBINTIO的市场授权申请书(MAA)得到了药代动力学(PK)和临床数据以及药理和毒理学数据的支持,这些数据表明AYBINTIO与贝伐单抗高度相似。此外,该公司于2019年9月提交了AYBINTIO的生物制剂许可申请(BLA),目前正在接受美国FDA的审查。
原始出处:
https://www.firstwordpharma.com/node/1735839?tsid=4
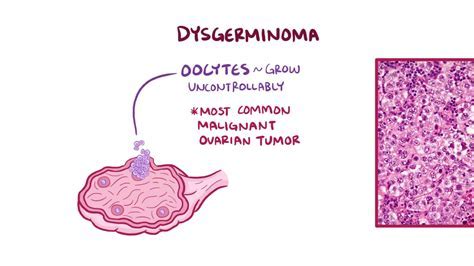
J Clin Oncol:2型神经纤维瘤病和进行性前庭神经鞘瘤高剂量贝伐单抗诱导治疗的多中心、前瞻性、阶段II和生物标记研究
![]() 0
2019-11-02
点击查看
0
2019-11-02
点击查看

NEJM:二次手术不能延长铂敏感的复发性卵巢癌患者生存期
![]() 0
2019-11-14
点击查看
0
2019-11-14
点击查看
NEJM:奥拉帕尼联合贝伐单抗一线治疗晚期卵巢癌
![]() 0
2019-12-19
点击查看
0
2019-12-19
点击查看
J Clin Oncol:III期试验:培美曲塞联合贝伐单抗作为NSCLC患者的维持疗法的有效性和安全性
![]() 0
2020-01-04
点击查看
0
2020-01-04
点击查看
Clin cancer res:FTD/TPI+伊立替康+贝伐单抗联合治疗晚期消化道肿瘤的疗效和安全性
![]() 0
2020-04-06
点击查看
0
2020-04-06
点击查看

LYNPARZA(olaparib)联合贝伐单抗一线治疗HRD阳性晚期卵巢癌:已获FDA首肯
![]() 0
2020-05-11
点击查看
0
2020-05-11
点击查看