背景:注射外源性基础胰岛素是1型糖尿病(T1DM)和二型糖尿病病(T2DM)患者降糖治疗的重要组成部分。甘精胰岛素(IGlarlantus[法国巴黎赛诺菲安万特]是一种长效基础胰岛素类似物,采用重组DNA技术开发,是首个获得监管机构批准的长效胰岛素类似物,于2000年获得批准。 LY2963016甘精胰岛素(LY IGlar欧洲联盟;Basaglar【美国】)的主要氨基酸序列、药物形式和强度与参考IGlar相同。LY IGlar是第一种生物仿制药胰岛素,于2014年9月获得欧洲药品管理局(EMA)的批准,并于2015年12月获得美国美国食品药品监督管理局(FDA)的批准。在西方和亚洲患者群中进行的多项随机III期非劣效性试验中,LY IGlar在T1DM和T2DM患者中显示出与IGlar相似的疗效和安全性。生物药物(如胰岛素类似物)是使用活细胞培养物生产的,具有内在的生产可变性,这可能导致同一药物不同批次之间以及生物仿制药和原生物制剂之间的免疫反应和临床效果的细微差异。因此,欧洲药品管理局、美国食品药品管理局和中国国家医疗产品管理局要求拟生产的生物仿制药在质量特征、生物活性、安全性和疗效方面与“原”或“参考”生物药物具有相似性。特别是,综合安全性评估要求包括免疫原性潜力的评估。在这方面,在全球随机III期ELEMENT-1和-2试验中,LY IGlar和IGlar在患有T1DM和T2DM的西方患者中表现出相当的免疫原性特征。
生物制药的免疫原性潜力取决于与产品和患者相关的各种因素。可能影响免疫原性的患者特异性因素包括免疫状态(即免疫活性与免疫抑制状态)、既往致敏、过敏、给药途径、人类白细胞抗原(HLA)单体型、细胞因子基因的遗传多态性、内源性蛋白质的数量或质量以及先前存在的抗体。种族因素可能影响药物的疗效和安全性,进而可能影响免疫原性。在主要招募白人患者的ELEMENT-1和ELEMENT-2试验中研究了甘精胰岛素(包括Lantus和生物仿制药)的免疫原性结果(ELEMENT-1,白人参与者74.5%;ELEMENT-2,白人参与者78.4%)。预计2021年中国成年糖尿病患者人数超过1.4亿,居世界第一。然而,尚未有关于东亚人群IGlar或LY IGlar免疫原性的研究报道。考虑到中国糖尿病患者的巨大数量,甘精胰岛素在中国人群中的免疫原性结果,包括其与临床结果的关联,因此将是非常有益的。
LY IGlar和IGlar在中国T1DM和T2DM患者中的有效性和安全性已分别在随机、开放的III期ABES和ABET试验中进行了研究。在ABES,T1DM成年患者接受LY IGlar或IGlar联合餐前胰岛素lispro,并在整个24周的治疗期内对免疫原性进行了评估。在ABET中,未服用胰岛素的T2DM成年患者被分配接受LY IGlar或IGlar联合≥2种口服抗高血糖药物,并在24周内对免疫原性进行了评估中国人群中LY IGlar和IGlar的准确免疫原性谱可以为医生提供关于胰岛素抗体发展潜力的信息。
目的:评价LY2963016甘精胰岛素(LY IGlar)与胰岛素原药甘精胰岛素(IGlar [Lantus ])在中国1型(T1DM)或二型糖尿病(T2DM)患者中的免疫原性。
材料和方法:ABES和ABET是前瞻性、随机、主动对照、开放标记、III期研究,分别招募了中国T1DM患者(N = 272)和T2DM患者(N = 536)。使用这些试验的数据,通过比较可检测到抗甘精胰岛素抗体的患者比例和治疗组之间的中位抗体水平(结合百分比),评估LY IGlar和IGlar的免疫原性。使用Fisher精确检验或Pearson卡方检验比较抗胰岛素抗体的发生率和治疗中出现的抗体反应(TEAR)。使用Wilcoxon秩和检验比较抗胰岛素抗体水平。我们还使用协方差、负二项式回归或偏相关分析评估了抗体形成或撕裂与临床结果之间的关系。
结果:在T1DM或T2DM患者中,可检测的抗胰岛素抗体、中位抗体水平或泪液的发生率,总体上或在最后一次观察后的第24周没有显著的治疗差异,并且在治疗24周后中位抗体水平较低(< 5%)。抗胰岛素抗体水平和泪液形成与疗效(糖化血红蛋白、胰岛素剂量[U/kg/d]和低血糖)或安全性结果无关。

图1 2型糖尿病糖尿病患者抗胰岛素抗体概述。a,可检测到的抗胰岛素甘精抗体患者的比例。b,胰岛素抗体中位数(结合百分比)。c,出现治疗紧急抗体反应(泪水)的患者比例。红色水平线表示筛选试验中5%的结合水平,大约相当于100 ng/mL。分析只包括基线时抗体检测有效和基线后≥1有效测量的患者。用费舍尔精确检验或皮尔逊卡方检验检验†治疗差异。‡数据是中位数,误差条代表四分位数范围(25%,75%)。采用Wilcoxon‘s秩和检验检验处理差异。IGlar,甘精胰岛素;LOCF,最后一次观察;:LY IGlar,LY2963016甘精胰岛素
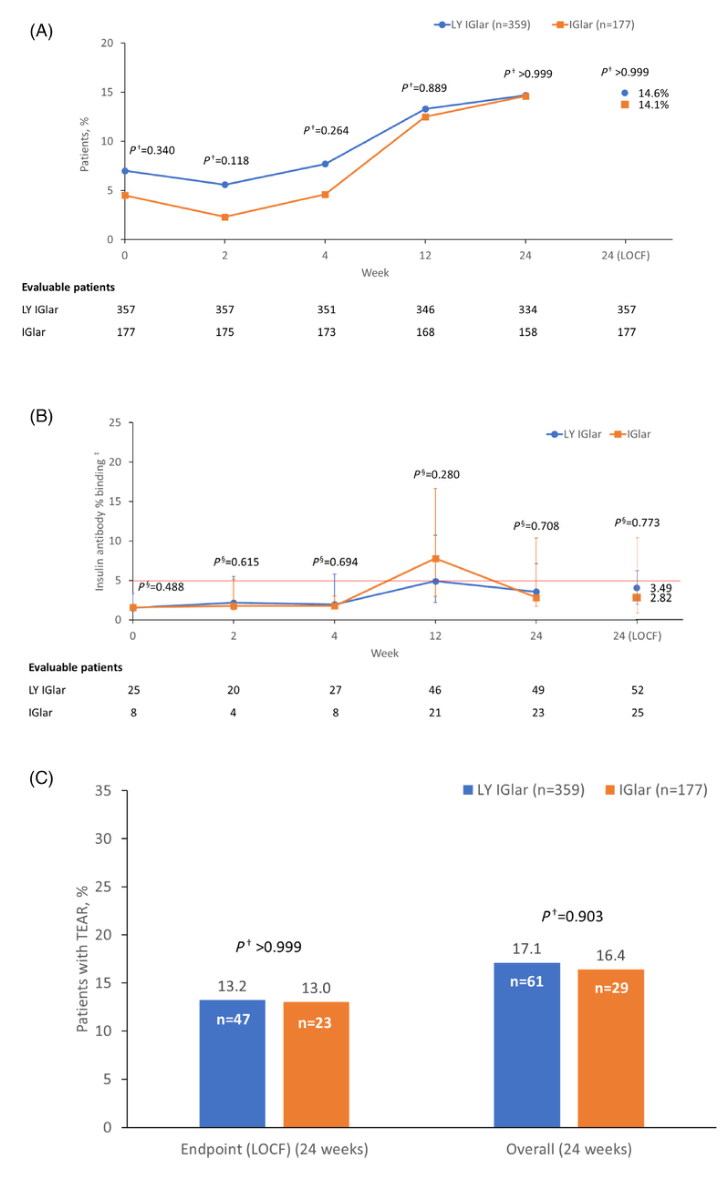
图2 2型糖尿病糖尿病患者抗胰岛素抗体概述。a、可检测到抗甘精胰岛素抗体的患者比例。b,胰岛素抗体的中值水平(结合百分比)。c,治疗中出现抗体反应(TEAR)的患者比例。粉红色水平线表示筛选分析中的5%结合水平,约等于100 ng/mL。只有基线时抗体检测有效且基线后测量有效≥1次的患者才纳入分析。治疗差异使用Fisher精确检验或Pearson卡方检验进行检验。数据是中间值,误差线代表四分位数范围(25%,75%)。使用Wilcoxon秩和检验对治疗差异进行检验。IGlar,甘精胰岛素;LOCF,最后一次观察;:LY IGlar,LY2963016甘精胰岛素
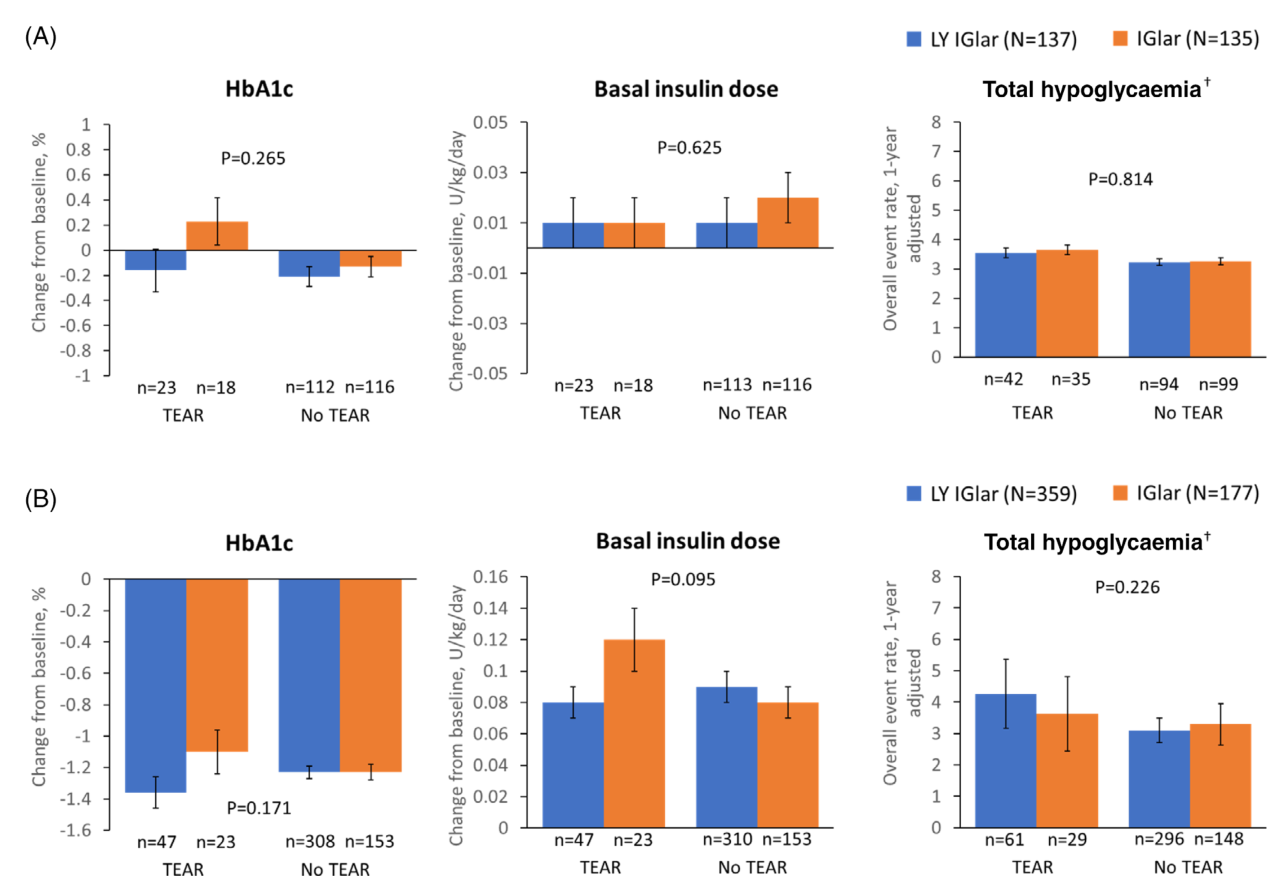
图3 在A组1型糖尿病患者和B组二型糖尿病糖尿病患者中,治疗中出现的抗体反应(TEAR)状态与疗效结果(HbA1c、基础胰岛素剂量和总低血糖率的变化,校正1年后)之间的关联。数据以从基线到LOCF终点的最小二乘平均标准误差变化表示。使用协方差分析(ANCOVA)模型计算泪液和糖化血红蛋白(HbA1c)或基础胰岛素剂量之间相互作用的p值;使用负二项式模型计算泪液和低血糖之间的相互作用。校正1年,包括血糖≤3.9毫摩尔/升的事件。IGlar,甘精胰岛素;LOCF,最后一次观察;:LY IGlar,LY2963016甘精胰岛素
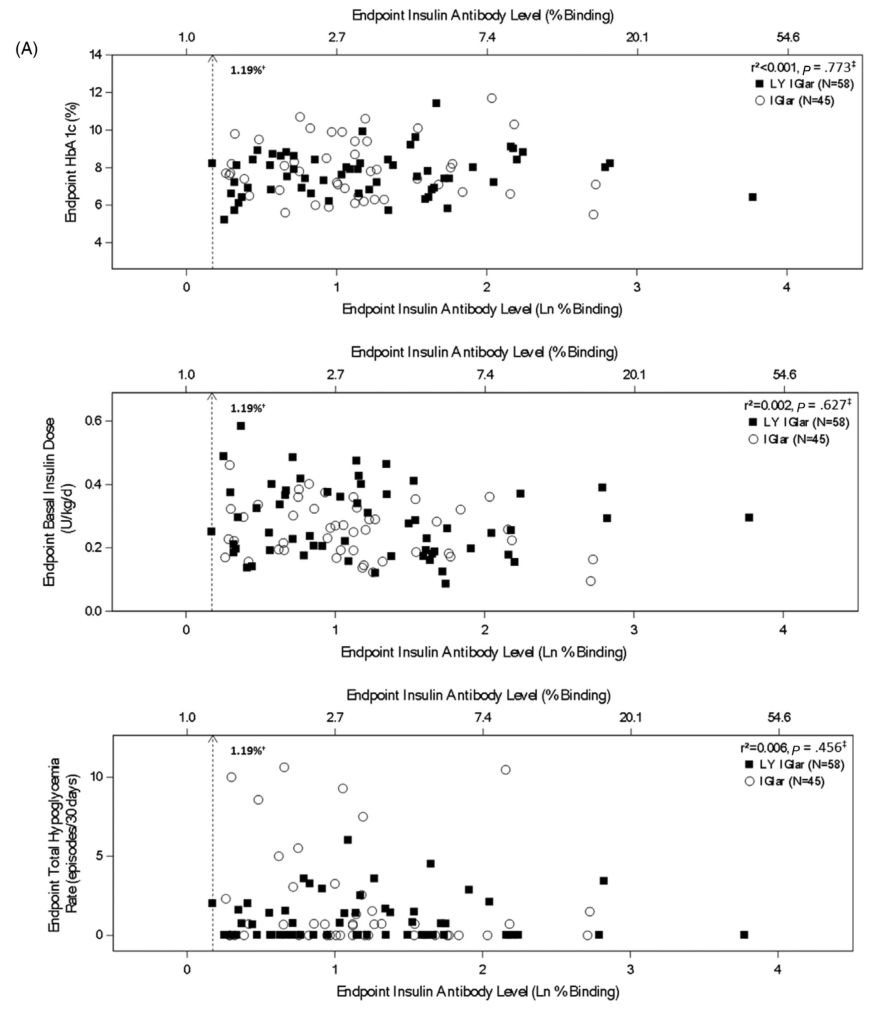
图4 在A组1型糖尿病患者和B组二型糖尿病糖尿病患者的终点(第24周,最后一次观察结转[LOCF])时,总胰岛素抗体水平(结合百分比)与疗效结果(糖化血红蛋白[HbA1c],基础胰岛素剂量和总低血糖率调整1年)之间的关系。检测的定量检测限。对基线HbA1c、研究开始时的基础胰岛素以及研究前二甲双胍或阿卡波糖的使用进行调整后,终点指标(HbA1c、基础胰岛素剂量或总低血糖率)与终点抗体水平之间关系的偏相关指标。只有终点抗体水平和基线值不缺失,且至少有一个应答变量基线后值不缺失的患者被纳入分析。IGlar,甘精胰岛素;LOCF,最后一次观察;:LY IGlar,LY2963016甘精胰岛素
结论:LY IGlar和IGlar的免疫原性相似,两种胰岛素的抗胰岛素抗体水平较低。没有观察到抗体水平或泪液状态与临床结果之间的关联。
原文出处:Wang W, Song X, Lou Y,et al.Immunogenicity of LY2963016 insulin glargine and Lantus® insulin glargine in Chinese patients with type 1 or type 2 diabetes mellitus.Diabetes Obes Metab 2022 06;24(6)
Diabetologia:脑脊液葡萄糖水平升高和糖尿病与神经毒性多元醇通路的激活有关。
![]() 0
2022-05-11
点击查看
0
2022-05-11
点击查看
JCEM:体重指数和腰臀比的蛋白质组学特征及其在糖尿病发病中的作用
![]() 0
2022-05-12
点击查看
0
2022-05-12
点击查看
Neurol Neuroimmunol Neuroinflamm:糖尿病是抗自身抗体阳性的淋巴结病的危险因素
![]() 0
2022-05-14
点击查看
0
2022-05-14
点击查看

专访清华大学程功教授:受糖尿病患者易感新冠启发,发现广谱抗新冠代谢物
![]() 0
2022-05-11
点击查看
0
2022-05-11
点击查看

Nat Med:两项多格列艾汀的III期研究结果公布,降糖作用显著且长期持续
![]() 0
2022-05-14
点击查看
0
2022-05-14
点击查看

一朝感染终生复发!慕尼黑学者:这种攻陷几十亿人口的病毒竟还会增加糖尿病风险
![]() 0
2022-05-16
点击查看
0
2022-05-16
点击查看