Mobocertinib(TAK-788,曾用代号AP32788)是武田制药研发的一款小分子EGFR/HER2抑制剂,日前美国FDA已授予突破性疗法认定(BTD)药物资格。2020年4月28日,AACR年会报道了1/2期临床试验(NCT02716116)结果。
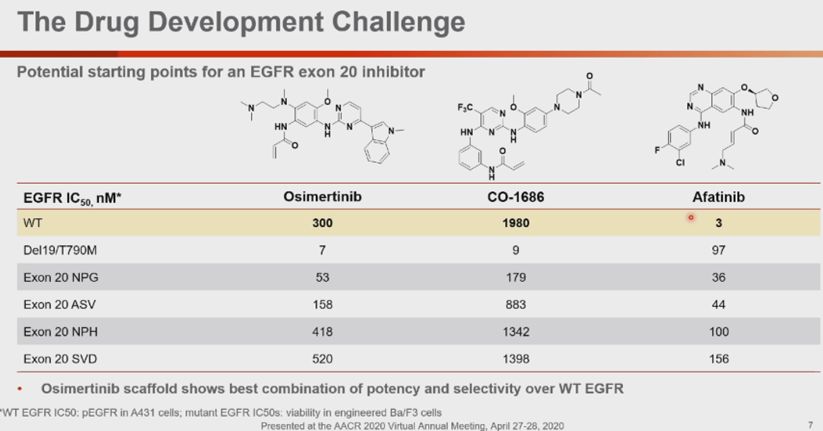
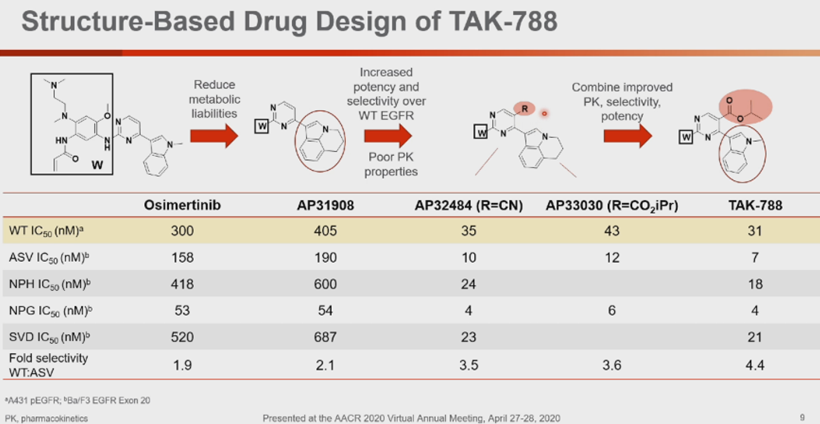
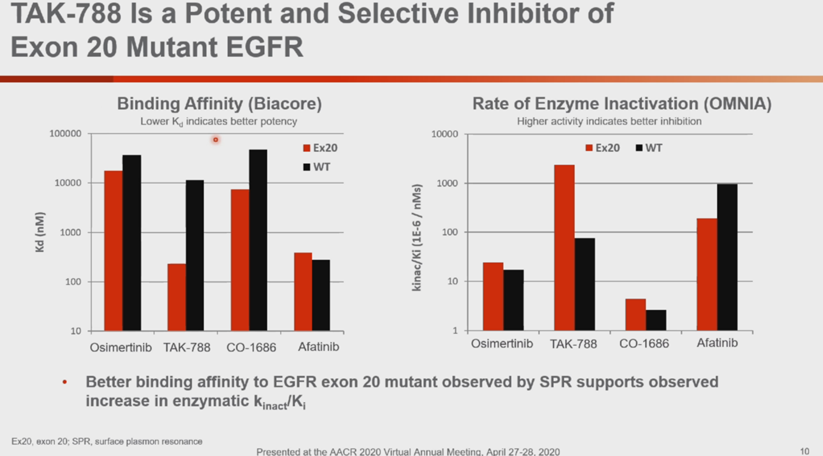
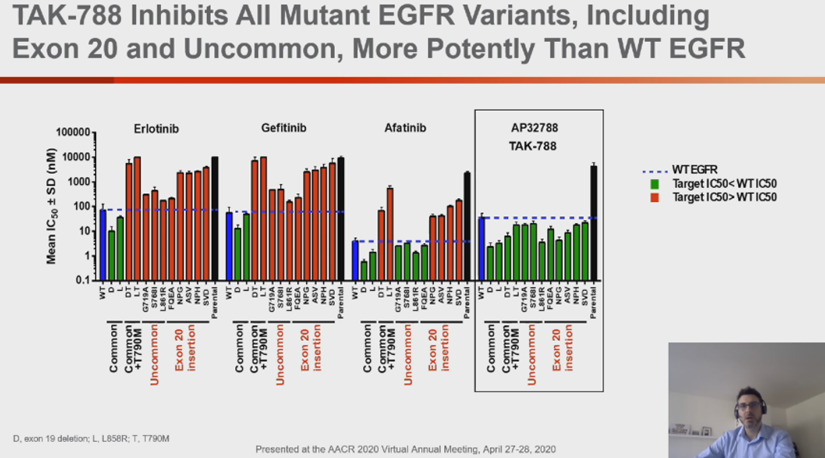
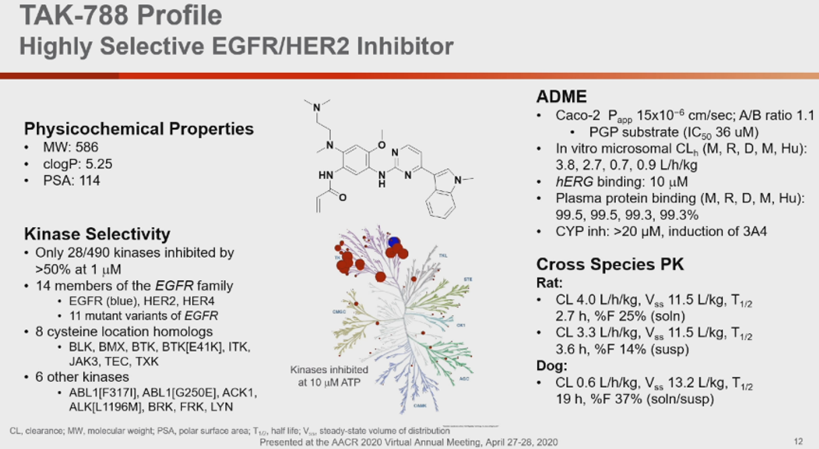
Mobocertinib基于奥希替尼的骨架核心改进,大大提高了对EGFR 20外显子插入突变的活性,需注意的是,幻灯片第12页中的分子式是错的,应该是图1所示。
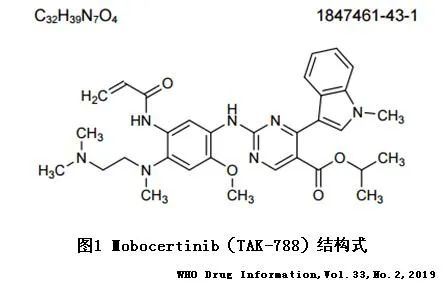
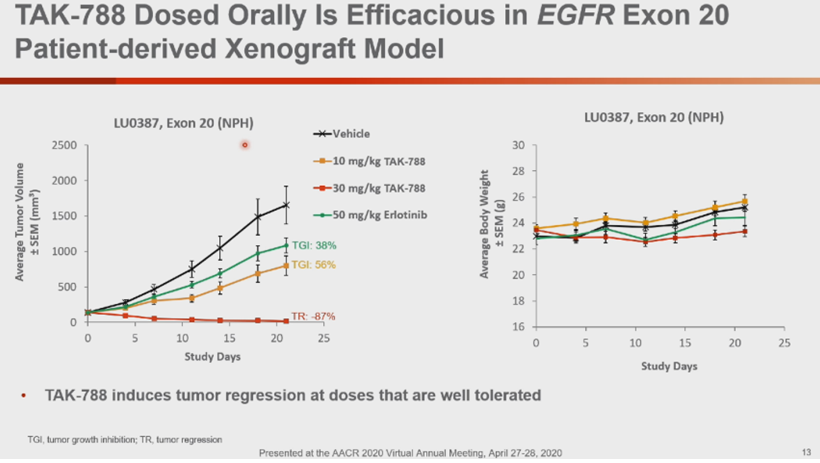
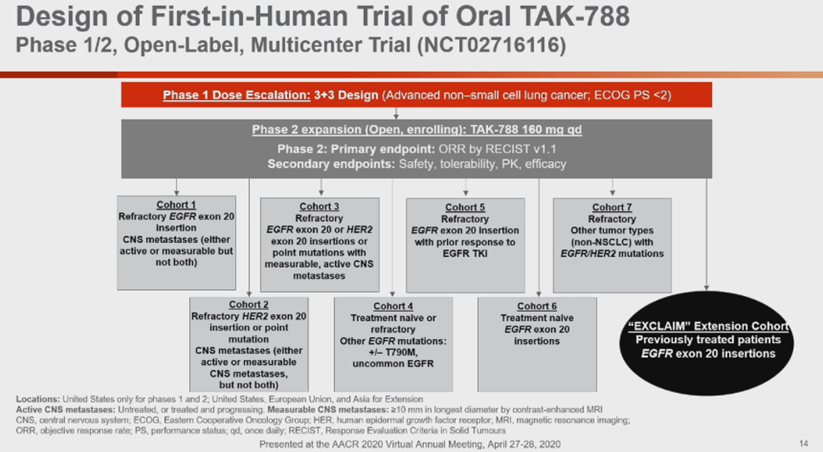
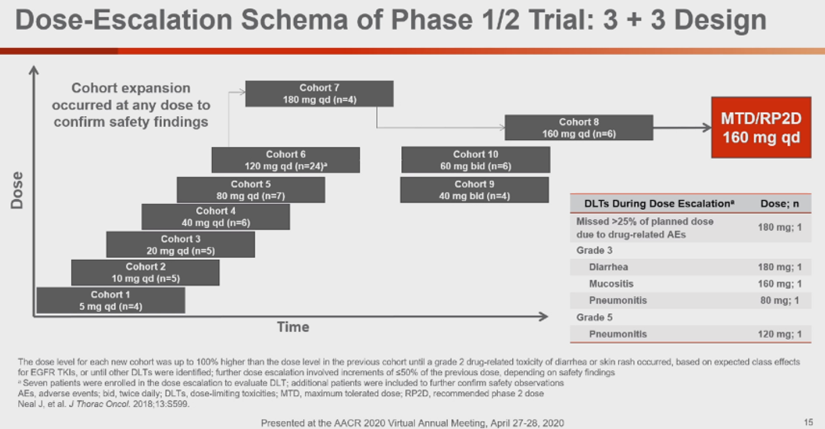
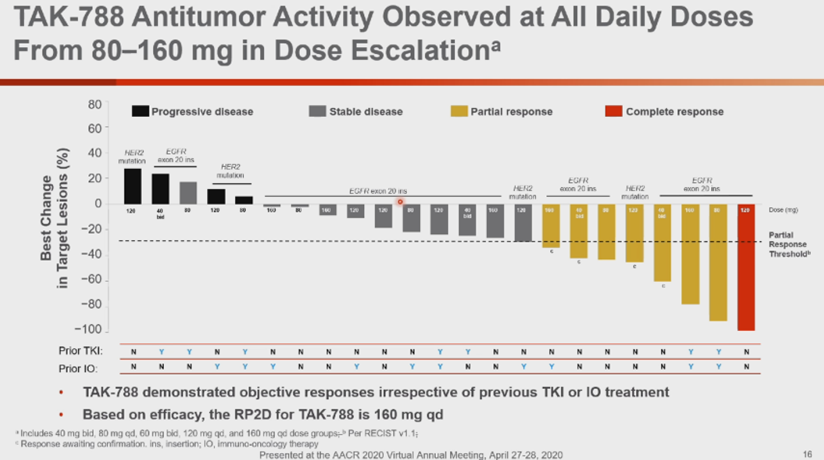
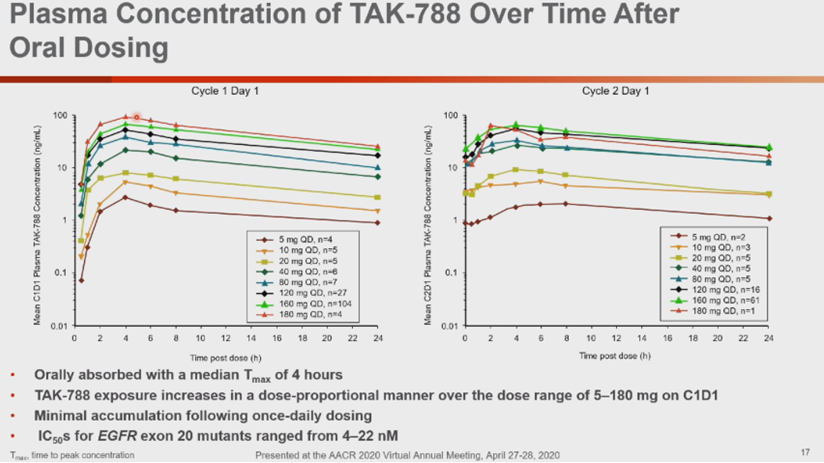
Mobocertinib的2期标准剂量(同时也是最大耐受剂量)为160mg每天一次,口服,是否空腹影响很小。 28例可供评估的EGFR 20外显子插入突变经治NSCLC患者,客观有效率43%,中位无进展生存期7.3月。
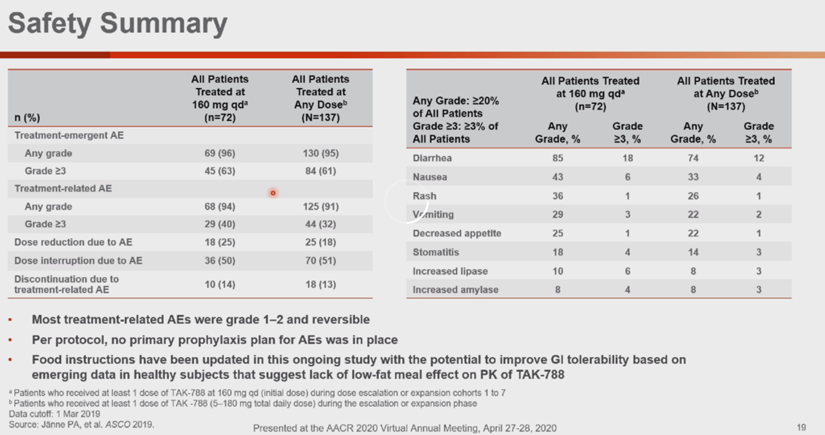
Mobocertinib 160mg每天一次剂量组的多数不良反应为1-2级,常见不良反应有腹泻(85%,3级以上18%),恶心(43%,3级以上6%),皮疹(36%,3级以上1%),呕吐(29%,3级以上3%),食欲下降(25%,3级以上1%),口腔炎(18%,3级以上4%),脂肪酶升高(10%,3级以上6%)和淀粉酶升高(8%,3级以上4%)。因不良反应,50%的患者暂停过药物,25%的患者药物减量,14%的患者永久停药。
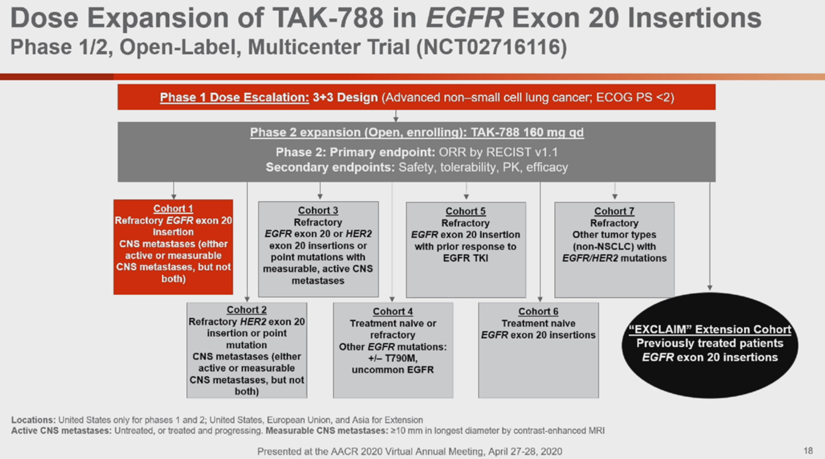
Mobocertinib对比培美曲塞联合铂类一线治疗EGFR 20外显子插入突变复发性或晚期NSCLC患者的三期临床试验(NCT04129502)已经开展(美国4个临床点,西班牙1个)。





AACR 2020:免疫联合治疗在三阴性乳腺癌治疗中获突破,OS高达16个月
![]() 0
2020-04-29
点击查看
0
2020-04-29
点击查看

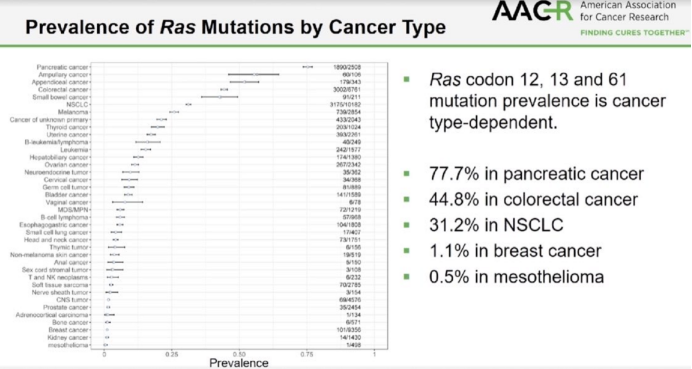
AACR 2020:KRAS突变在不同癌肿的发生率
![]() 0
2020-04-29
点击查看
0
2020-04-29
点击查看
AACR 2020:基因治疗肾细胞癌获突破,DCR可达75%!
![]() 0
2020-04-29
点击查看
0
2020-04-29
点击查看

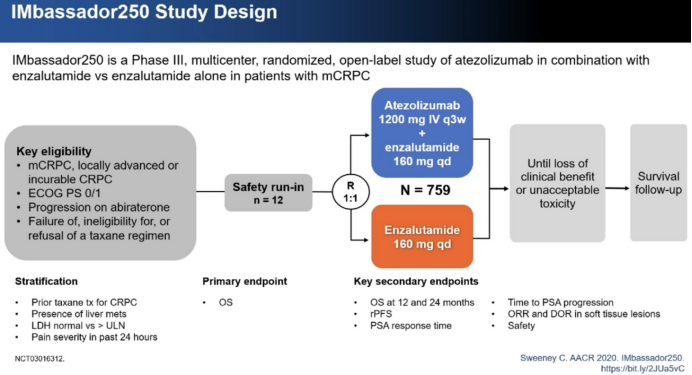
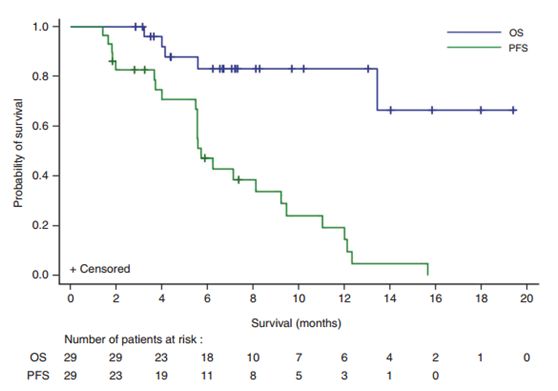
AACR 2020:PD-L1+恩杂鲁胺治疗去势抵抗性前列腺癌,未获成功
![]() 0
2020-04-29
点击查看
0
2020-04-29
点击查看
AACR 2020:肝内胆管癌的FGFR2一个新型突变被发现
![]() 0
2020-04-29
点击查看
0
2020-04-29
点击查看
AACR 2020:蔡红兵教授分享COVID-19疫情癌症患者的数据
![]() 0
2020-04-29
点击查看
0
2020-04-29
点击查看
